Содержание
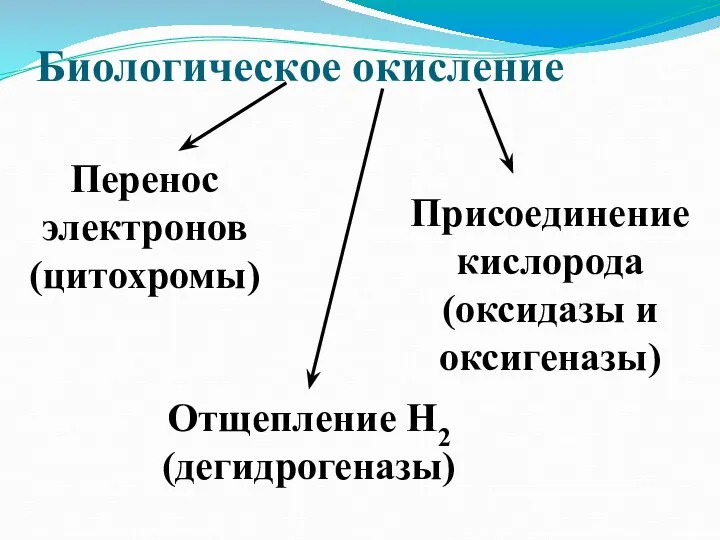
- 2. Биологическое окисление Перенос электронов (цитохромы) Присоединение кислорода (оксидазы и оксигеназы) Отщепление Н2 (дегидрогеназы)
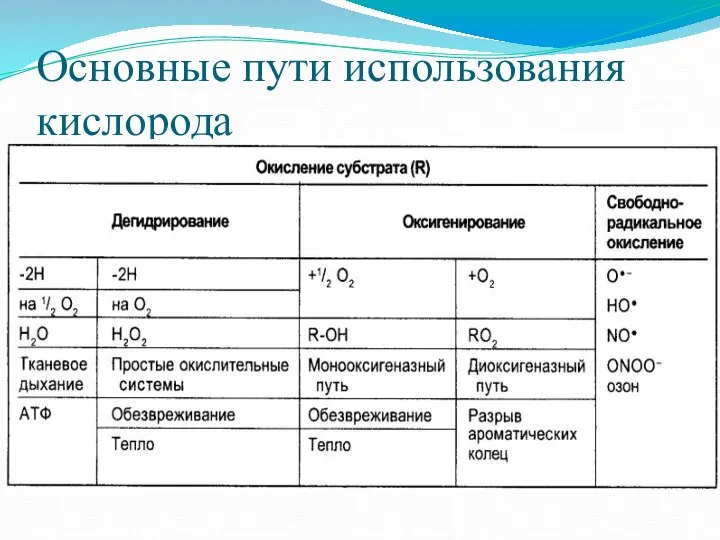
- 3. Основные пути использования кислорода
- 4. В биохимии и клеточной биологии под тканевым (клеточным) дыханием понимают молекулярные процессы, в результате которых происходит
- 5. Процесс тканевого дыхания оценивают с помощью дыхательного коэффициента: RQ = число молей образованного СО2 / число
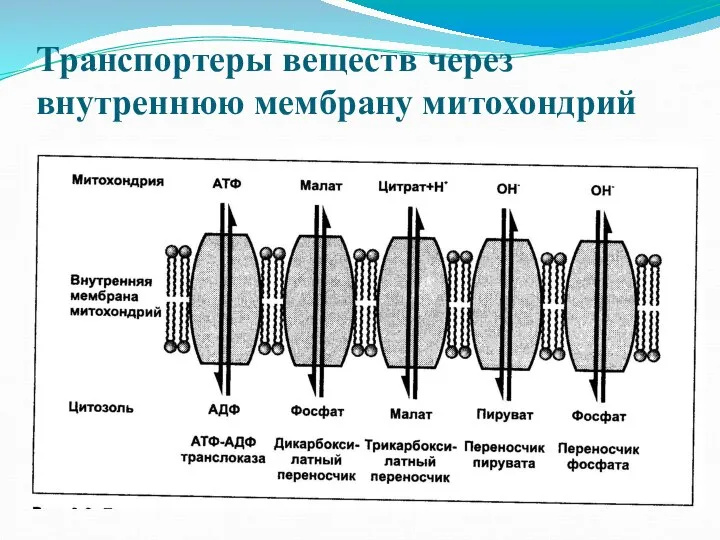
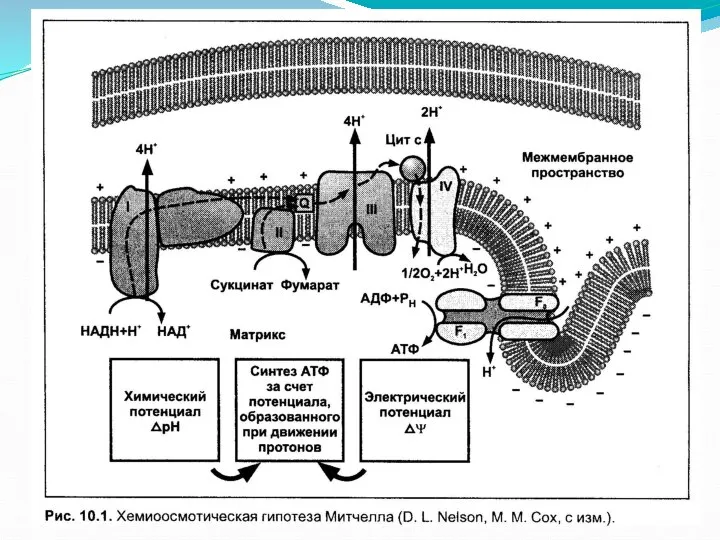
- 7. Транспортеры веществ через внутреннюю мембрану митохондрий
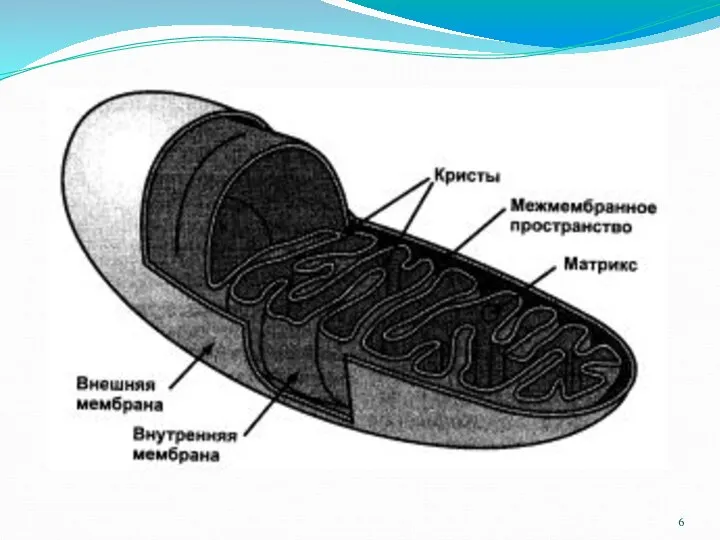
- 8. Функциональная компартментализации митохондрий 1. Внешняя мембрана MX отграничивает внутреннее пространство; проницаема для О2 и ряда низкомолекулярных
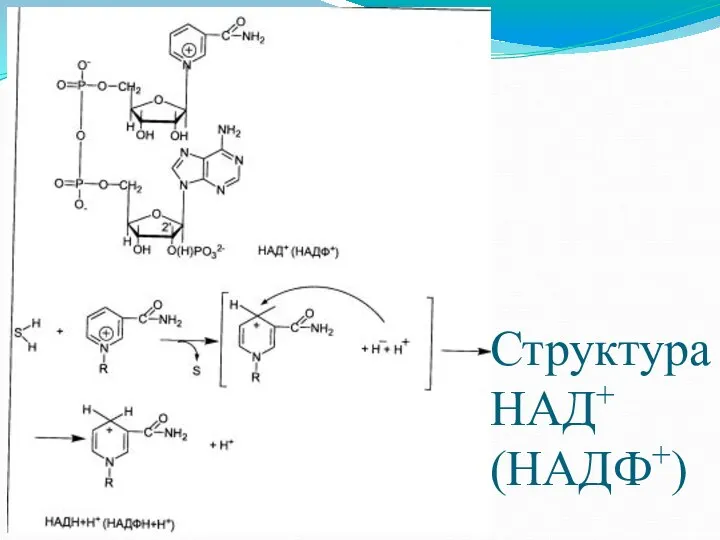
- 10. Структура НАД+ (НАДФ+)
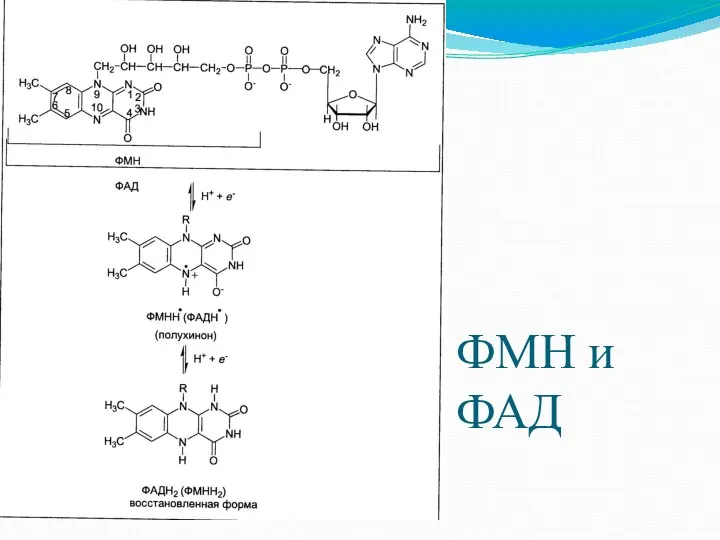
- 11. ФМН и ФАД
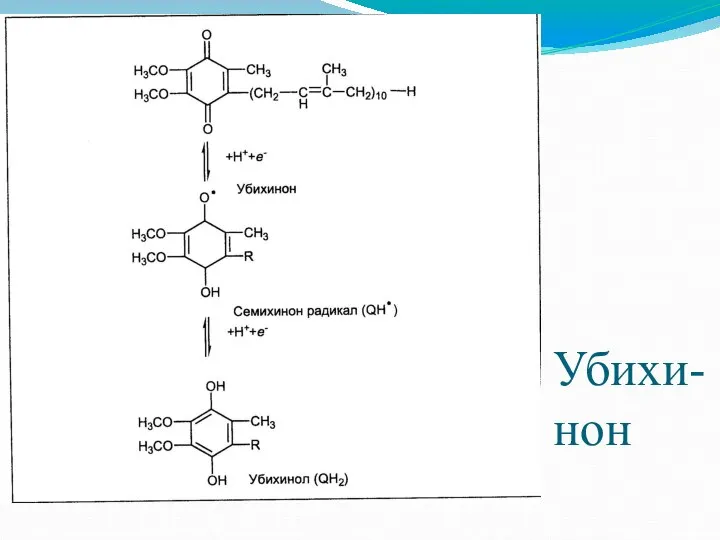
- 12. Убихи-нон
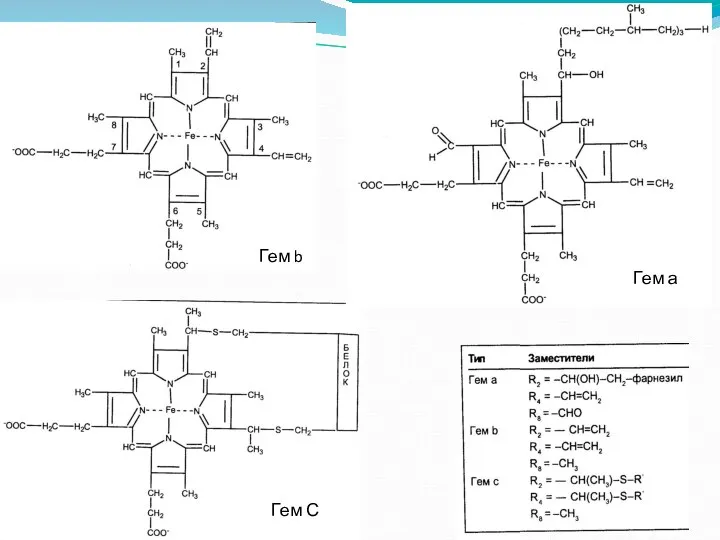
- 13. Гем b Гем С Гем а
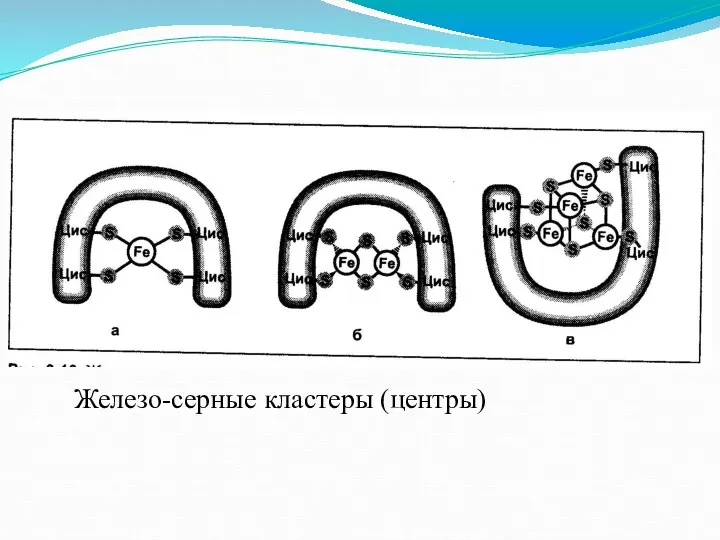
- 14. Железо-серные кластеры (центры)
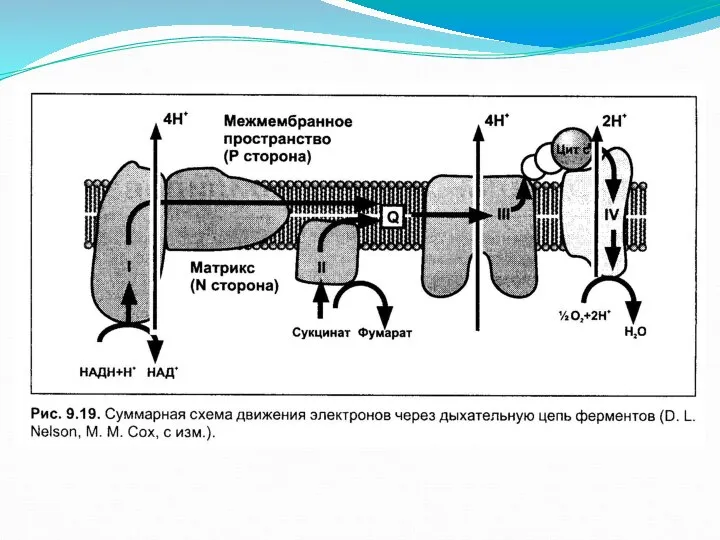
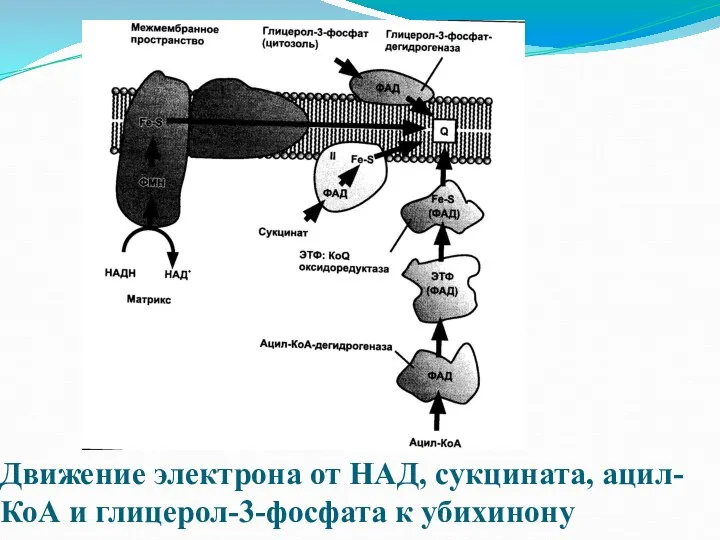
- 16. Движение электрона от НАД, сукцината, ацил-КоА и глицерол-3-фосфата к убихинону
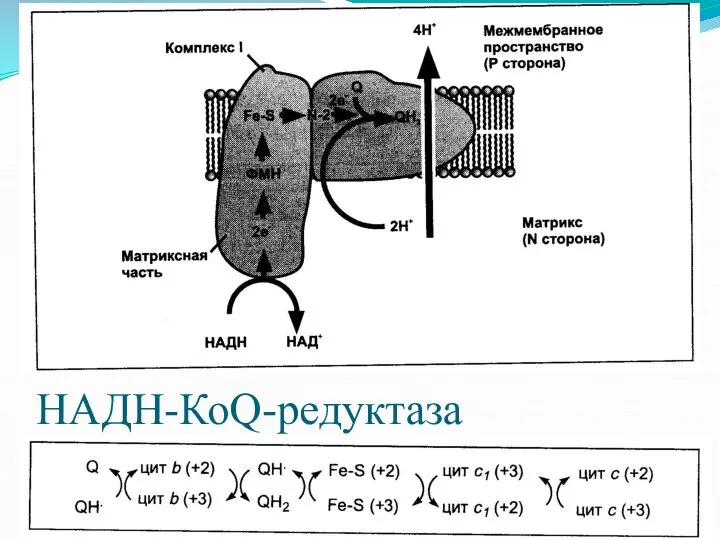
- 17. НАДН-КоQ-редуктаза
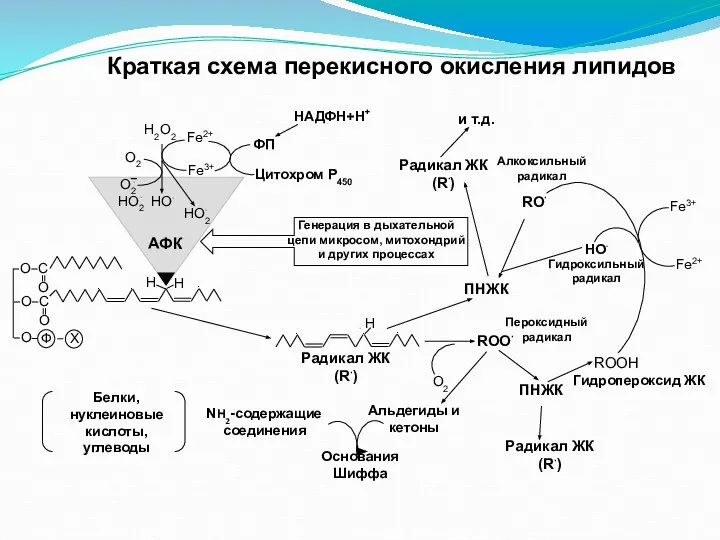
- 25. Краткая схема перекисного окисления липидов Н2О2 О2 Fe2+ Fe3+ ФП Цитохром Р450 НАДФН+Н+ АФК О О
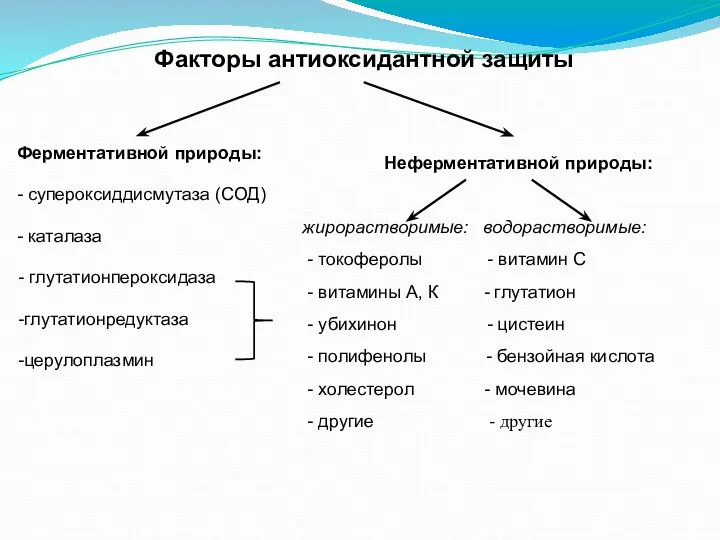
- 26. Факторы антиоксидантной защиты Ферментативной природы: - супероксиддисмутаза (СОД) - каталаза глутатионпероксидаза глутатионредуктаза церулоплазмин Неферментативной природы: жирорастворимые:
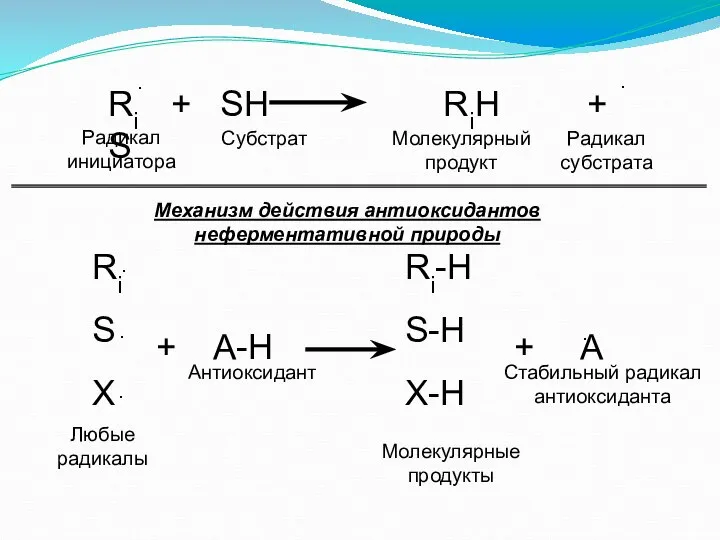
- 27. Ri + SH RiH + S ∙ Радикал инициатора Субстрат Молекулярный продукт Радикал субстрата Ri S
- 29. Скачать презентацию






 Поликонденсация. Фенолформальдегидные смолы
Поликонденсация. Фенолформальдегидные смолы Соединения алюминия
Соединения алюминия Фізичні методи дослідження хімічних сполук
Фізичні методи дослідження хімічних сполук Физико-химический процесс элелктролиз. (11 класс)
Физико-химический процесс элелктролиз. (11 класс) Репликация ДНК
Репликация ДНК Будова, роль та значення полісахаридів у метаболізмі рослинної клітини
Будова, роль та значення полісахаридів у метаболізмі рослинної клітини Перетворення карбонатів та гідрокарбонатів у природі,утворення сталактитів і сталагмітів. Кальцій карбонат у складі черепашо
Перетворення карбонатів та гідрокарбонатів у природі,утворення сталактитів і сталагмітів. Кальцій карбонат у складі черепашо Фосфор. Получение. Химические свойства
Фосфор. Получение. Химические свойства В мире кристаллов
В мире кристаллов Строение вещества. Химические элементы
Строение вещества. Химические элементы Химическая связь. Электроотрицательность. Ковалентная связь
Химическая связь. Электроотрицательность. Ковалентная связь Химический диктант
Химический диктант Проверьте себя: Электроотрицательность - это ……. Ковалентная полярная связь – это ….. Ковалентная неполярная связь – это ….. Элемент, имеющий самое высокое значение электроотрицательности ……. Какую кристаллическую решетку имеют вещества с ковалентны
Проверьте себя: Электроотрицательность - это ……. Ковалентная полярная связь – это ….. Ковалентная неполярная связь – это ….. Элемент, имеющий самое высокое значение электроотрицательности ……. Какую кристаллическую решетку имеют вещества с ковалентны Причина отказа повреждений технологического оборудования и принятия мер по их устранению установки производства газовой серы
Причина отказа повреждений технологического оборудования и принятия мер по их устранению установки производства газовой серы Моль. Молярная масса
Моль. Молярная масса Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы
Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы Жидкие системы
Жидкие системы Материаловедение
Материаловедение Введение в химию биологически активных веществ. (Тема 1)
Введение в химию биологически активных веществ. (Тема 1) Задания на ЕГЭ
Задания на ЕГЭ Дифузія у побуті
Дифузія у побуті Осадительное титрование. Сущность метода
Осадительное титрование. Сущность метода Ацетилен и его гомологи
Ацетилен и его гомологи Аллотропия. Аллотропные модификации
Аллотропия. Аллотропные модификации Органічні сполуки в побуті
Органічні сполуки в побуті 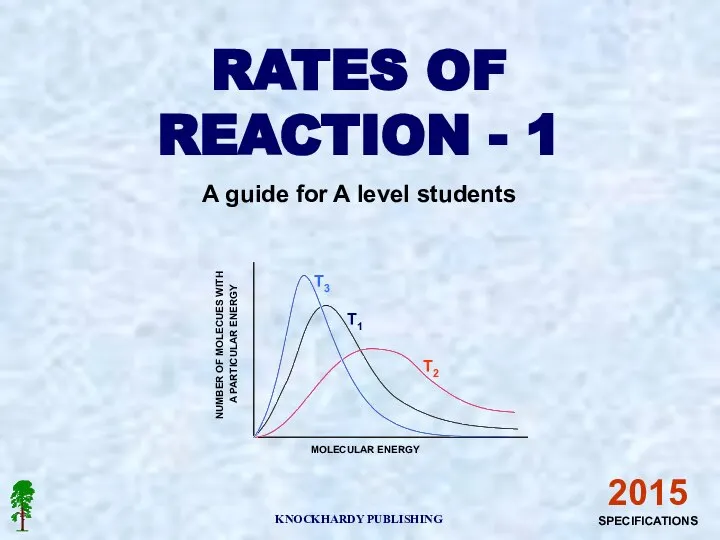 Number of molecues with a particular energy
Number of molecues with a particular energy Химический элемент платина
Химический элемент платина Беттiк құбылыстар, олардың ағзадағы маңызы. Адсорбция
Беттiк құбылыстар, олардың ағзадағы маңызы. Адсорбция