Содержание
- 3. Элелктролиз Это физико-химический процесс, протекающий в растворе или расплаве электролита, при пропускании через него электрического тока.
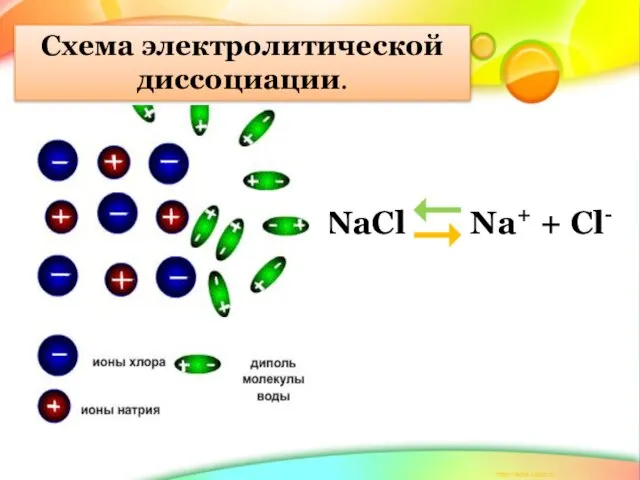
- 4. NaCl Na+ + Cl- Схема электролитической диссоциации.
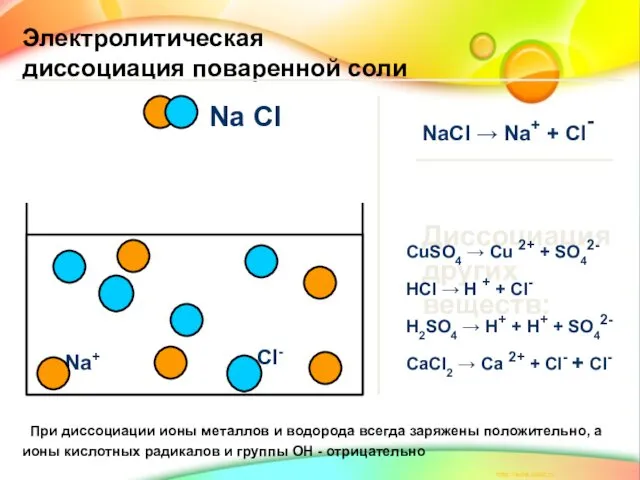
- 5. Na Cl Na+ Cl- Электролитическая диссоциация поваренной соли NaCl → Na+ + Cl- Диссоциация других веществ:
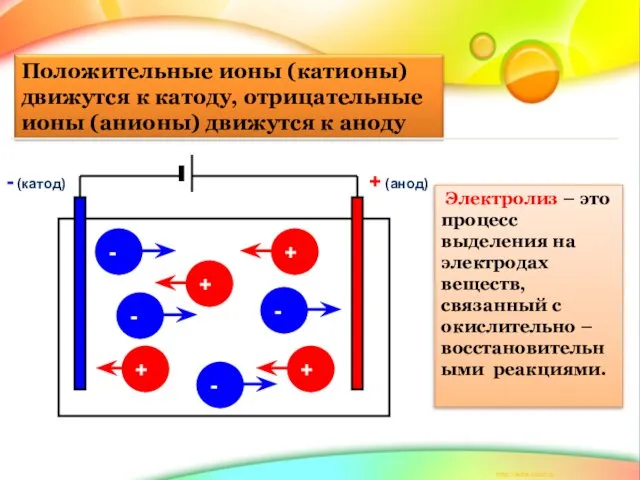
- 6. + (анод) - (катод) + + + - - - + - Электролиз – это процесс
- 7. Электрохимический ряд напряжений металлов Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Zn→Cr→Fe→Cd→Co→Ni→Sn→Pb→H→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au
- 8. Исследовал электролиз и открыл его законы английский физик Майкл Фарадей в 1834 году Майкл Фарадей (1791
- 9. Второй закон электролиза При одинаковом количестве электричества (электрическом заряде, прошедшем через электролит) масса вещества, выделившегося при
- 12. Гальваностегия это процесс, который позволяет покрыть изделие слоем (плёнкой) благородного металла защитить его от коррозии, повысить
- 13. Покрытие предметов слоем благородного металла
- 16. это получение электролитическим способом более толстых отложений (до нескольких миллиметров). ГАЛЬВАНОПЛАСТИКА Копия барельефа, полученная методом гальванопластики
- 17. Изготовление медалей, монет.
- 18. Произведения искусства: Барельефы для: Исаакиевского собора
- 19. Петропавловского собора
- 20. Эрмитажа
- 21. Зимнего дворца
- 22. Большого театра
- 23. Медные клише для типографии
- 24. Пресс-формы из пластмассы, резины, металла
- 25. Пресс-формы из пластмассы, резины, металла
- 27. Скачать презентацию





















 Компания «Родник здоровья»
Компания «Родник здоровья» Электродный потенциал. Критерий протекания окислительно-восстановительных реакций
Электродный потенциал. Критерий протекания окислительно-восстановительных реакций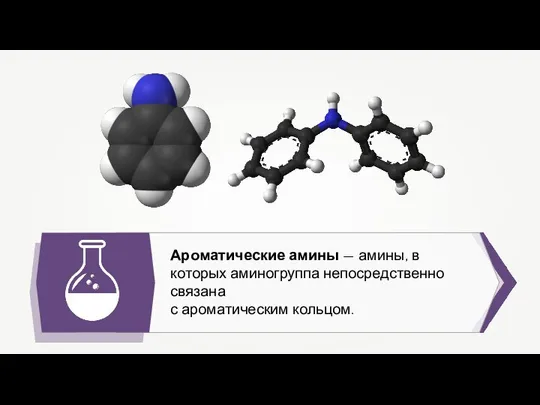 Ароматические амины
Ароматические амины Электропроводность растворов электролитов. Числа переноса
Электропроводность растворов электролитов. Числа переноса Полимерные растворы – условия образования
Полимерные растворы – условия образования Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией
Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией Семинар на тему Природные источники углеводородов и их переработка
Семинар на тему Природные источники углеводородов и их переработка Вода и растворы. Лекция 3
Вода и растворы. Лекция 3 Энергия алмасудың бірінші сатысы: күрделі заттардың арнайы жолдармен ыдырап, универсалды аралық өнімдерге айналуы
Энергия алмасудың бірінші сатысы: күрделі заттардың арнайы жолдармен ыдырап, универсалды аралық өнімдерге айналуы Митохондрии и пластиды
Митохондрии и пластиды Склеивание древесины. Клеи
Склеивание древесины. Клеи Минералы и горные породы Крыма
Минералы и горные породы Крыма Краун-эфиры
Краун-эфиры Углеводы. Дисахариды и полисахариды
Углеводы. Дисахариды и полисахариды Химический источник электрического тока
Химический источник электрического тока Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть
Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть  Застосування нових сучасних матеріалів з оригінльними властивостями
Застосування нових сучасних матеріалів з оригінльними властивостями  Внеклассное мероприятие по химии. Своя игра
Внеклассное мероприятие по химии. Своя игра Основы химической термодинамики
Основы химической термодинамики Роль химии в жизни человека
Роль химии в жизни человека Амфотерные неорганические и органические соединения МОУ «Гатчинская СОШ №2» Учитель химии: Г.Г.Павлова Учитель инфор
Амфотерные неорганические и органические соединения МОУ «Гатчинская СОШ №2» Учитель химии: Г.Г.Павлова Учитель инфор К 180-летию со дня рождения Д.И. Менделеева
К 180-летию со дня рождения Д.И. Менделеева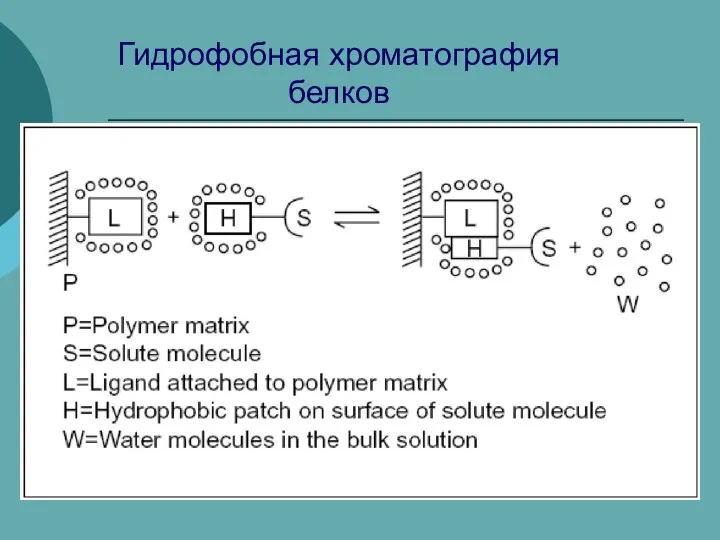 Гидрофобная хроматография белков
Гидрофобная хроматография белков Алюминий и его сплавы. Назначение
Алюминий и его сплавы. Назначение Классификация и номенклатура органических соединений. (Лекция 1)
Классификация и номенклатура органических соединений. (Лекция 1) Научные основы процессов разделения
Научные основы процессов разделения Chemical bonds
Chemical bonds Материаловедение
Материаловедение