Понятие электрохимии. Процессы на границе металл – раствор. Электродные потенциалы. Гальванические элементы. Уравнение Нернста
Содержание
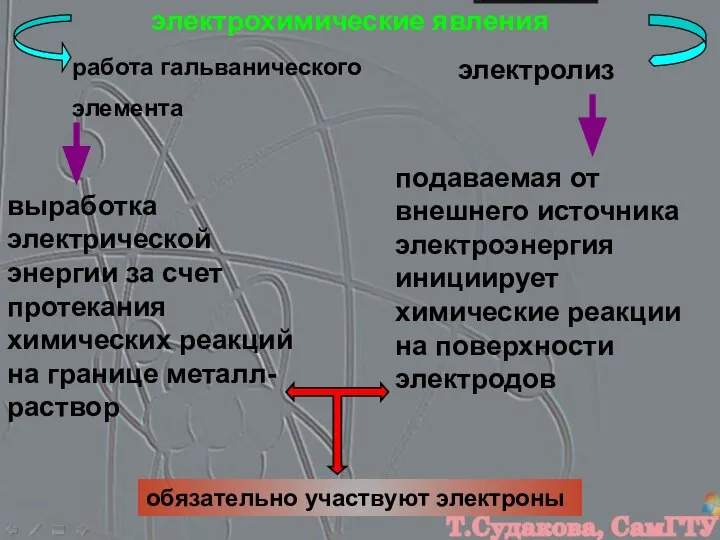
- 2. электрохимические явления работа гальванического элемента электролиз выработка электрической энергии за счет протекания химических реакций на границе
- 3. «электричество» - от греческого «electron», т.е. янтарь – вещество, которое при трении электризуется электрохимия берет начало
- 4. Гальванический элемент (ГЭ) – устройство, преобразующее энергию химических реакций в электрическую апельсиновая батарейка электроды ЭЛЕКТРОД -
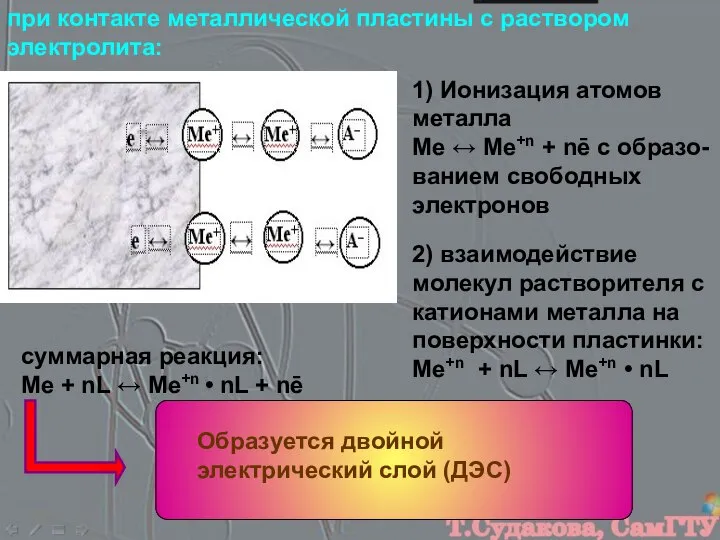
- 5. 2) взаимодействие молекул растворителя с катионами металла на поверхности пластинки: Ме+n + nL ↔ Ме+n •
- 6. ДЭС обуславливает возникновение электродного потенциала – разности электростатических потенциалов между электродом и находящимся с ним в
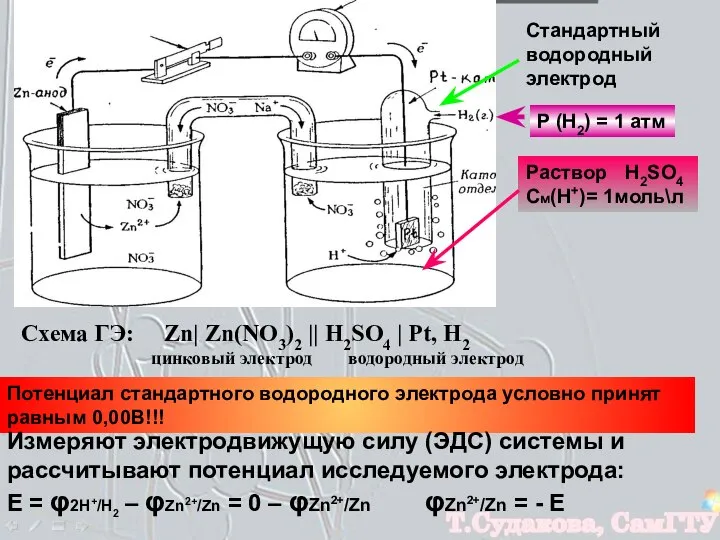
- 7. Стандартный водородный электрод Р (Н2) = 1 атм Раствор H2SO4 См(Н+)= 1моль\л Потенциал стандартного водородного электрода
- 8. Стандартные условия: 298К, концентрация окисленной формы 1 моль\л ΔG0 = - nFϕ0
- 9. уравнение Нернста: φ=φ0+(RT/nF)•lnKp=φ0+(RT/nF)• ln([Ox]/[Red]) где φ – потенциал электрода в нестандартных условиях; φ0- стандартный электродный потенциал;
- 10. Для происходящей на поверхности металла обратимой реакции Ме(к) Ме+n (р-р) + nē Кр = [Ме+n]/[Ме], но
- 11. Гальванический элемент – устройство, преобразующее энергию химических реакций в электрическую энергию.
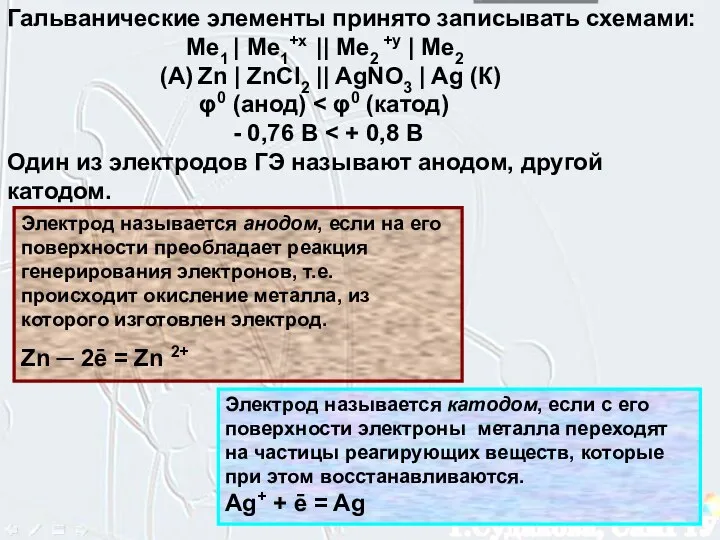
- 12. Гальванические элементы принято записывать схемами: Ме1 | Ме1+х || Ме2 +y | Ме2 (А) Zn |
- 13. Вольтов столб, Zn и Ag
- 14. ТИПЫ ГЭ (ХИТ) 1) первичные ГЭ – это элементы, в которых происходит необратимая ОВР и дальнейшее
- 15. 2) вторичные ГЭ – аккумуляторы- элементы, работа которых основана на обратимой ОВР и процессы зарядки и
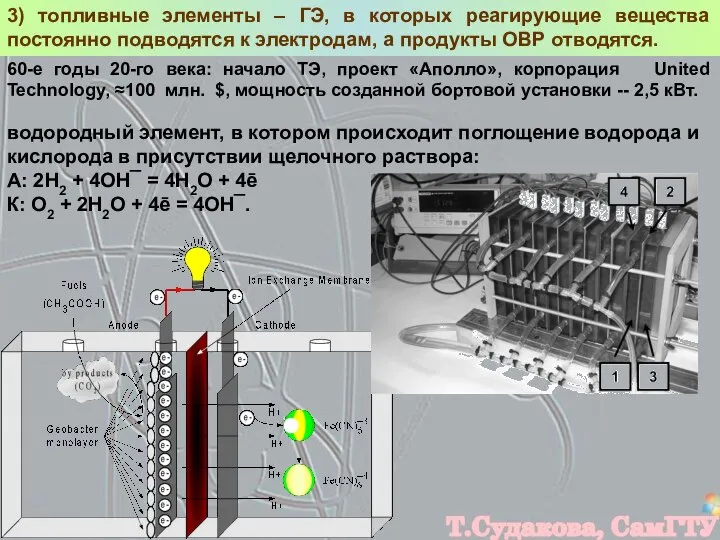
- 16. 3) топливные элементы – ГЭ, в которых реагирующие вещества постоянно подводятся к электродам, а продукты ОВР
- 17. ЭЛЕКТРОЛИЗ Потенциал разложения – это минимальная необходимая разность потенциалов, при которой начинается электролиз данного вещества. φ0разл.
- 18. Примеси сырья SiO2 и Fe2O3 необходимо удалять, иначе они будут подвергаться электролизу вместе с Al2O3 Условие
- 19. Правила разрядки частиц на электродах при электролизе: 1) на катоде в первую очередь восстанавливается вещество с
- 20. электролиз раствора NaCl на инертных электродах: 1) диссоциация NaCl = Na+ + Cl─ 2) движение ионов
- 21. Количественные соотношения при электролизе были установлены М. Фарадеем и сформулированы им в виде законов электролиза: Количество
- 22. Поляризация (Δφ) – явление отклонения значения электродного потенциала от равновесного под действием проходящего электрического тока. Величина
- 23. Применение электролиза: 1. Получение Al, Cl2, F2, NaOH, O2, H2, щелочных и щелочно-земельных металлов, некоторых органических
- 25. Скачать презентацию




![уравнение Нернста: φ=φ0+(RT/nF)•lnKp=φ0+(RT/nF)• ln([Ox]/[Red]) где φ – потенциал электрода в нестандартных](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405341/slide-8.jpg)











 Химия сверхкритических жидкостей
Химия сверхкритических жидкостей Презентация Химический состав мороженного
Презентация Химический состав мороженного Аминокислоты
Аминокислоты Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Дмитрий Иванович Менделеев (1834–1907)
Дмитрий Иванович Менделеев (1834–1907) Яковлева Татьяна Алексеевна Ярославль, 2009 г.
Яковлева Татьяна Алексеевна Ярославль, 2009 г.  Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола
Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола Гидролиз органических веществ
Гидролиз органических веществ Лекарственная форма порошки
Лекарственная форма порошки Математический аппарат квантовой механики
Математический аппарат квантовой механики Жиры (триглицериды)
Жиры (триглицериды) Аттестационная работа. Способ формирования метапредметных результатов обучения при обучении химии в условиях реализации ФГОС
Аттестационная работа. Способ формирования метапредметных результатов обучения при обучении химии в условиях реализации ФГОС Субстраты для гидропоники
Субстраты для гидропоники Альдегидтер
Альдегидтер Anionic Polymerization
Anionic Polymerization Воздух
Воздух Теория строения химических соединений А. М. Бутлерова
Теория строения химических соединений А. М. Бутлерова Дисперсные системы (продолжение)
Дисперсные системы (продолжение) Диоксины, глобальные экотоксиканты
Диоксины, глобальные экотоксиканты Загальна характеристика рослинних кормiв. (Тема 1)
Загальна характеристика рослинних кормiв. (Тема 1) Технология производства хлорбензола
Технология производства хлорбензола Химиялық формула
Химиялық формула БЕРИЛИЙ, МАГНИЙ И ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
БЕРИЛИЙ, МАГНИЙ И ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ оксиды - св-ва — уч-ся
оксиды - св-ва — уч-ся Алкиндер
Алкиндер Кислотные дожди
Кислотные дожди Фосфор и его соединения
Фосфор и его соединения Твердоконтактные электрохимические платформы для потенциометрических измерений
Твердоконтактные электрохимические платформы для потенциометрических измерений