Содержание
- 2. Цель: изучить свойства фосфорной кислоты, как электролита.
- 3. Электролиты Электролиты – это вещества, водные растворы или расплавы которых проводят электрический ток. Вещества с ионной
- 4. Диссоциация электролитов Диссоциация - обратимый процесс: параллельно с распадом молекул на ионы (диссоциация) протекает процесс соединения
- 5. Электролиты Сильные электролиты – химические соединения, которые при растворении в воде полностью распадаются на ионы. Примеры:
- 7. Скачать презентацию




 Физические свойства металлов
Физические свойства металлов Тема урока: Аллотропия Презентацию выполнил учитель химии Стрейф Александра
Тема урока: Аллотропия Презентацию выполнил учитель химии Стрейф Александра  Лекция на тему: «Витамины»
Лекция на тему: «Витамины» Вклад ученых–химиков в победу над фашизмом в годы Великой Отечественной Войны
Вклад ученых–химиков в победу над фашизмом в годы Великой Отечественной Войны Серная кислота. (9 класс)
Серная кислота. (9 класс) Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения
Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия
Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия Коррозия металлов
Коррозия металлов Биохимическая трансформация веществ (3)
Биохимическая трансформация веществ (3) Металлы
Металлы Приготовление раствора сахара
Приготовление раствора сахара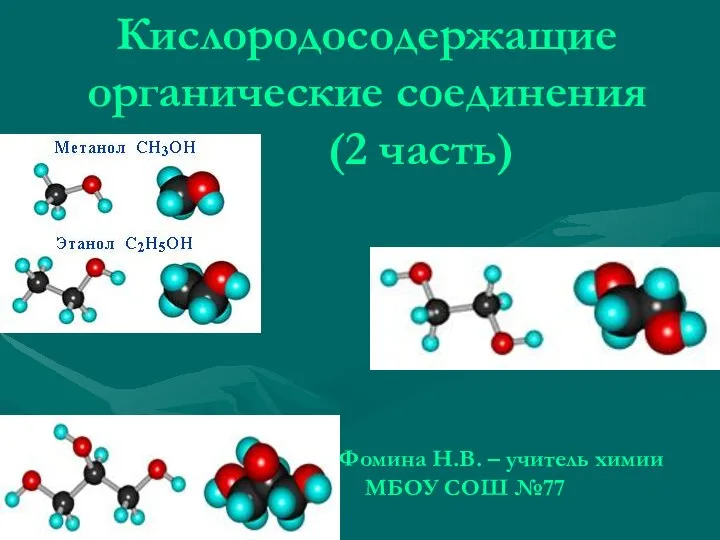 Кислородосодержащие органические соединения (2 часть)
Кислородосодержащие органические соединения (2 часть) Силикатная промышленность Подготовила ученица 9 А класса Семёнова Екатерина
Силикатная промышленность Подготовила ученица 9 А класса Семёнова Екатерина Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений
Особенности строения, реакционной способности и методы синтеза азотсодержащих соединений Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения Горные породы и минералы. Камни-самоцветы
Горные породы и минералы. Камни-самоцветы Металлы. Урок – обобщения
Металлы. Урок – обобщения Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Биохимия. Ферменты (Лекция№2)
Биохимия. Ферменты (Лекция№2) Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой
Комплексные соединения хлоридов европия и гадолиния с салициловой кислотой Соли.
Соли. Органические вещества в быту
Органические вещества в быту  Производство органических препаратов ароматического ряда
Производство органических препаратов ароматического ряда Cинтетичні миючі засоби і їхній вплив на людину
Cинтетичні миючі засоби і їхній вплив на людину  Характеристика элемента по его положению в периодической системе. Урок 33
Характеристика элемента по его положению в периодической системе. Урок 33 Презентация по Химии "Презентация Пищевые цепи" - скачать смотреть
Презентация по Химии "Презентация Пищевые цепи" - скачать смотреть  Физическая химия дисперсных систем. Коллоидные растворы
Физическая химия дисперсных систем. Коллоидные растворы Щелочи
Щелочи