Содержание
- 2. Раствор — это однородная система, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.
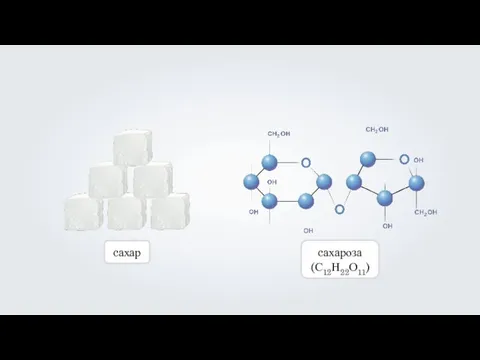
- 3. cахар cахароза (С12Н22О11)
- 5. Отношение массы растворённого вещества к общей массе раствора называют массовой долей растворённого вещества.
- 6. 20 5 70 мл 200 мл \ Проведём опыт
- 7. + = 25 г 70 мл \ Проведём опыт
- 8. Дано: V(H2O) = 70 мл Решение. w(С12Н22О11) — ? m(p-p) = m(С12Н22О11) + m(Н2О). Ответ: w(С12Н22О11)
- 9. Дано: NA = 6 ∙ 1023 моль–1 Решение. N(мол. сах.) = NA ∙ n(С12Н22О11). N(мол.сах.) —
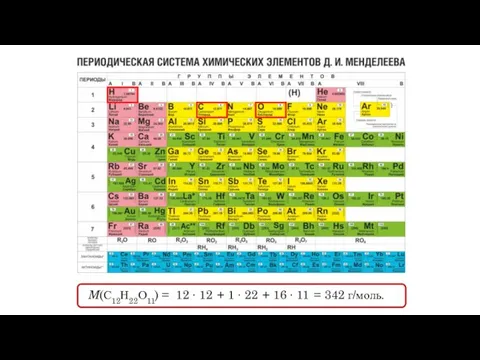
- 10. M(С12Н22О11) = 12 ∙ 12 + 1 ∙ 22 + 16 ∙ 11 = 342 г/моль.
- 11. Дано: NA = 6 ∙ 1023 моль–1 Решение. N(мол. сах.) = NA ∙ n(С12Н22О11). N(мол.сах.) —
- 13. Скачать презентацию








 Зелёная химия
Зелёная химия Электролитическая диссоциация
Электролитическая диссоциация Биохимия. Введение
Биохимия. Введение «Системно – деятельностный подход как механизм реализации ФГОС нового поколения» обучающий семинар МБОУ «СОШ №15», п.Аршан – 2015г
«Системно – деятельностный подход как механизм реализации ФГОС нового поколения» обучающий семинар МБОУ «СОШ №15», п.Аршан – 2015г Презентация по Химии "Прославившиеся ученые Саратовской области" - скачать смотреть
Презентация по Химии "Прославившиеся ученые Саратовской области" - скачать смотреть  Углеводы. Строение и функции
Углеводы. Строение и функции Кинетика ферментативного катализа. (Лекция 5)
Кинетика ферментативного катализа. (Лекция 5) Разноцветные кристаллы
Разноцветные кристаллы Периодическая Система Д. И. Менделеева в свете учения о строении атома
Периодическая Система Д. И. Менделеева в свете учения о строении атома Ферменты. Свойства ферментов
Ферменты. Свойства ферментов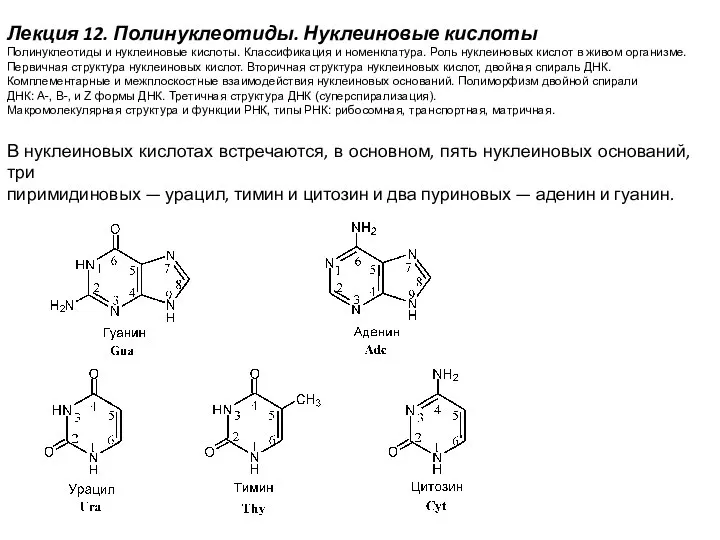 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Методи визначення питомої поверхні
Методи визначення питомої поверхні Азотная кислота и ее соли. Раскаленный уголек, брошенный в концентрированную азотную кислоту, продолжает гореть, при этом выде
Азотная кислота и ее соли. Раскаленный уголек, брошенный в концентрированную азотную кислоту, продолжает гореть, при этом выде Методы составления уравнений окислительно-восстановительных реакций. Лекция №20
Методы составления уравнений окислительно-восстановительных реакций. Лекция №20 Химия функциональных материалов. Адсорбционные материалы. Цеолиты
Химия функциональных материалов. Адсорбционные материалы. Цеолиты Бор (Borum)
Бор (Borum) Биополимеры. Классификация полисахаридов (гликаны)
Биополимеры. Классификация полисахаридов (гликаны) Щелочные металлы — это элементы главной подгруппы I группы
Щелочные металлы — это элементы главной подгруппы I группы Воздух - источник жизни на земле. (3 класс)
Воздух - источник жизни на земле. (3 класс) Металлы в природе. Общие способы их получения.
Металлы в природе. Общие способы их получения. Задача о смесях
Задача о смесях МОЛЬ – ЭТО ТАКОЕ КОЛИЧЕСТВО ВЕЩЕСТВА, В КОТОРОМ СОДЕРЖИТСЯ 6 ∙1023 ЧАСТИЦ (молекул или атомов) ЭТОГО ВЕЩЕСТВА.
МОЛЬ – ЭТО ТАКОЕ КОЛИЧЕСТВО ВЕЩЕСТВА, В КОТОРОМ СОДЕРЖИТСЯ 6 ∙1023 ЧАСТИЦ (молекул или атомов) ЭТОГО ВЕЩЕСТВА. Индивидуальные задания для самостоятельной работы студентов нехимических специальностей
Индивидуальные задания для самостоятельной работы студентов нехимических специальностей Процессы технологии природных энергоносителей и углеродных материалов
Процессы технологии природных энергоносителей и углеродных материалов Технология поликристаллического кремния. Его применение
Технология поликристаллического кремния. Его применение Липидтер, жіктелуі (қарапайым және күрделі липидтер), қызметі, май қышқылдары
Липидтер, жіктелуі (қарапайым және күрделі липидтер), қызметі, май қышқылдары Презентация по Химии "Металлы. Типы сплавов" - скачать смотреть
Презентация по Химии "Металлы. Типы сплавов" - скачать смотреть  Скорость химических реакций Разработка урока по химии 11 класс
Скорость химических реакций Разработка урока по химии 11 класс