Содержание
- 2. Задание 1 Определите степени окисления элементов в соединениях: AlCl3, MgS, Ba3N2, Cu2O, CuO Назовите вещества
- 3. Задание 2 Составьте формулы веществ по названиям Сульфид лития, оксид серы (VI); Хлорид меди (II), карбид
- 4. Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения
- 5. Cu2O, CuO, SO3, Fe2O3. Определите основные признаки оксидов
- 6. I. Оксиды Оксиды – это сложные вещества, состоящие из атомов двух химических элементов, один из которых
- 7. Номенклатура оксидов: называют их просто – «оксид» «элемента» и указывают степень окисления, если она переменна. Например:
- 8. Классификация оксидов: - оксиды металлов - Na2O, СuO, Al2O3 - оксиды неметаллов - NO2, SO2, Cl2O7
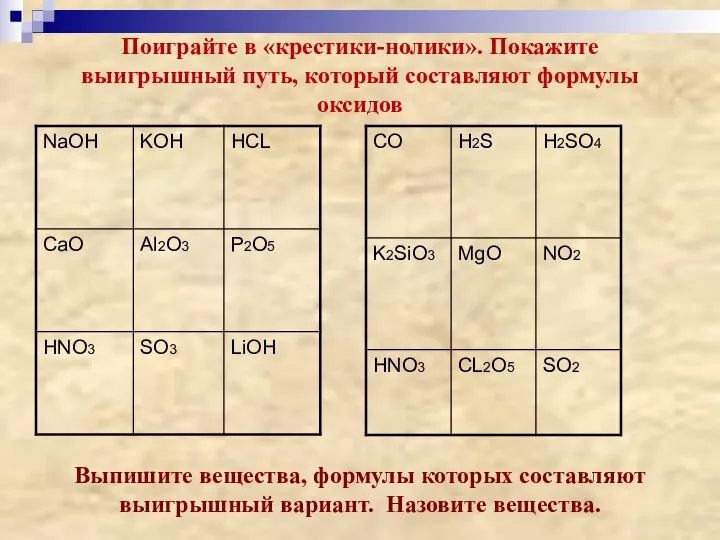
- 9. Поиграйте в «крестики-нолики». Покажите выигрышный путь, который составляют формулы оксидов Выпишите вещества, формулы которых составляют выигрышный
- 10. Выберите формулы оксидов, дайте им названия OF2N2O3MgSiO2CS2NаBr2 Fe2O3K2SK2OCaCl2CO2 OF2N2O3MgSiO2CS2NаBr2 Fe2O3K2SK2OCaCl2CO2 N2O3 – оксид азота (III) SiO2
- 11. Составьте формулы названных в тексте оксидов В земной коре – литосфере – находятся оксид алюминия …
- 12. Ответ: AL2O3, SiO2, Fe2O3, H2O, CO2, CO, SO2, NO2
- 13. Важнейшие представители оксидов
- 14. Самым распространенным оксидом на нашей планете является вода H2O Важнейшие представители оксидов
- 15. Вода (Н2О) самое распространенное вещество на нашей планете, она покрывает 71% площади поверхности Земли, льдом покрыто
- 16. Углекислый газ (CO2) CO2 – содержится в составе вулканических газов, участвует в процессе фотосинтеза, используется при
- 17. Углекислый газ (CO2) содержание углекислого газа в атмосфере 0,04-0,03%, растения, благодаря фотосинтезу, усваивают углекислый газ из
- 18. Углекислый газ (CO2) образуется углекислый газ при дыхании и сгорании топлива, при тлении и гниении органических
- 19. Угарный газ (CO) образуется при неполном сгорании топлива, в выхлопных газах. очень опасен для здоровья, загрязняет
- 20. Негашёная известь (CаO) белое тугоплавкое вещество, энергично взаимодействует с водой, образуя гашёную известь, применяемую в строительстве,
- 21. СаО
- 22. Оксид кремния (SiO2) оксиды кремния и алюминия составляют основную массу земной коры – литосферы, образуя многочисленные
- 23. SiO2 Агат Сапфир Al2O3 Рубин Яшма Опал Халцедон
- 24. Оксид алюминия (Al2O3) используется в ювелирном деле, в металлургии, как огнеупорный материал, катализатор Боксит (глина), рубин,
- 25. Оксид хрома (III) (Cr2O3) кристаллическое вещество зеленого цвета, нерастворимое в воде, используют как пигмент при изготовлении
- 26. II. Водородные соединения элементов NaH, HCl, MgH2, H2S, H3N, KH, HF, HBr, CaH2 Водородные соединения металлов
- 27. 1. Водородные соединения металлов – гидриды: - твёрдые, - нелетучие, - тугоплавкие вещества, в кото- рых
- 28. 2. Водородные соединения неметаллов – летучие водородные соединения: - летучие, - как правило газообразные, - хорошо
- 29. Хлороводород (НCl) бесцветный газ, тяжелее воздуха, хорошо растворим в воде, в 1 объёме воды может раствориться
- 30. Применение хлороводородной (соляной) кислоты
- 31. Аммиак (NН3) бесцветный газ, своеобразный резкий запах, почти в 2 раза легче воздуха, хорошо растворим в
- 33. Скачать презентацию




























 Количество вещества
Количество вещества Драгоценные камни
Драгоценные камни Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Классификация химических элементтов
Классификация химических элементтов Кристаллы и правильные многогранники. 11 класс
Кристаллы и правильные многогранники. 11 класс Кислород. Сера
Кислород. Сера Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна
Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна  Генетика клеточного цикла. Надклеточный контроль клеточного деления, роста и апоптоза. (Глава 5)
Генетика клеточного цикла. Надклеточный контроль клеточного деления, роста и апоптоза. (Глава 5) Амоніак
Амоніак  Atmospheric chemistry
Atmospheric chemistry Презентация по Химии "Презентация Металлы в организме человека" - скачать смотреть
Презентация по Химии "Презентация Металлы в организме человека" - скачать смотреть  ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар
ЩЕЛОЧНЫЕ МЕТАЛЛЫ Выполнили: Патренкина Наталия, Иванова Кристина, ученицы 9«А» класса СОШ №6 Руководитель: Овсяникова Мар Дисциплина: Химия. Лекция 1. Растворы
Дисциплина: Химия. Лекция 1. Растворы Общие пути обмена аминокислот. (Лекция 11)
Общие пути обмена аминокислот. (Лекция 11) Коллоидные растворы
Коллоидные растворы Введение. Предмет и содержание фармацевтической химии, её связи с другими науками
Введение. Предмет и содержание фармацевтической химии, её связи с другими науками Ионная химическая связь
Ионная химическая связь Углеводы: моносахариды, олиго- и полисахариды
Углеводы: моносахариды, олиго- и полисахариды Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2)
Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2) Металлы: общая характеристика
Металлы: общая характеристика Итоговая консультация. Формульный диктант
Итоговая консультация. Формульный диктант Металлы и их активность
Металлы и их активность Химиялық элемент алюминий
Химиялық элемент алюминий Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Ориентационная вытяжка полимеров
Ориентационная вытяжка полимеров Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В.
Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В. Углеводы. Моносахариды, олигосахариды (дисахариды)
Углеводы. Моносахариды, олигосахариды (дисахариды) Сера. Строение атома, аллотропия, свойства и применение серы
Сера. Строение атома, аллотропия, свойства и применение серы