Содержание
- 2. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ Растворы всех веществ можно разделить на две группы: проводят электрический ток или проводниками
- 3. Для объяснения особенностей водных растворов электролитов шведским ученым С. Аррениусом в 1887 г. была предложена теория
- 4. 1. Электролиты при растворении в воде или расплавлении распадаются (диссоциируют)на ионы – положительно (катионы) и отрицательно
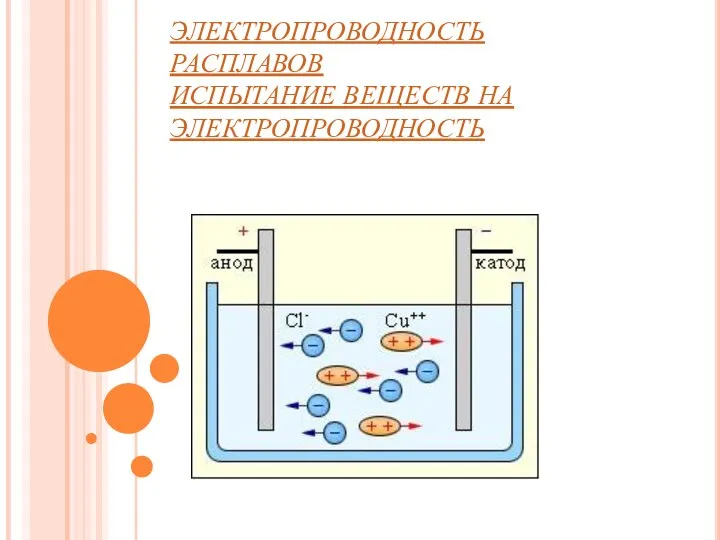
- 5. ЭЛЕКТРОПРОВОДНОСТЬ РАСПЛАВОВ ИСПЫТАНИЕ ВЕЩЕСТВ НА ЭЛЕКТРОПРОВОДНОСТЬ
- 6. К сильным электролитам относятся 1) кислоты (H2SO4, HCl, HNO3, HBr, HI, HClO4, HМnO4); 2) основания –
- 7. К слабым электролитам относятся: 1) неорганические кислоты (H2CO3, H2S, HNO2, H2SO3 , HCN, H3PO4, H2SiO3, HCNS,
- 8. Уравнения диссоциации Уравнение, отражающее обратимый процесс (↔) диссоциации данного вещества, называется уравнением диссоциации. В растворе или
- 9. Диссоциация кислот Кислотами называют электролиты, которые при диссоциации образуют катионы только Н+, например: HNO3 ⬄ H+
- 10. Диссоциация оснований Основаниями называют электролиты, которые при диссоциации образуют анионы только OH─ : NaOH ⬄ Na+
- 11. Диссоциация солей Солями называют электролиты, которые при диссоциации образуют катионы металла (или аммония NH4+) и анионы
- 12. Тест по теме "Электролитическая диссоциация. Реакции ионного обмена" 1. К неэлектролитам относится: 1) нитрат калия 2)
- 14. Скачать презентацию










 Исследование соединений со структурой слоистого перовскита
Исследование соединений со структурой слоистого перовскита Коллоидное состояние вещества
Коллоидное состояние вещества Непредельные углеводороды (обобщающий урок)
Непредельные углеводороды (обобщающий урок) Специфические пути обмена отдельных аминокислот. Патология. (Лекция 12)
Специфические пути обмена отдельных аминокислот. Патология. (Лекция 12) Основные понятия и законы химии. Эквивалент. Закон эквивалентов. Закон титрования
Основные понятия и законы химии. Эквивалент. Закон эквивалентов. Закон титрования Углерод. Аллотропные состояния углерода
Углерод. Аллотропные состояния углерода Оксиды и гидроксиды металлов
Оксиды и гидроксиды металлов Электронное строение атома
Электронное строение атома Характеристики раствора Вкус Цвет Что растворено (раствор сахара, соли, спирта, уксусной кислоты и т.д.) Что является растворител
Характеристики раствора Вкус Цвет Что растворено (раствор сахара, соли, спирта, уксусной кислоты и т.д.) Что является растворител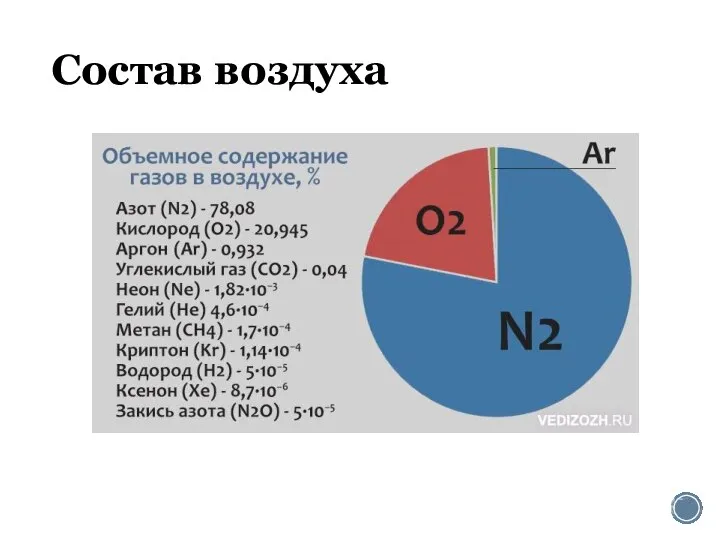 Состав воздуха. Азот
Состав воздуха. Азот Презентация по Химии "Сера" - скачать смотреть
Презентация по Химии "Сера" - скачать смотреть  Полимеризация бутилена и пропилена
Полимеризация бутилена и пропилена Роль химии в жизни человека
Роль химии в жизни человека Химическая коррозия
Химическая коррозия Колебания кристаллической решетки и ее тепловые свойства. Динамика решетки
Колебания кристаллической решетки и ее тепловые свойства. Динамика решетки Теория валентных связей
Теория валентных связей Медь. Содержание в природе
Медь. Содержание в природе Кислород, получение, свойства
Кислород, получение, свойства Массовая доля компонентов
Массовая доля компонентов Амины
Амины АЛЮМІНІЄВІ СПЛАВИ Підготувала учениця 10 класу Кисленко Єлизавета
АЛЮМІНІЄВІ СПЛАВИ Підготувала учениця 10 класу Кисленко Єлизавета  Задача №7. По щам! Команда «Карбораны»
Задача №7. По щам! Команда «Карбораны» Процессы нитрования
Процессы нитрования Магний. Электронное строение атома Mg
Магний. Электронное строение атома Mg Ультраосновные породы щелочные и умереннощелочные
Ультраосновные породы щелочные и умереннощелочные Механизмы образования ковалентной связи
Механизмы образования ковалентной связи При растворении в воде гидроксид-ионы образует вещество, формула которого При растворении в воде гидроксид-ионы образует веществ
При растворении в воде гидроксид-ионы образует вещество, формула которого При растворении в воде гидроксид-ионы образует веществ Взаимное притяжение и отталкивание молекул. Тема 11
Взаимное притяжение и отталкивание молекул. Тема 11