Содержание
- 2. C6H12O6 + 6O2 = 6CO2 + 6H2O + 673 ккал/моль CuSO4 + H2O + 2* 96500
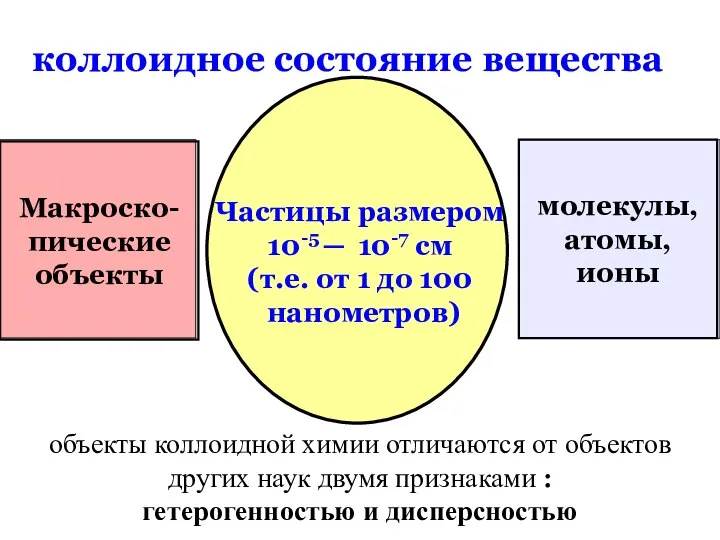
- 3. коллоидное состояние вещества Макроско- пические объекты молекулы, атомы, ионы Частицы размером 10-5 ─ 10-7 см (т.е.
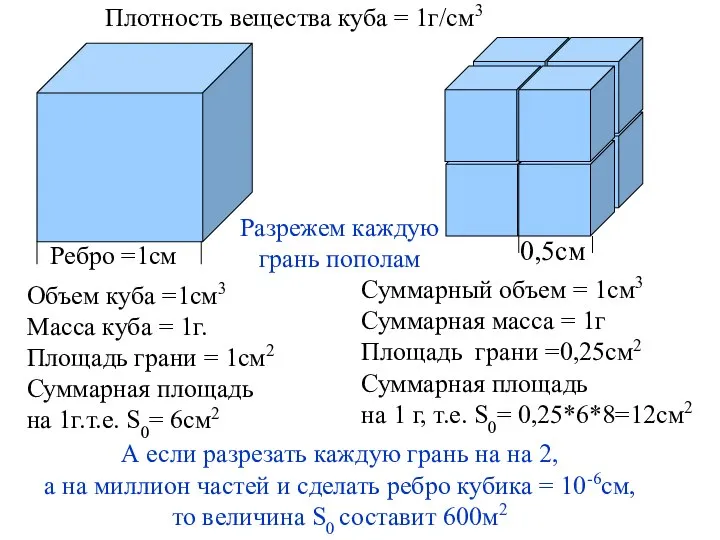
- 4. Плотность вещества куба = 1г/см3 Ребро =1см Объем куба =1см3 Масса куба = 1г. Площадь грани
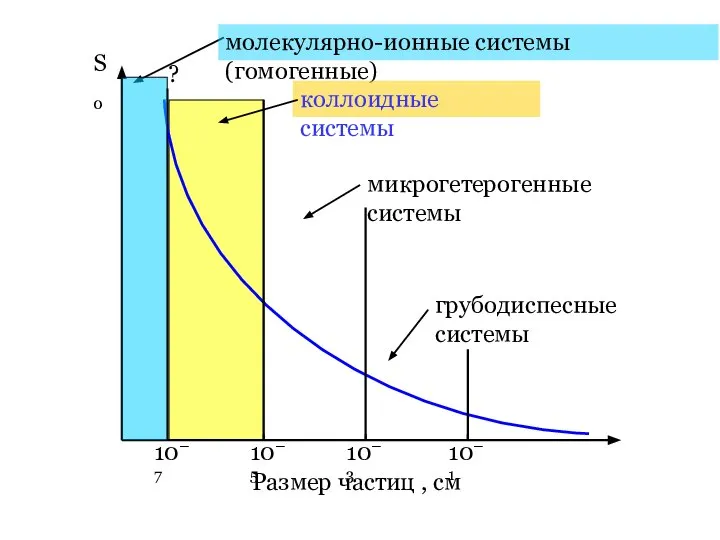
- 5. S0 Размер частиц , см 10–7 10–3 10–5 10–1 молекулярно-ионные системы (гомогенные) коллоидные системы микрогетерогенные системы
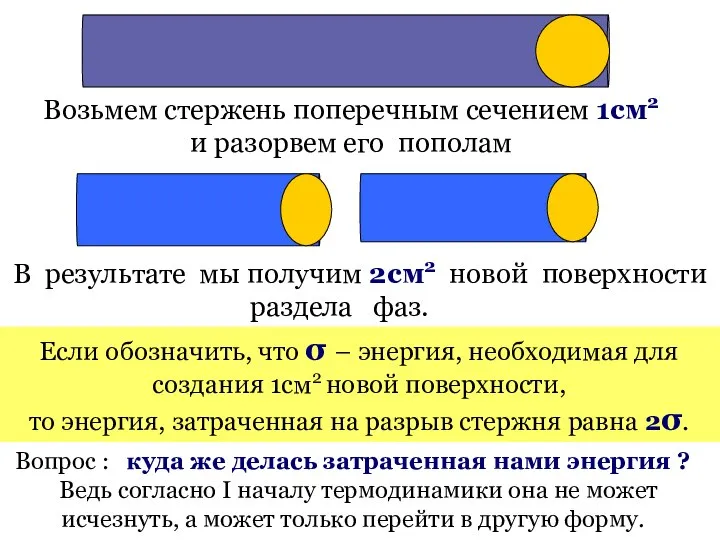
- 7. Возьмем стержень поперечным сечением 1см2 и разорвем его пополам В результате мы получим 2см2 новой поверхности
- 8. (В.I) dG = - S*dT +V*dP + σ*ds + μi*dni + φ*dq тепловая поверхностная химическая механическая
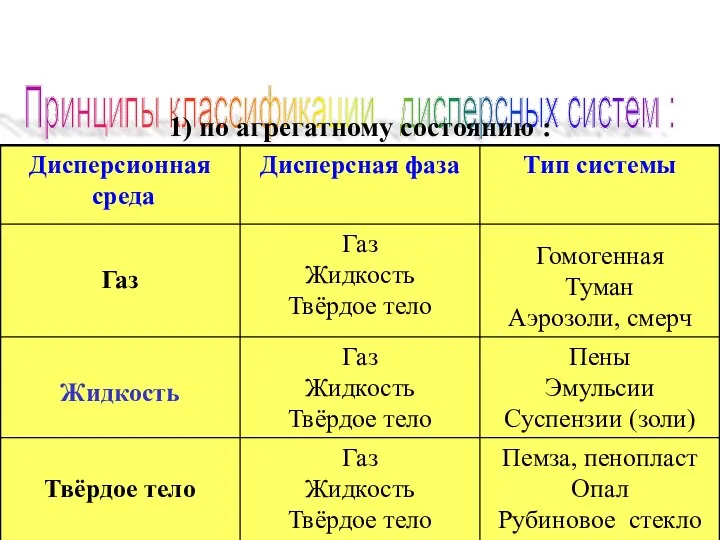
- 9. Принципы классификации дисперсных систем : 1) по агрегатному состоянию :
- 10. Туман
- 11. Смерч
- 13. Цветные стекла
- 14. 2) по структуре : а) свободно ─ дисперсные ; b) связно ─ дисперсные 3) по степени
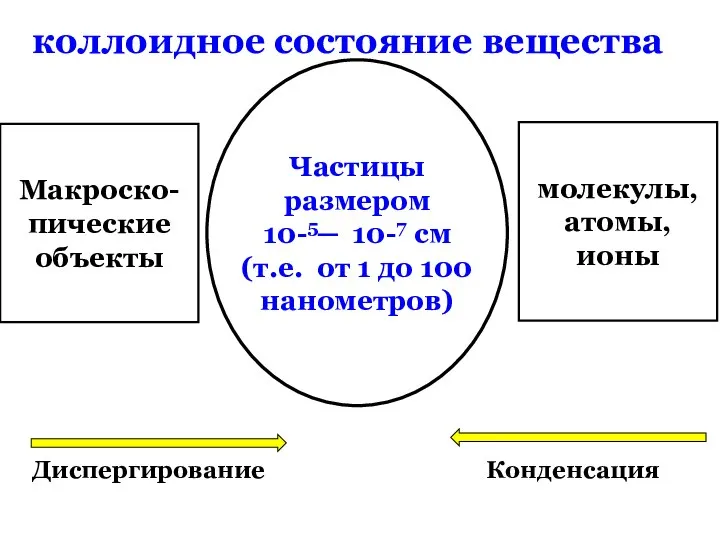
- 15. коллоидное состояние вещества Макроско- пические объекты молекулы, атомы, ионы Диспергирование Конденсация Частицы размером 10-5─ 10-7 см
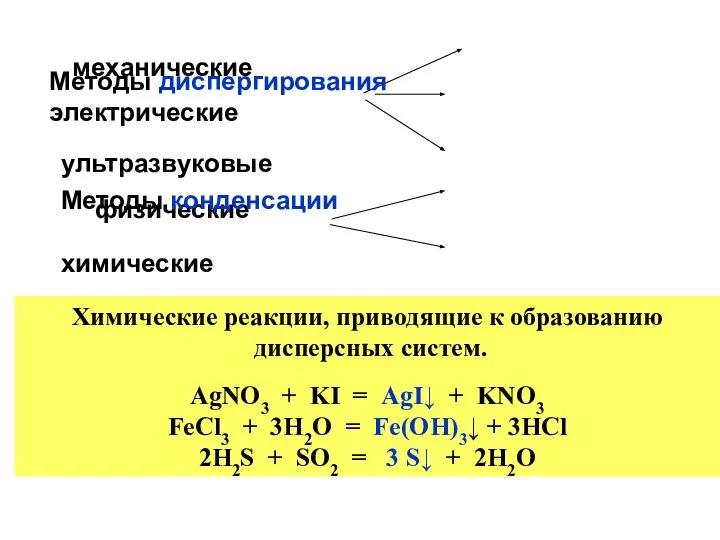
- 16. механические Методы диспергирования электрические ультразвуковые физические Методы конденсации химические Химические реакции, приводящие к образованию дисперсных систем.
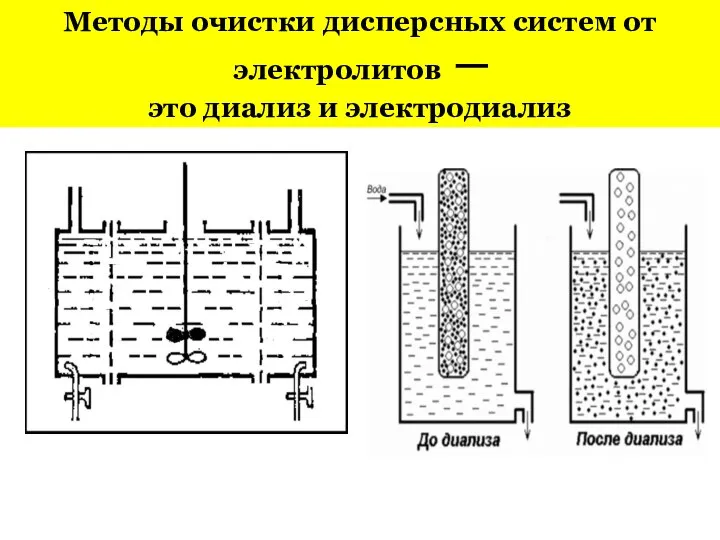
- 17. Методы очистки дисперсных систем от электролитов ─ это диализ и электродиализ
- 18. Некоторые физические свойства разбавленных растворов зависят не от их химического состава , а от числа кинетических
- 19. С открытием коллоидного состояния вещества возник вопрос ― характерны ли эти свойства для частиц , занимающих
- 20. Решающий сдвиг во взглядах на этот вопрос произошел после открытия в 1827 г английским ботаником Р.Броуном
- 22. Теоретические расчеты Эйнштейна и Смолуховского , связавшие величину среднего квадратичного сдвига частицы ∆х2 с коэффициентом диффузии
- 23. Диффузией называется процес самопроизвольного выравнивания концентраций в системе , приводящий к установлению одинаковых значений химического потенциала
- 24. Явление диффузии необратимо и она протекает до полного выравнивания концентраций , т.к хаотическому распределению частиц соответствует
- 25. Эйнштейн вывел уравнение ( III.3 ) : D = RT/ 6πηrNA , из которого следует ,
- 26. Считая , что макромолекула имеет сферическую форму и зная плотность вещества ρ , можно сначала ,
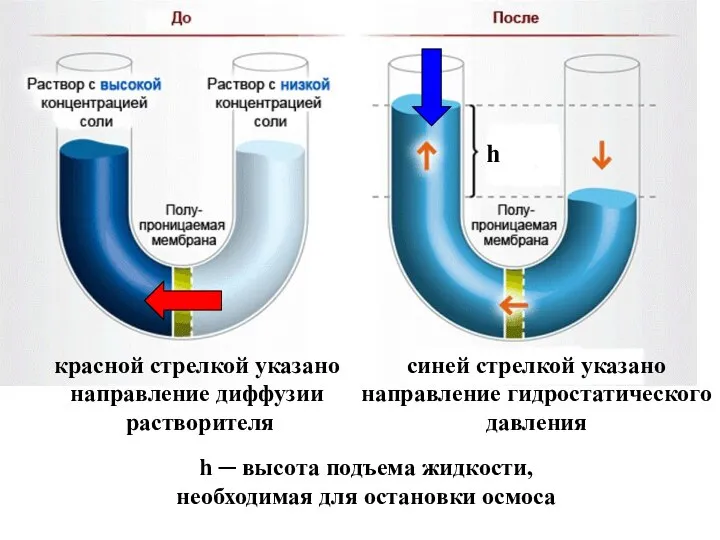
- 27. Осмосом называется явление массопереноса растворителя через полупроницаемую мембрану из разбавленного раствора в раствор более высокой концентрации.
- 28. красной стрелкой указано направление диффузии растворителя h синей стрелкой указано направление гидростатического давления h ─ высота
- 29. Процесс перехода растворителя в раствор самопроизволен, но обратный процесс самопроизвольно осуществляться не может, поэтому для разделения
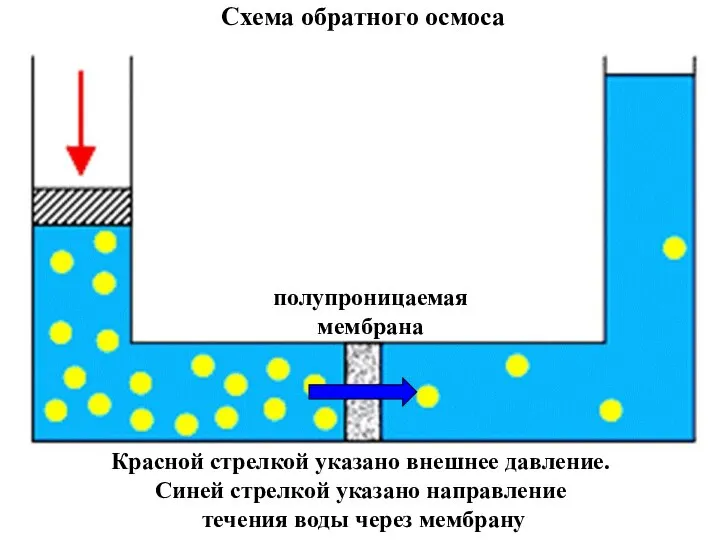
- 30. полупроницаемая мембрана Схема обратного осмоса Красной стрелкой указано внешнее давление. Синей стрелкой указано направление течения воды
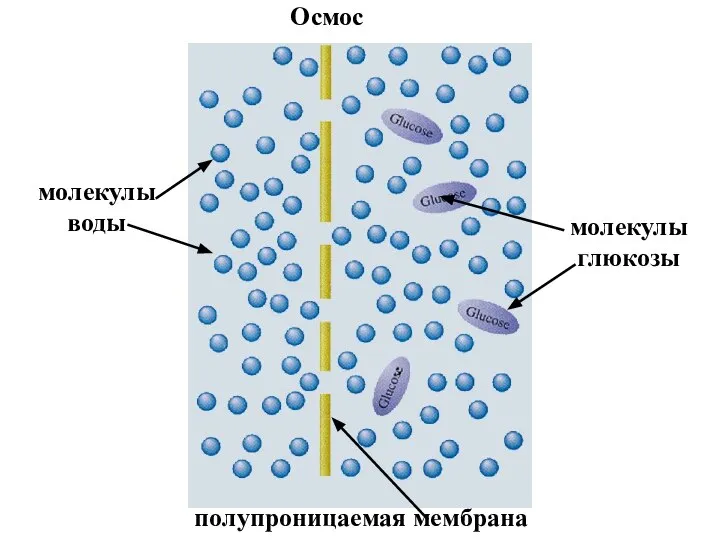
- 31. молекулы воды молекулы глюкозы полупроницаемая мембрана Осмос
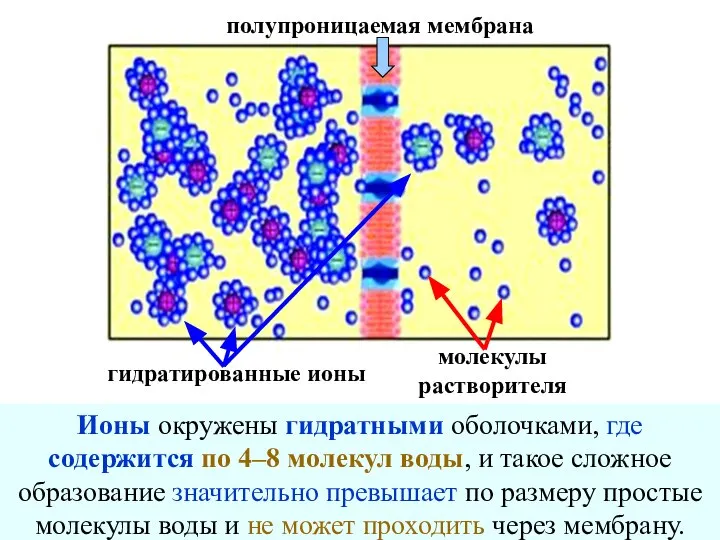
- 32. Понятно, что через полупроницаемую мембрану не могут проходить частицы коллоидного размера и большие молекулы, например, молекулы
- 33. гидратированные ионы молекулы растворителя полупроницаемая мембрана Ионы окружены гидратными оболочками, где содержится по 4–8 молекул воды,
- 34. Осмос и осмотическое давление имеют огромное значение в биологических явлениях, т. к. оболочки клеток биологических тканей
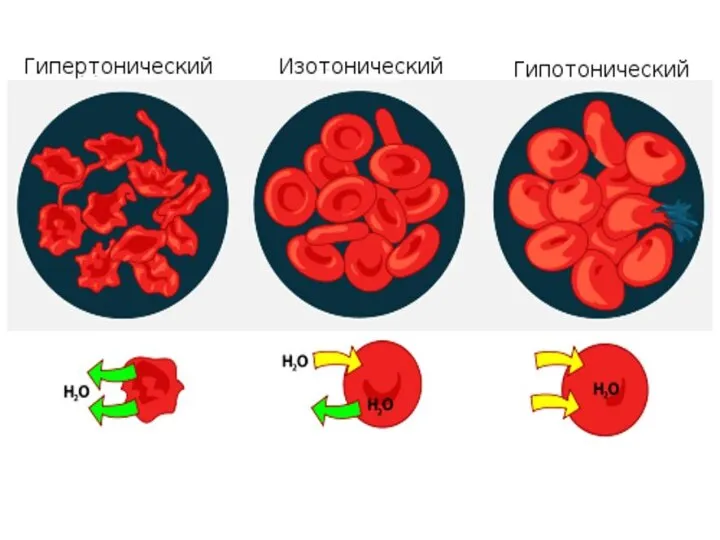
- 35. Плазма крови , в которой взвешены эритроциты , является изотонической с жидкостью , находящейся внутри эритроцитов
- 36. В гипертоническом растворе, осмотическое давление которого выше осмотического давления крови, эритроциты сморщиваются, так как вода выходит
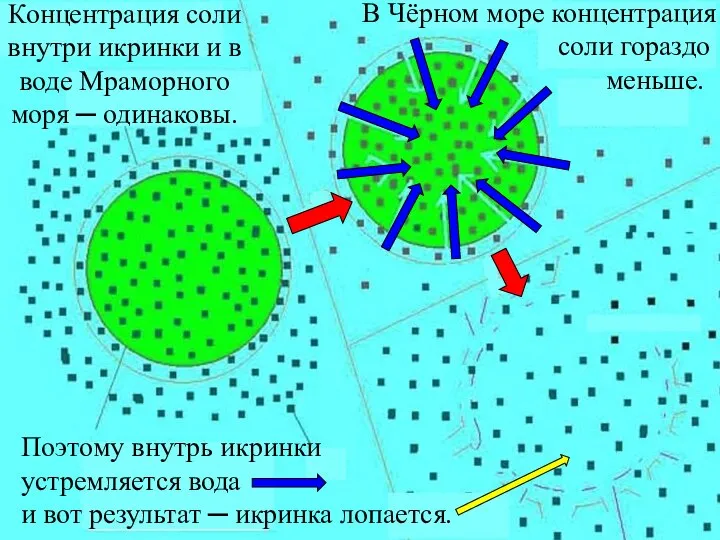
- 38. А гибнут икринки морских животных в Черном море из-за осмоса : концентрация соли в икринке –
- 39. Концентрация соли внутри икринки и в воде Мраморного моря ─ одинаковы. В Чёрном море концентрация соли
- 40. Для разбавленных растворов известно уравнение Вант-Гоффа : (III.6) Π = сRT , где : Π –
- 41. Такие же растворы электролитов (NaCl или KNO3) имеют осмотическое давление в два раза больше. Аналогичные растворы
- 42. Изотонический коэффициент показывает, насколько в растворе электролита больше кинетических единиц (т.е. ионов) по сравнению с раствором
- 43. Для ответа на этот вопрос прежде всего необходимо определиться с понятием концентрации дисперсной системы . Поскольку
- 44. Как видно из данного примера , частичная концентрация Сd оказывается на семь порядков (!) меньше ,
- 45. Зато в растворах ВМС, где размеры макромолекул меньше, чем у частиц золота, величины осмотического давления оказались
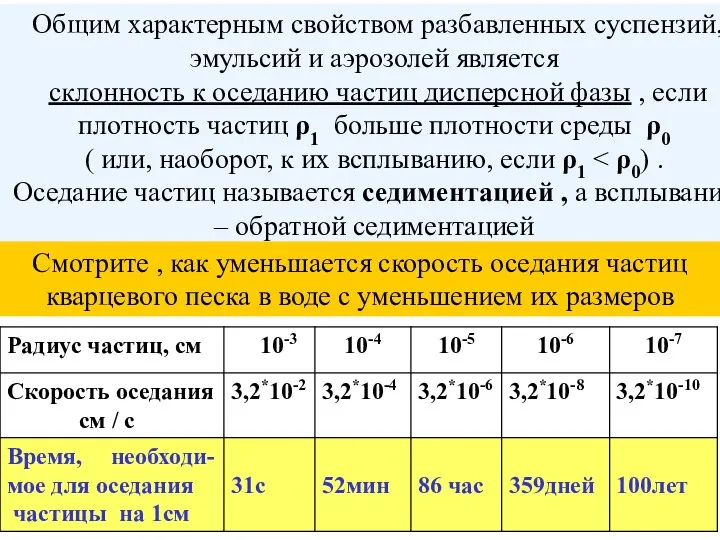
- 46. Общим характерным свойством разбавленных суспензий, эмульсий и аэрозолей является склонность к оседанию частиц дисперсной фазы ,
- 47. Столь интересные данные объясняются тем , что для частиц коллоидного размера гравитационное поле , стремящееся создать
- 48. Чтобы применить эту же формулу к коллоидной системе (золю) , заменим отношение Р0 / Р1 на
- 49. Уравнение Перрена имеет еще и большое историческое значение , т.к. с его помощью было впервые экспериментально
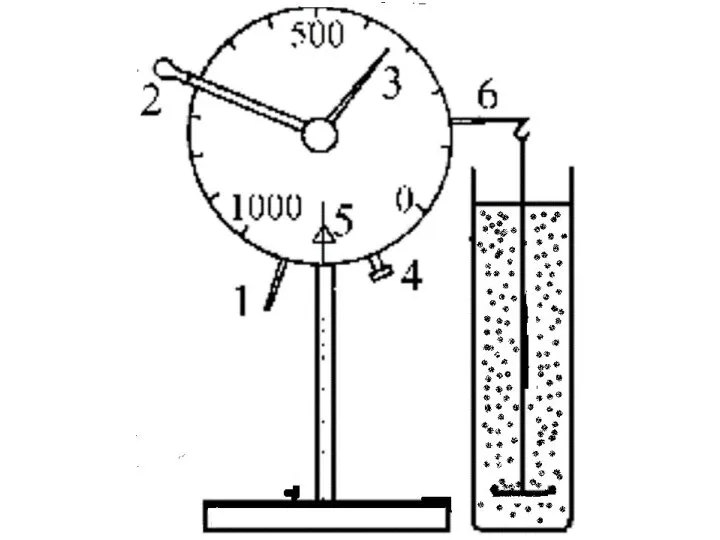
- 50. с установлением стационарного режима оседания , т.е. равномерного , прямолинейного движения частицы в жидкости , для
- 51. Эта формула используется в дисперсионном анализе, который позволяет определить размеры частиц в дисперсной системе и процентное
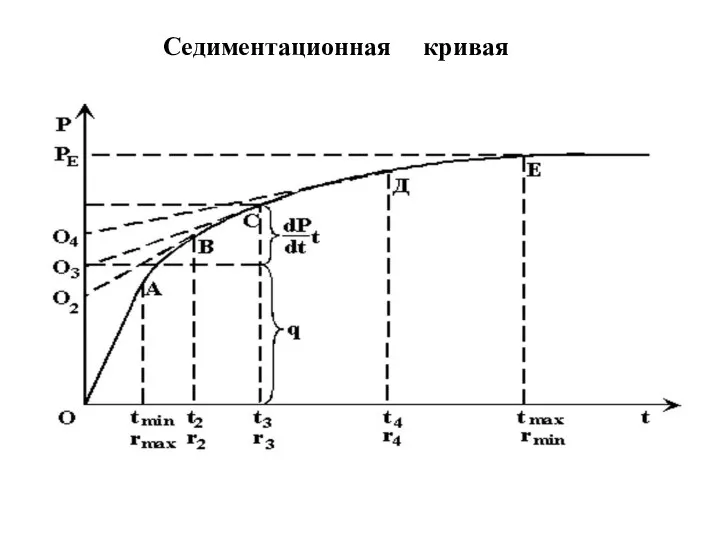
- 54. Cедиментационная кривая
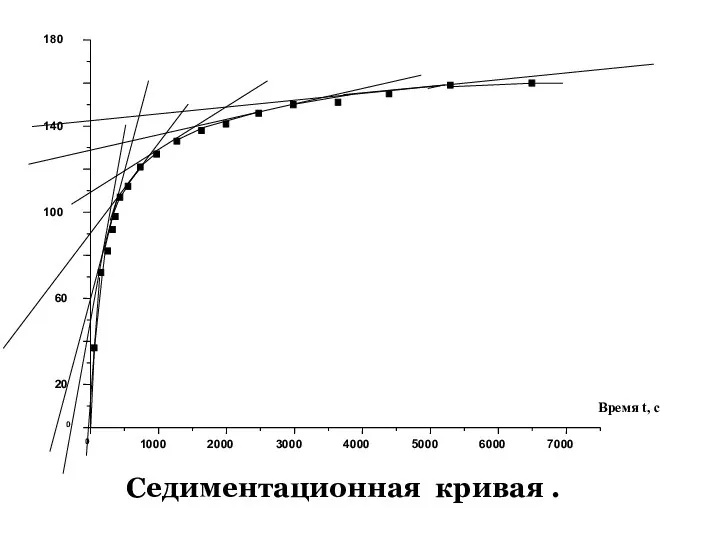
- 55. Седиментационная кривая .
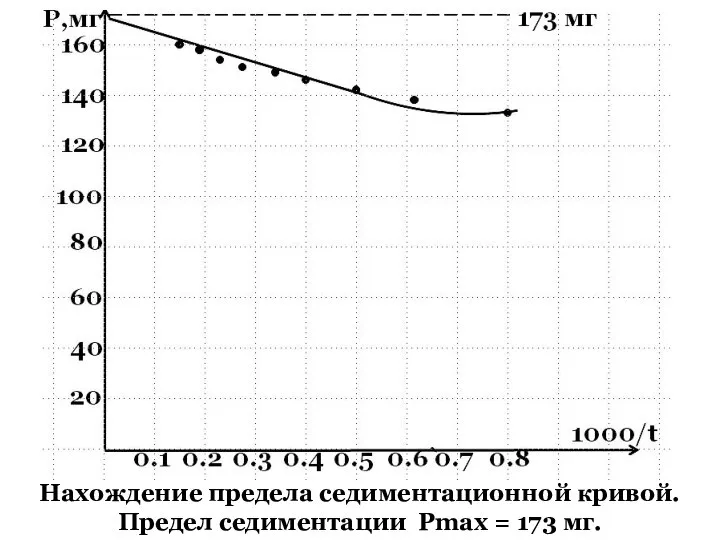
- 56. Нахождение предела седиментационной кривой. Предел седиментации Pmax = 173 мг.
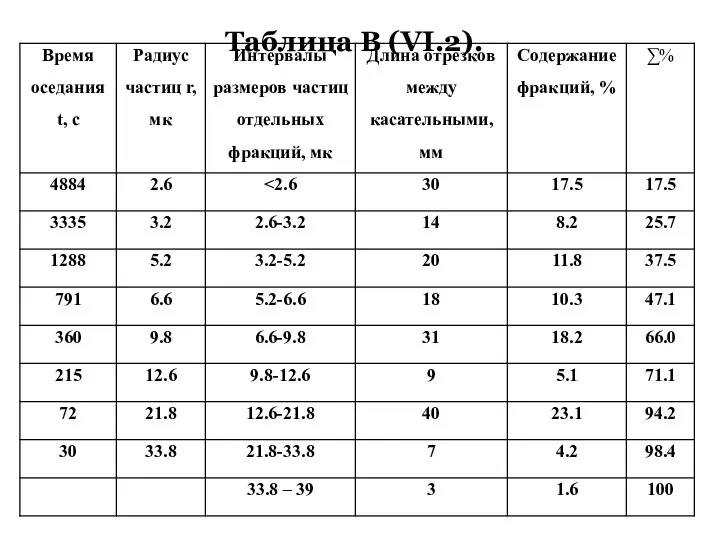
- 57. Определив предел седиментации PE , проводят несколько касательных к седиментационной кривой в точках, соответствующих различному времени
- 58. Таблица В (VI.2).
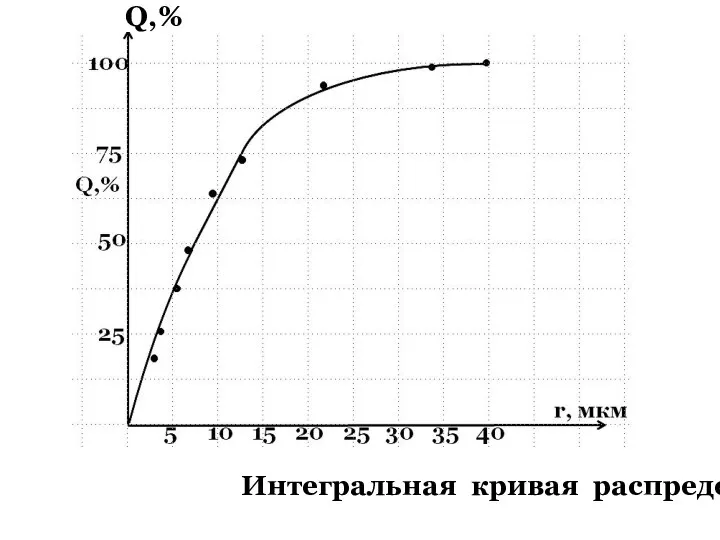
- 59. Интегральная кривая распределения . Q,%
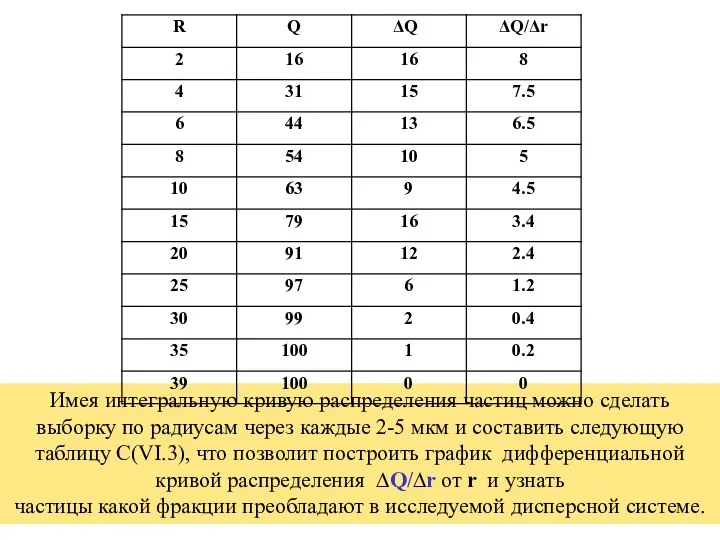
- 60. Имея интегральную кривую распределения частиц можно сделать выборку по радиусам через каждые 2-5 мкм и составить
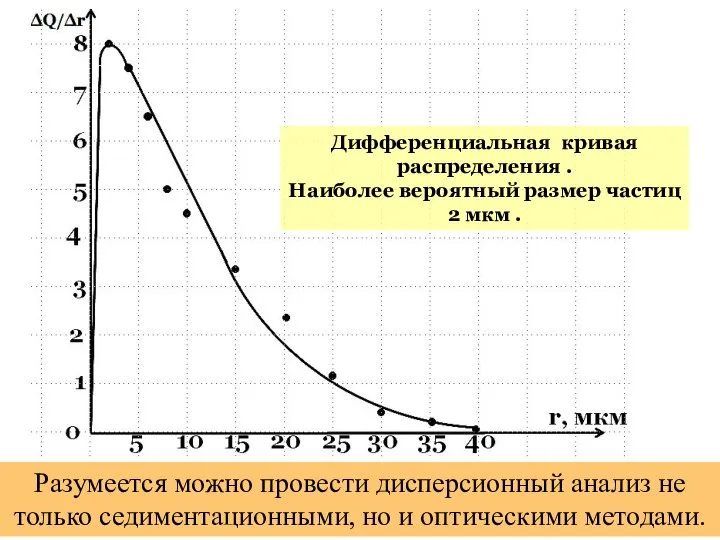
- 61. Дифференциальная кривая распределения . Наиболее вероятный размер частиц 2 мкм . Разумеется можно провести дисперсионный анализ
- 62. Оптические свойства дисперсных систем Подавляющее большинство окружающих нас природных дисперсных систем являются коллоидными : земная атмосфера,
- 63. 1) прохождение света через систему – характерно для молекулярно-ионных гомогенных систем ; 2) преломление и отражение
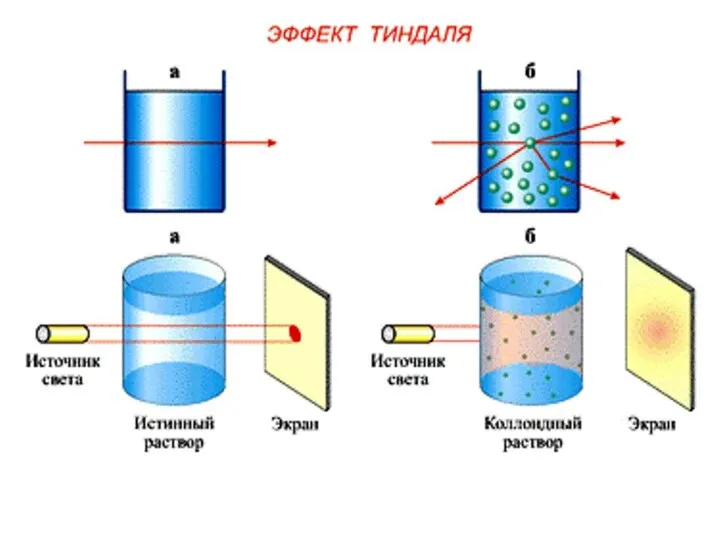
- 64. Это явление называется опалесценцией и обусловлено оно рассеянием света вследствие дифракции его в микронеоднородной дисперсной системе
- 68. Запишем уравнение ( III.12 ) в более простой форме , (убрав все , что можно в
- 69. Если бесцветную коллоидную систему облучать белым светом , то сбоку мы увидим голубую окраску , а
- 73. 4) Опалесценция зависит от разности показателей преломления дисперсной фазы и среды , поэтому если выбрать систему
- 74. Абсорбция ( поглощение ) света . При прохождении света через раствор интенсивность на выходе может стать
- 75. Подставив (III.15) в (III.14) , получим выражение для закона Бугера- Ламберта – Бэра : (III.16 )
- 76. Молярный коэффициент поглощения ε является величиной постоянной , характерной для данного вещества, зависящей от длины волны
- 77. В этом случае формула (III.16) превращается в (III.18) Iпр = I0 e ─ (ε + k)
- 78. Оптические свойства дисперсных систем в первую очередь используются для дисперсионного анализа , т.е определения размеров и
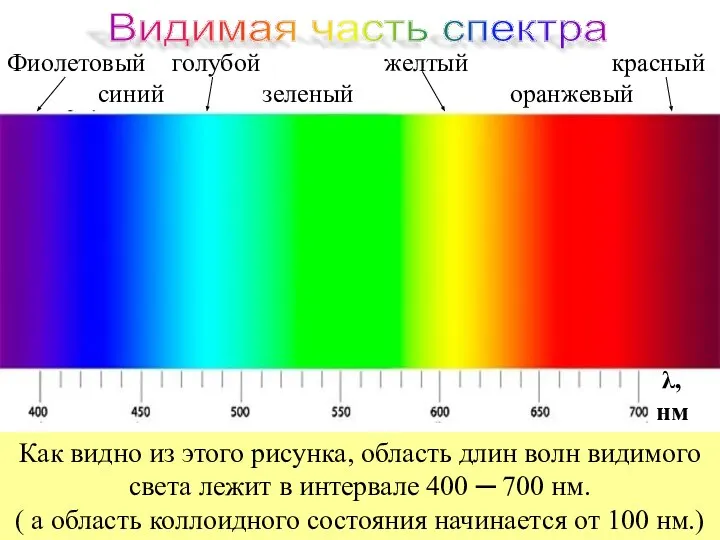
- 79. Фиолетовый голубой желтый красный синий зеленый оранжевый λ, нм Как видно из этого рисунка, область длин
- 80. Обычный оптический микроскоп
- 81. Разрешающая способность обычного микроскопа λ (III.20) d = -------------- где : 2 n sin (α/2) λ
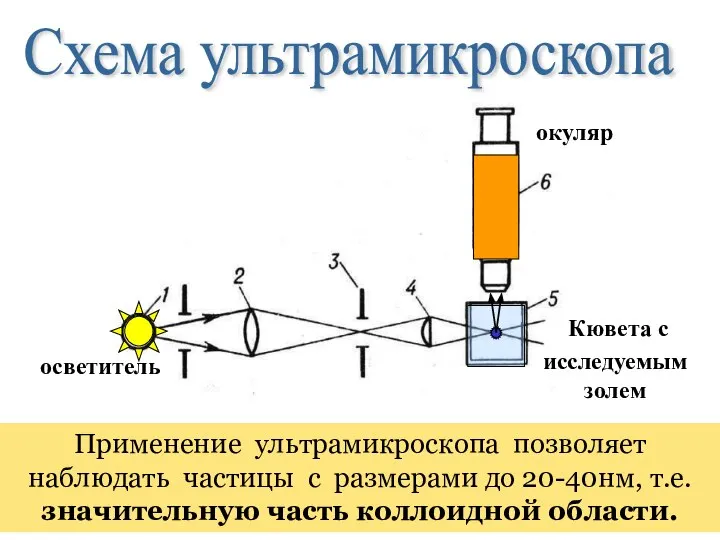
- 82. В 1903 г. Р. Зигмонди и Р. Зидентопфом был изобретен оптический ультрамикроскоп, в котором дисперсная система
- 83. Кювета с исследуемым золем осветитель окуляр Применение ультрамикроскопа позволяет наблюдать частицы с размерами до 20-40нм, т.е.
- 84. Ещё более высокой разрешающей способностью обладают современные электронные микроскопы (рис.VI.3), в которых световой пучок заменяется потоком
- 85. Правда, у электронной микроскопии есть свои недостатки: в них нельзя наблюдать гидрозоли и аэрозоли, а также
- 86. А вот и снимок, сделанный электронным микроскопом: Как ни странно, но это …. обычная…. блоха. Кто
- 87. "Какими будут свойства материалов, если мы действительно сможем располагать атомы так, как нам нужно?“ задал свой
- 88. Но и оптический и электронный микроскоп дают лишь плоскую картинку. Увидеть трёхмерную структуру микромира удалось только
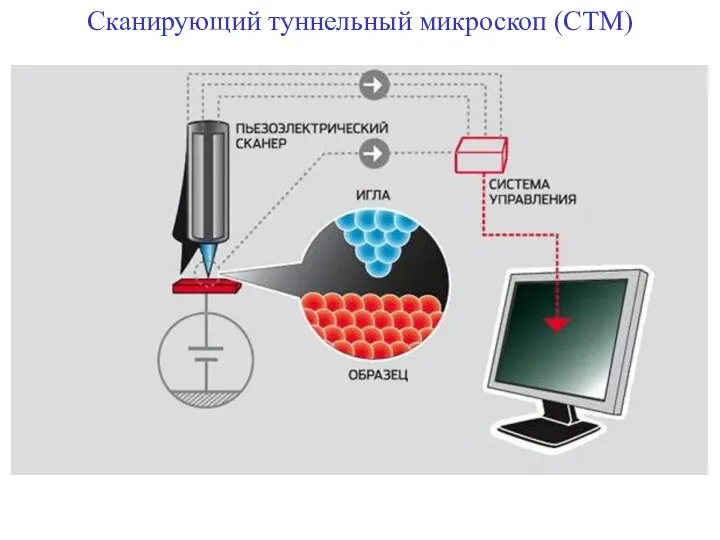
- 89. Сканирующий туннельный микроскоп (СТМ)
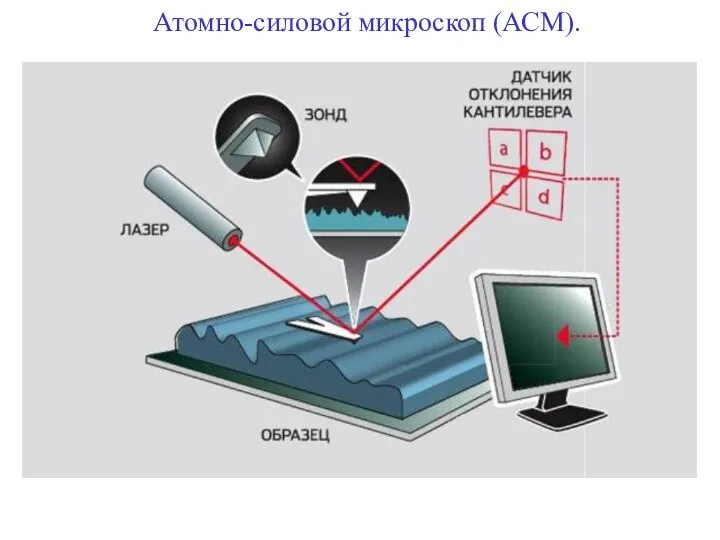
- 90. Атомно-силовой микроскоп (АСМ).
- 91. На конце кантилевера расположен микрозонд ─ острый шип (радиус закругления от 1 до 10 нм). При
- 93. Разрешающая способность метода составляет примерно 0,1–1 нм по горизонтали и 0,01 нм по вертикали. Так ученые
- 95. Скачать презентацию





























































 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Методы комплексонометрии. Количественный анализ
Методы комплексонометрии. Количественный анализ Природа активності та кислотності цеолітних каталізаторів
Природа активності та кислотності цеолітних каталізаторів Хромопротеиды: биологическая роль. Синтез и распад гема. Метаболизм билирубина
Хромопротеиды: биологическая роль. Синтез и распад гема. Метаболизм билирубина Автомобильные бензины и дизельное топливо
Автомобильные бензины и дизельное топливо Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Альдегиды и кетоны
Альдегиды и кетоны Щёлочноземельные металлы. Выполнила: Ученица 9 Б класса МОУ СОШ № 172 Мошкова Любовь.
Щёлочноземельные металлы. Выполнила: Ученица 9 Б класса МОУ СОШ № 172 Мошкова Любовь. Презентация по Химии "открытие органической химии" - скачать смотреть
Презентация по Химии "открытие органической химии" - скачать смотреть  Камни и Скорпион
Камни и Скорпион Производная в химии
Производная в химии Синильная Кислота - циановодород
Синильная Кислота - циановодород Тема:Хімія
Тема:Хімія  Дослідження на тему: Повітря Христинівщини За проектом “Екологічна ситуація у рідному місті”
Дослідження на тему: Повітря Христинівщини За проектом “Екологічна ситуація у рідному місті” Сырьё для получения фенолальдегидных полимеров
Сырьё для получения фенолальдегидных полимеров Химия элементов VIIA-группы
Химия элементов VIIA-группы Химический элемент Алюминий
Химический элемент Алюминий «Көмірсулар» Қайталау сабағы
«Көмірсулар» Қайталау сабағы Природні джерела вуглеводнів Підготувала: Савчук Ірина
Природні джерела вуглеводнів Підготувала: Савчук Ірина  Применение неметаллов и их соединений
Применение неметаллов и их соединений Ферменты. Часть I
Ферменты. Часть I Химия в профессии компьютерные сети (КС)
Химия в профессии компьютерные сети (КС)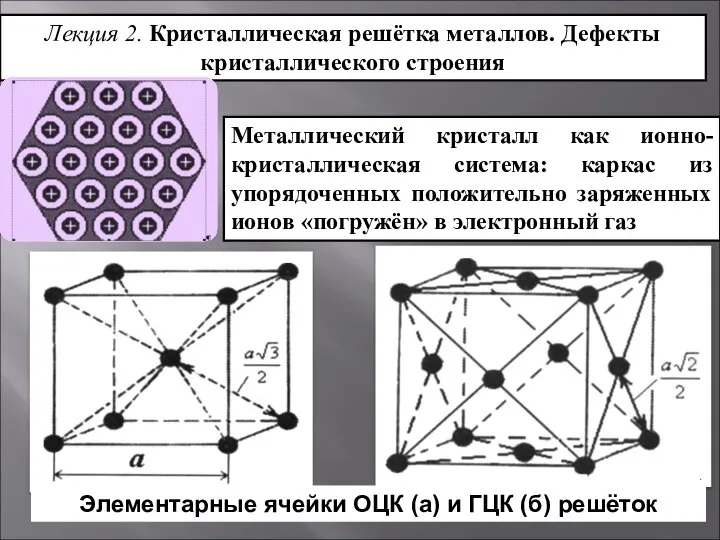 Кристаллическая решётка металлов. Дефекты кристаллического строения. Лекция 2
Кристаллическая решётка металлов. Дефекты кристаллического строения. Лекция 2 Серная кислота. Физические свойства
Серная кислота. Физические свойства АЛЮМИНИЙ Овчинникова Ольга Анатольевна Учитель химии МБОУ Российская гимназия № 59 г.Улан-Удэ
АЛЮМИНИЙ Овчинникова Ольга Анатольевна Учитель химии МБОУ Российская гимназия № 59 г.Улан-Удэ Основы общей химии
Основы общей химии Закономерности взаимодействия организма и химических веществ
Закономерности взаимодействия организма и химических веществ