Содержание
- 2. Электролизом называется окислительно-восстановительное разложение вещества под действием проходящего через него постоянного электрического тока. Процессы, протекающие при
- 3. Электролиза возможен при соблюдении двух условий: 1. Необходима электропроводность вещества, т.е. наличие проводников второго рода (ионов).
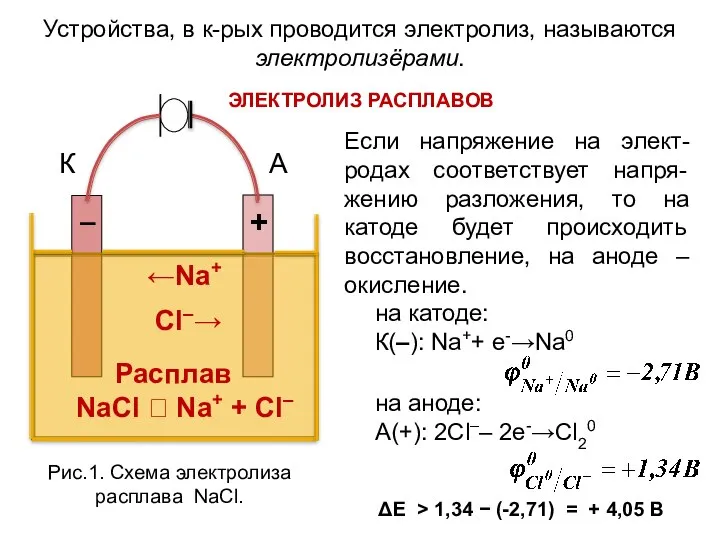
- 4. ←Na+ Cl–→ Расплав NaCl ⮀ Na+ + Cl– Устройства, в к-рых проводится электролиз, называются электролизёрами. ЭЛЕКТРОЛИЗ
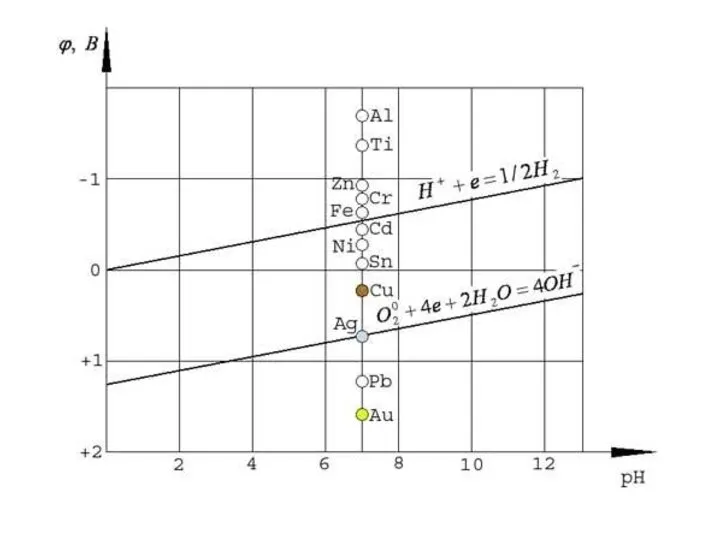
- 5. ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ При электролизе растворов наряду с разложением растворённого вещества возможен и электролиз растворителя. Последовательность
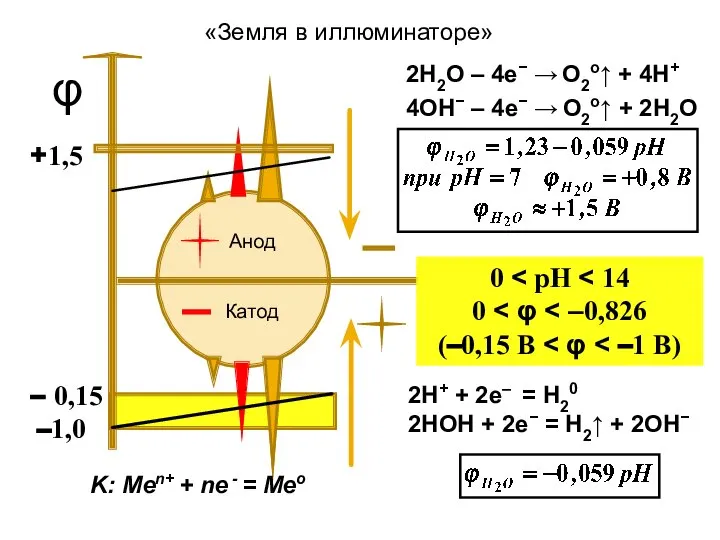
- 7. Анод Катод φ 0 0 (–0,15 B K: Меn+ + nе - = Мео 2Н+ +
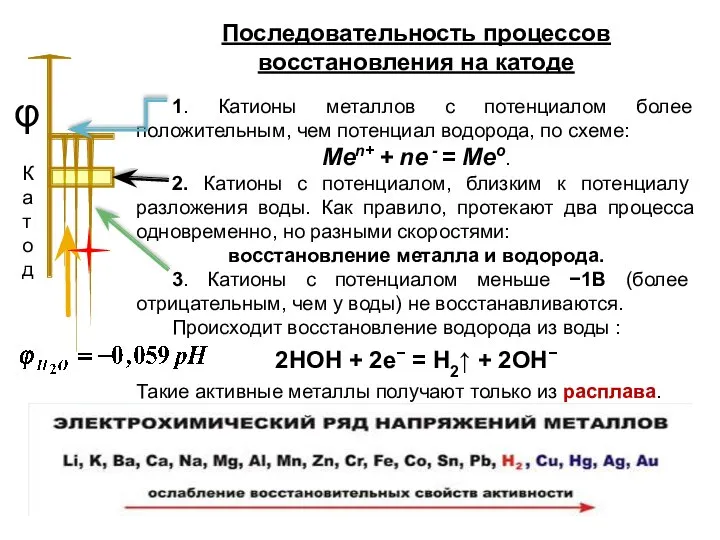
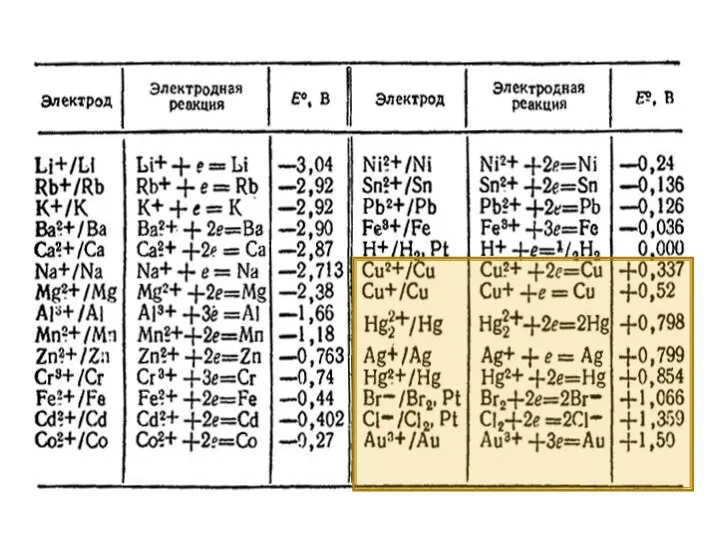
- 9. Последовательность процессов восстановления на катоде 1. Катионы металлов с потенциалом более положительным, чем потенциал водорода, по
- 10. Последовательность процессов окисления на аноде 1. электролиз с растворимым (активным) анодом. Если анод выполнен из активного
- 11. 3. Выделение кислорода при окислении ионов ОН− и воды протекает при отсутствии бескислородных анионов по схеме.
- 12. Законы электролиза (з-ны Фарадея) Количественные закономерности, к-рым подчиняются процессы эл-за, установлены в 1833-1834г.г. М. Фарадеем: Кол-во
- 13. На практике масса покрытия (mпракт) оказывается ниже теоретически рассчитанной. Объясняется это протеканием разл. побочных процессов, например,
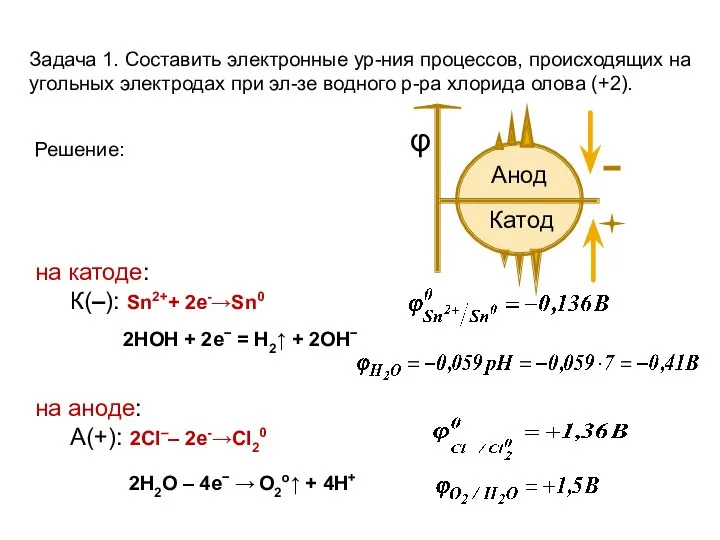
- 14. Задача 1. Составить электронные ур-ния процессов, происходящих на угольных электродах при эл-зе водного р-ра хлорида олова
- 15. Задача 2. Деталь хромируется в водном р-ре сульфата хрома (+3). Определить силу тока, если в течение
- 16. Анод Катод φ
- 25. Скачать презентацию











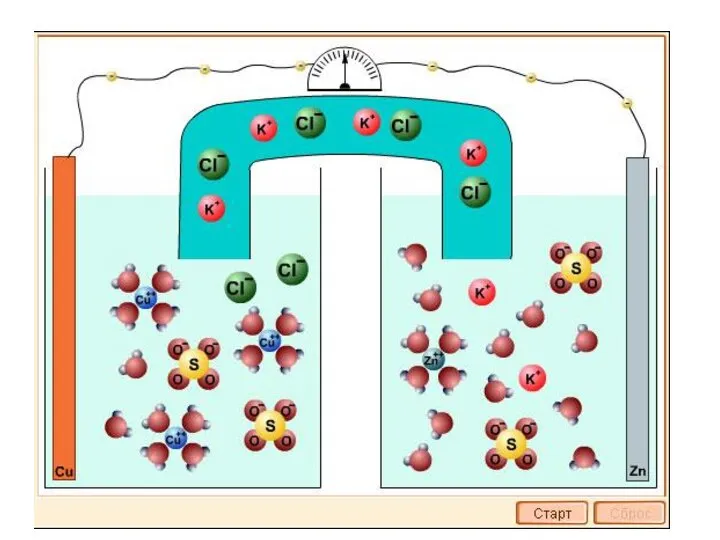
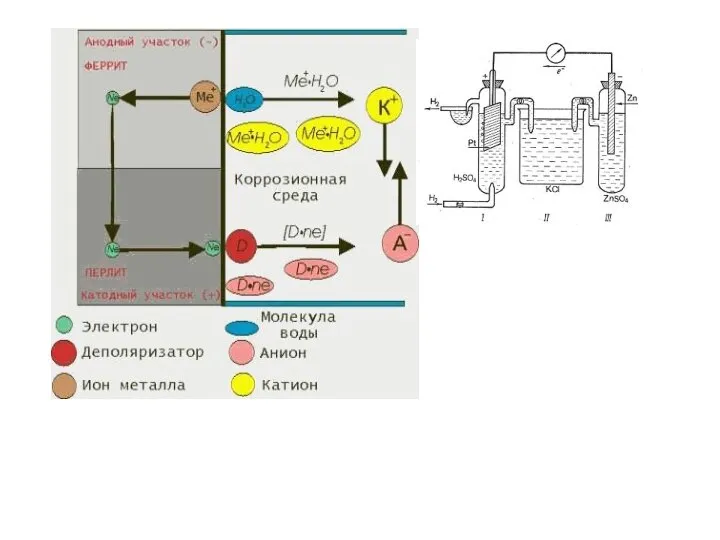
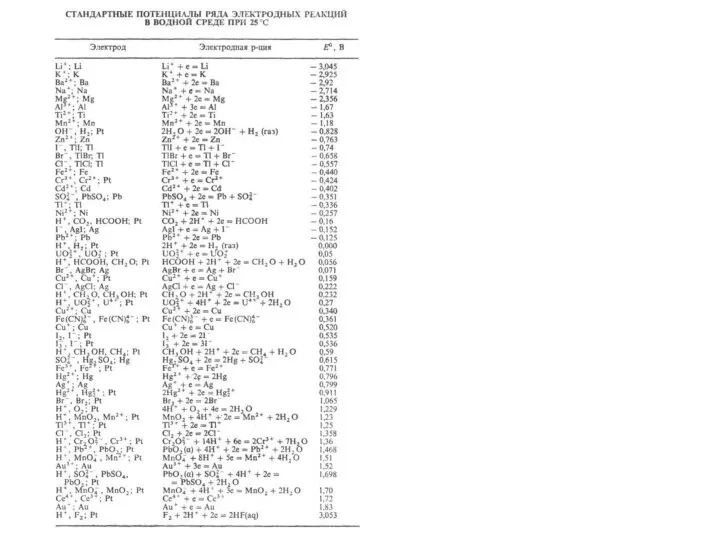
 НАШ НЕБЕЗПЕЧНИЙ ПОБУТ Презентація на тему того,про що ми не думаємо у повсякденному житті.
НАШ НЕБЕЗПЕЧНИЙ ПОБУТ Презентація на тему того,про що ми не думаємо у повсякденному житті.  Решение задач на долю вещества в растворе с участием кристаллогидратов
Решение задач на долю вещества в растворе с участием кристаллогидратов Бензол молекуласында байланыстардың түзілу сызбанұсқасы
Бензол молекуласында байланыстардың түзілу сызбанұсқасы Дисперсные системы и растворы
Дисперсные системы и растворы Общая характеристика элементов главной подгруппы второй группы
Общая характеристика элементов главной подгруппы второй группы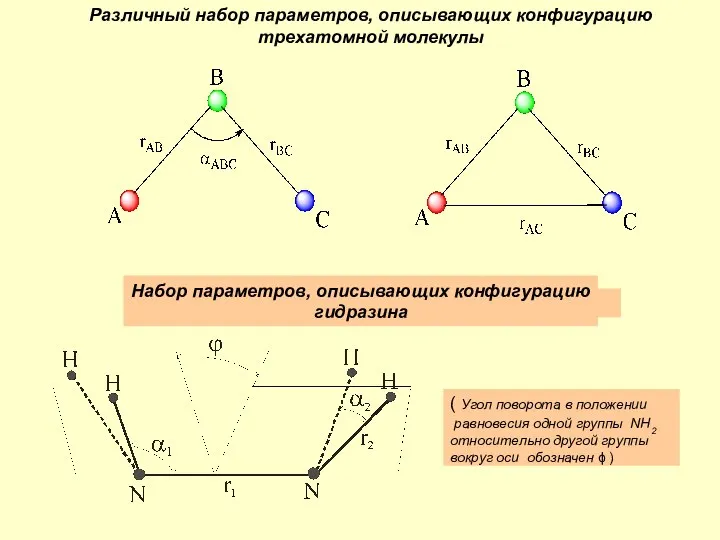 Различный набор параметров, описывающих конфигурацию трехатомной молекулы
Различный набор параметров, описывающих конфигурацию трехатомной молекулы Metode electrochimice. Generalităţi
Metode electrochimice. Generalităţi Обмен нуклеотидов. (Лекция 13)
Обмен нуклеотидов. (Лекция 13) Техника безопасности на уроках химии_
Техника безопасности на уроках химии_ Производные индола
Производные индола Диагенез и катагенез горных пород
Диагенез и катагенез горных пород The molecular basis of inheritance. (Chapter 16)
The molecular basis of inheritance. (Chapter 16) Алкан «бутан» (C4H10)
Алкан «бутан» (C4H10) Словарь просторечных молодёжных слов
Словарь просторечных молодёжных слов Свойства простых веществ 8 класс
Свойства простых веществ 8 класс Экологическая оценка качества воды поверхностных водоемов г. Донецка
Экологическая оценка качества воды поверхностных водоемов г. Донецка Презентация по Химии "Презентация Коррозия металлов" - скачать смотреть
Презентация по Химии "Презентация Коррозия металлов" - скачать смотреть  Химическая связь
Химическая связь Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі
Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі Основные химические понятия
Основные химические понятия Углеводороды: классификация
Углеводороды: классификация Современные оборудования в лаборатории
Современные оборудования в лаборатории Адские задания. ЕГЭ по химии
Адские задания. ЕГЭ по химии Нитрофенилалкиламины
Нитрофенилалкиламины Хімічні методи підвищення продуктивності свердловини
Хімічні методи підвищення продуктивності свердловини Аміни
Аміни Виды присадок к моторным топливам (бензин)
Виды присадок к моторным топливам (бензин) Биологическая химия с основами физической и коллоидной химии
Биологическая химия с основами физической и коллоидной химии