Содержание
- 2. Внутри молекул имеется запас энергии. Эта энергия может быть высвобождена в виде: теплоты при сгорании топлива;
- 3. Системы, состояния и функции состояния Можно условно считать, что вселенная состоит из двух частей: системы и
- 4. Например, на рисунке ниже показано, что реакционный сосуд может иметь тепловой контакт с окружением, машина –
- 6. Итак, система может произвести работу, или над ней будет произведена работа; она может отдать тепло и
- 7. dU = dq + dw (1) Условимся, что dq имеет положительный знак, если теплота переходит к
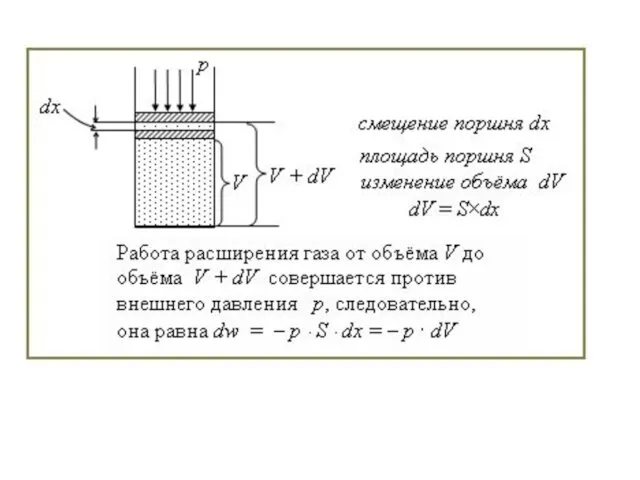
- 8. Термодинамическое понятие работы легче всего рассмотреть на системе, представляющей собой цилиндр с идеальным газом и поршнем.
- 9. Это уравнение (2) иллюстрируется рисунком (1). Сила, действующая на поршень со стороны атмосферы, равна произведению площади
- 11. Работа на отрезке от xн до xк равна : (если р = const) (3)
- 12. Теперь рассмотрим термодинамическое понятие теплоты. Если через стенки в систему переходит количество теплоты dq, то её
- 13. Константа С называется теплоёмкостью системы. Теплоёмкость 1 моля вещества называется мольной теплоёмкостью и обозначается символом Сm.
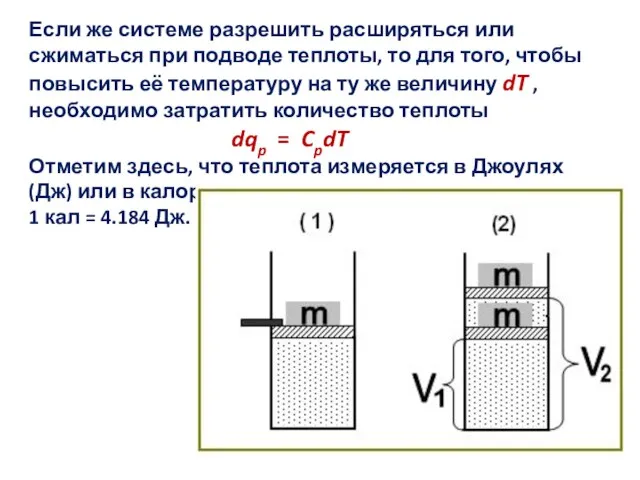
- 14. Если же системе разрешить расширяться или сжиматься при подводе теплоты, то для того, чтобы повысить её
- 15. Рассмотрим рисунок. В первом случае газ находится в цилиндре под поршнем, на котором лежит груз m,
- 16. Очевидно далее, что CvdT есть теплота, переданная телу но её можно связать с увеличением внутренней энергии.
- 17. Это определение пока что формально. Запишем полный дифференциал функции H. Из её определения: (5) По первому
- 18. Итак, Этот новый параметр H окажется очень полезным, у него особое название ЭНТАЛЬПИЯ или теплосодержание. Итак,
- 19. СОСТОЯНИЯ В термодинамике систему определяют её состоянием. Под этим разумеют, что она имеет какие-то свойства. Например,
- 20. Предположим, что мы перешли из одного состояния системы, характеризуемого функциями (параметрами) в другое Так вот, изменение
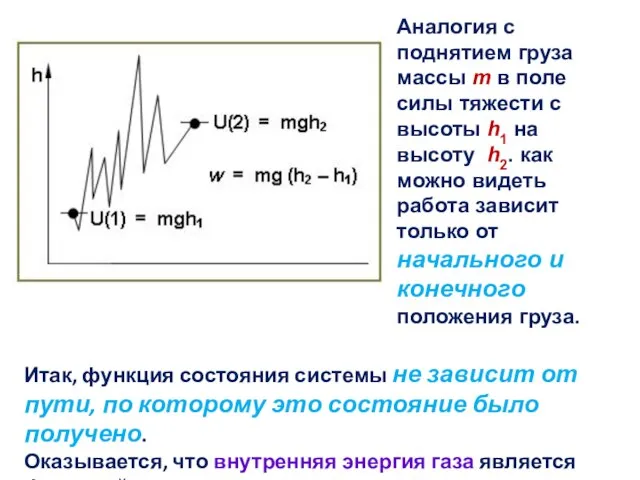
- 21. Аналогия с поднятием груза массы m в поле силы тяжести с высоты h1 на высоту h2.
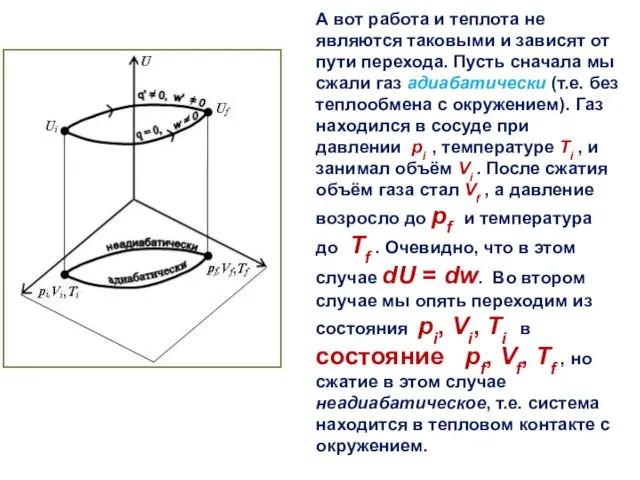
- 22. А вот работа и теплота не являются таковыми и зависят от пути перехода. Пусть сначала мы
- 23. Внутренние энергии начального и конечного состояния не изменятся, так как они являются функциями состояния, а теплота
- 24. Оказывается, энтальпия тоже является функцией состояния. Зачем же нам понадобилась эта функция? Оказывается, удобно описывать состояние
- 25. ТЕПЛОТЫ ХИМИЧЕСКИХ РЕАКЦИЙ Мы рассмотрим реакционный сосуд, как термодинамическую систему. К счастью очень большое число химических
- 26. Итак, мы установили идентичность термохимически наблюдаемых величин ( ) ( ) или с изменением термодинамических функций
- 27. Очевидно, что парообразные молекулы воды, полученные по реакции (а), должны выделить теплоту парообразования при конденсации в
- 28. Если и исходные вещества и конечные продукты находятся в стандартных состояниях, то Теплота выделяется, когда теплосодержание
- 29. ЗАКОН ГЕССА Закон Гесса является следствием того факта, что энтальпия - есть функция состояния. Следовательно, если
- 30. Закон Гесса состоит в том, что изменение энтальпии любой реакции можно выразить в виде суммы изменений
- 31. Уравнения (1) – (4) дают в сумме уравнение (5) есть сумма значений продуктов реакции - сумма
- 33. Скачать презентацию


























 Ядра и частицы
Ядра и частицы Водородная связь
Водородная связь Этанол. Одноатомный спирт
Этанол. Одноатомный спирт Химия полимерных материалов для буровых растворов. Лекция 3. Технологические жидкости для бурения скважин
Химия полимерных материалов для буровых растворов. Лекция 3. Технологические жидкости для бурения скважин Классификация неорганических веществ
Классификация неорганических веществ Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно
Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно Дизельное топливо
Дизельное топливо Гидролиз солей
Гидролиз солей Дисперсные системы
Дисперсные системы Синтетические лекарственные препараты
Синтетические лекарственные препараты Неорганическое композиционное антикоррозионное покрытие для защиты стальных деталей и особенности его формирования
Неорганическое композиционное антикоррозионное покрытие для защиты стальных деталей и особенности его формирования Образовательная программа дополнительного образования «Химия в центре наук»
Образовательная программа дополнительного образования «Химия в центре наук» Configuratia electronica. Sistemul periodic al elementelor. (Curs 3)
Configuratia electronica. Sistemul periodic al elementelor. (Curs 3) Хромотография, явления, атомы и молекулы. 8 класс
Хромотография, явления, атомы и молекулы. 8 класс Дюралюминий. Дюраль
Дюралюминий. Дюраль Роль металлов в истории человеческой цивилизации
Роль металлов в истории человеческой цивилизации Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства Кремний – бог неорганической природы
Кремний – бог неорганической природы Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н.
Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н. Металлы и их соединения
Металлы и их соединения Биогеохимиялық шет аймақтар туралы түсінік
Биогеохимиялық шет аймақтар туралы түсінік Аминокислоты Модели молекул
Аминокислоты Модели молекул Органическая химия
Органическая химия Обмен нуклеотидов. Матричные биосинтезы
Обмен нуклеотидов. Матричные биосинтезы Основы безопасности при уничтожении химического оружия
Основы безопасности при уничтожении химического оружия Химические волокна. Свойства и технология производства
Химические волокна. Свойства и технология производства Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы
Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы Минеральные удобрения
Минеральные удобрения