Содержание
- 2. Атомы углерода способны образовывать друг с другом не только двойные, но и тройные связи.
- 3. Алкины (ацетиленовые углеводороды) — алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна тройная
- 4. Ацетилен (этин) (С2Н2) Н3С—СН3 Этилен (этен) (С2Н4) Этан (С2Н6)
- 5. Алкины образуют свой гомологический ряд с общей формулой СnH2n-2. СnН2n–2
- 6. Строение алкинов Ацетилен (этин) (С2Н2) Н:С:::С:Н Первым и основным представителем гомологического ряда алкинов является ацетилен или
- 7. Строение алкинов Тройная связь короче и прочнее двойной связи. Она образована тремя парами электронов и включает
- 8. По названию первого представителя этого ряда — ацетилена — эти непредельные углеводороды называют ацетиленовыми. Строение алкинов
- 9. Модели пространственного строения молекулы ацетилена А — тетраэдрическая Б — шаростержневая В — по Бриглебу С
- 10. Строение алкинов В алкинах атомы углерода находятся в третьем валентном состоянии sp-гибридизации. Между углеродными атомами возникает
- 11. Строение алкинов Ацетилен (этин) (С2Н2) Длина тройной связи равна 0,12 нм, а энергия её образования составляет
- 12. Номенклатура алкинов Ацетилен (этин) (С2Н2) Ацетиленовые углеводороды называют, заменяя в алканах суффикс -ан на суффикс -ин.
- 13. Номенклатура алкинов Венилацетилен (С4Н4) Если молекула содержит одновременно и двойную, и тройную связи, то предпочтение в
- 14. Номенклатура алкинов Венилацетилен (С4Н4) По рациональной номенклатуре алкиновые соединения называют, как производные ацетилена.
- 15. Номенклатура алкинов Этилацетилен (бутин-1) Диметилацетилен (бутин-2) Пропин
- 16. Номенклатура алкинов 3-метилбутин-1 (С5Н8)
- 17. Ацетилен или этин — бесцветный газ, без запаха. Ацетилен мало растворим в воде, хорошо — в
- 18. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
- 19. Ацетилен (этин) (С2Н2) Н:С:::С:Н Простейшим представителем углеводородов с тройной связью является ацетилен — родоначальник гомологического ряда
- 20. Впервые ацетилен был выделен в 1836 году Эдмундом Дэви при разложении водой карбида калия, полученного при
- 21. Свойства ацетилена
- 22. М. Бертло 1827–1907 гг. В 1860 г. Марселен Бертло впервые получил ацетилен в разряде дуги между
- 23. Алкины — это ненасыщенные углеводороды, которые в своём составе имеют тройную связь. Ацетилен
- 24. Физические свойства алкинов При обычных условиях: 1. С2–С4 — газы; 2. C5–C16 — жидкости; 3. начиная
- 25. Физические свойства алкинов
- 26. Физические свойства алкинов Растворимость низших алкинов в воде несколько выше, чем алкенов и алканов, однако она
- 27. Химические свойства алкинов Алкины способны вступать в реакции присоединения, замещения, полимеризации и окисления. Этилацетилен (бутин-1) Пропин
- 28. Ацетилен (этин) (С2Н2) Н:С:::С:Н Простейшим представителем углеводородов с тройной связью является ацетилен — родоначальник гомологического ряда
- 29. Впервые ацетилен был выделен в 1836 году Эдмундом Дэви при разложении водой карбида калия, полученного при
- 30. Свойства ацетилена
- 31. М. Бертло 1827–1907 гг. В 1860 г. Марселен Бертло впервые получил ацетилен в разряде дуги между
- 32. Алкины — это ненасыщенные углеводороды, которые в своём составе имеют тройную связь. Ацетилен
- 33. Физические свойства алкинов При обычных условиях: 1. С2–С4 — газы; 2. C5–C16 — жидкости; 3. начиная
- 34. Физические свойства алкинов
- 35. Физические свойства алкинов Растворимость низших алкинов в воде несколько выше, чем алкенов и алканов, однако она
- 36. Химические свойства алкинов Алкины способны вступать в реакции присоединения, замещения, полимеризации и окисления. Этилацетилен (бутин-1) Пропин
- 37. Реакция присоединения CH3—C—СН → CH3—CСl—СН2 → CH3—CСl2—СН3 — — — HCl HCl
- 38. Химические свойства алкинов Углеродные атомы в молекулах алкинов расположены ближе друг к другу, чем в алкенах,
- 39. π-электроны, находясь ближе к ядрам углерода, проявляют несколько меньшую активность в реакциях электрофильного присоединения. Образование тройной
- 40. Реакция присоединения спиртов к алкинам НC—СН + С2H5ОН → C2H5—О—СН—СН2 — — —
- 41. НC—С—СН3 → CH2—CH—СН3 → CH3—CH2—СН3 — +Н2 t, Ni +Н2 t, Ni — — Реакция гидрирования
- 42. НC—СН → BrHC—СНBr → Br2HC—CHBr2 +Br2 — Реакция галогенирования +Br2 — — 1,2-дибромэтен 1,1,2,2-тетрабромэтан
- 43. Реакция присоединения галогеноводородов 2-бромпропен 2,2-дибромпропан
- 44. Замещение водородных атомов ацетилена на металлы, называется реакцией металлирования. В результате образуются металлические производные ацетилена —ацетилениды.
- 45. Реакция металлирования — —
- 46. С ацетиленидами в сухом виде следует обращаться очень осторожно: они крайне взрывоопасны.
- 47. Реакция изомеризации Бутин-1 — — — Бутин-2 Na (спирт. р-р)
- 48. Ацетилен в зависимости от условий реакции способен образовывать различные продукты полимеризации — линейные или циклические.
- 49. Реакция полимеризации НС—CН + НС—СН → HC—СН—СН—CH2 Винилацетилен Cu2Cl2 — — —
- 50. Реакция полимеризации 3НС—CН → CН2—СН—С—CH—3С2Н 2 →С6Н6 Бензол — t °С
- 51. М. Бертло 1827–1907 гг. Реакцию полимеризации открыл французский учёный Марселен Бертло.
- 52. Уксусная кислота Синтетический каучук Перчатки из поливинилхлорида Растворитель Doudnick_Val
- 53. Кислородно-ацетиленовое соединение используют для сварки металлов.
- 55. Скачать презентацию




















































 Кинетика химических реакций. (Лекция 12)
Кинетика химических реакций. (Лекция 12) Углеводороды. Природный газ. Алканы
Углеводороды. Природный газ. Алканы Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура соединений
Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура соединений Исследование химического состава шоколада и способов его приготовления
Исследование химического состава шоколада и способов его приготовления Природные источники углеводородов
Природные источники углеводородов Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ
Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ Химические свойства карбокатионов
Химические свойства карбокатионов Аттестационная работа. Многогранники: от молекулы до кристалла
Аттестационная работа. Многогранники: от молекулы до кристалла Химия переходных элементов
Химия переходных элементов ОКСИДИ – це бінарні сполуки , що складаються з двох елементів , одним з яких є Оксиген . Загальна формула оксидів : E2On n – вале
ОКСИДИ – це бінарні сполуки , що складаються з двох елементів , одним з яких є Оксиген . Загальна формула оксидів : E2On n – вале Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие
Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров
ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров Презентация по Химии "Азотная кислота" - скачать смотреть
Презентация по Химии "Азотная кислота" - скачать смотреть  Історія виникнення мила Розмаїтого Дмитра, 9-Б клас
Історія виникнення мила Розмаїтого Дмитра, 9-Б клас  Электрохимические методы анализа. Лекция 3
Электрохимические методы анализа. Лекция 3 Тривиальные названия неорганических соединений
Тривиальные названия неорганических соединений Структура аминокислот
Структура аминокислот Дифференцированный подход в обучении химии
Дифференцированный подход в обучении химии Физико-химические методы анализа
Физико-химические методы анализа Кинетические методы анализа
Кинетические методы анализа Полипропилен. Молекулалық құрылымы
Полипропилен. Молекулалық құрылымы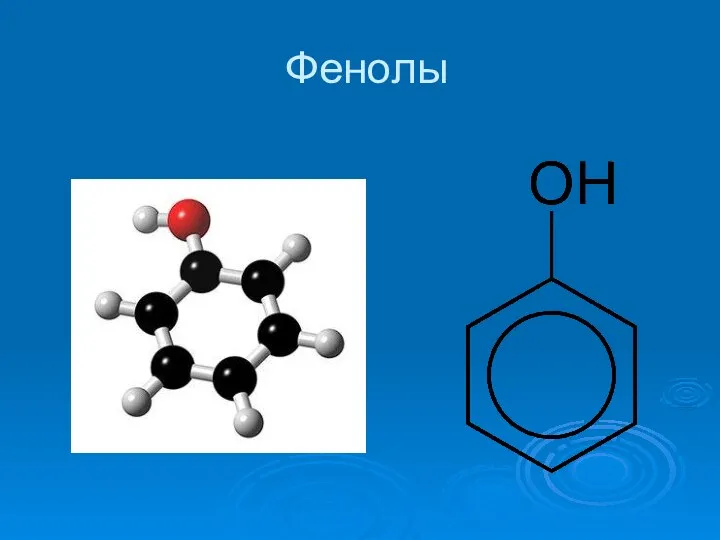 Фенолы. Физические свойства. Получение
Фенолы. Физические свойства. Получение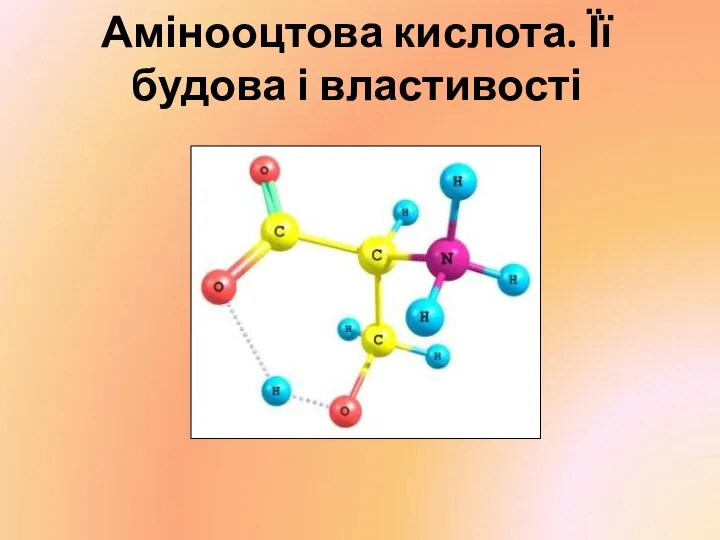 Амінооцтова кислота. Її будова і властивості
Амінооцтова кислота. Її будова і властивості Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері
Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері Пища, с точки зрения химика
Пища, с точки зрения химика Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией
Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией  Классификация минералов по химическому принципу
Классификация минералов по химическому принципу