Ерiтiндiлер туралы iлiм. Сұйытылған бейэлектролит және электролит ерiтiнндiлерiнiң коллигативтiк қасиеттерi
Содержание
- 2. Мақсаты: Сұйық ерiтiндiлердiң ерiген заттың санына тәуелдi – коллигативтi қасиеттерiн қарау ағзадағы процесстерді түсінуге мүмкіндік береді.
- 3. Дәрiс жоспары. Ерiтiндiлер. Ағза тiршiлiгiндегi ерiтiндiлердiң манызы. Бейэлектролит ерітінділерінің коллигативті қасиеттері. Рауль заңы және оның салдары
- 4. Дәрiс тезистерi Еріген заттан, еріткіштен және олардың өзара әрекеттесуінен түзілген өнімдерден тұратын біртекті жүйе қалай аталады?
- 5. Ерітінді
- 6. Ерітінділер қатты (құймалар), сұйық (дәрілік заттардың судағы немесе спирттегі ерітінділері), газ тәріздес (ауа) болады. Медицина үшін
- 7. Температураны жоғарлатқанда әдетте газдардан басқа заттардың ерігіштік қасиеті өседі. Газдардың ерігіштігіне қысым да әсер етеді. Генри
- 8. Сұйытылған ерітінділердің коллигативтік қасиеттері еріген заттың бөлшектерінің санына тәуелді, олардың табиғатына тәуелсіз: ерітінді үстіндегі бу қысымының
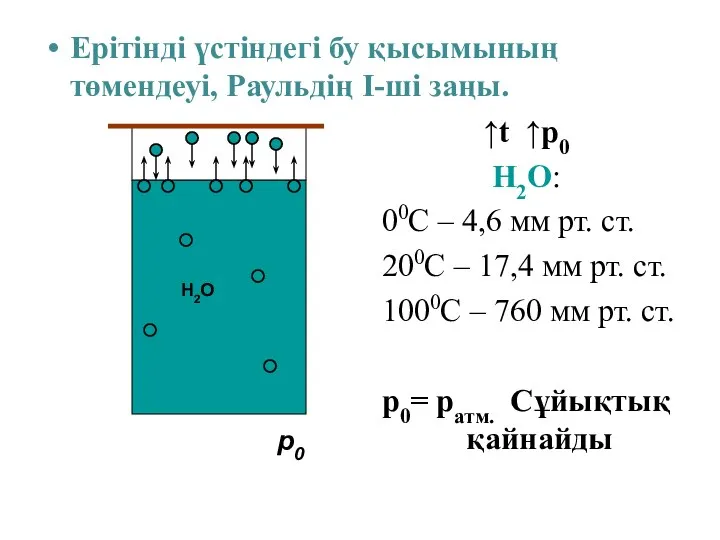
- 9. Ерітінді үстіндегі бу қысымының төмендеуі, Раульдің І-ші заңы. p0 ↑t ↑p0 H2O: 00C – 4,6 мм
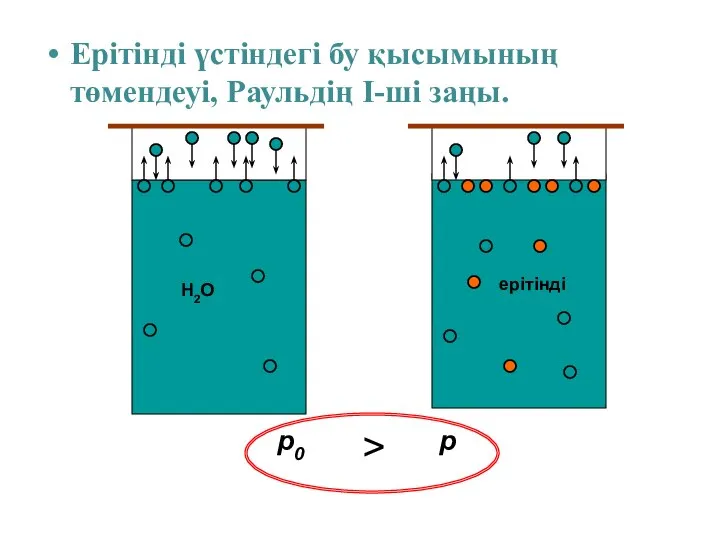
- 10. Ерітінді үстіндегі бу қысымының төмендеуі, Раульдің І-ші заңы. p0 p >
- 11. Франсуа Мари Рауль (фр. François-Marie Raoult; 10 мамыр1830, Фурн-ан-Веп, Нор, — 1 сәуір1901, Гренобль) — француз
- 12. Раульдің бірінші заңы: электролит емес заттардың сұйытылған ерітінділерінің үстіндегі бу қысымының салыстырмалы төмендеуі еріген заттың молярлық
- 13. Рауыльдің екінші заңы: электролит емес ерітінділердің қайнау температурасының жоғарылауы және қату температурасының төмендеуі еріген заттың молярлық
- 14. Сm – моляльді концентрация – 1 кг еріткіштегі еріген заттың мольманы(моль/кг): m ер. зат Cm =
- 15. Криометрия –қату температурасы бойынша заттың молярлық массасын (М) анықтау әдісі: Кз · m ер.зат М ер.зат
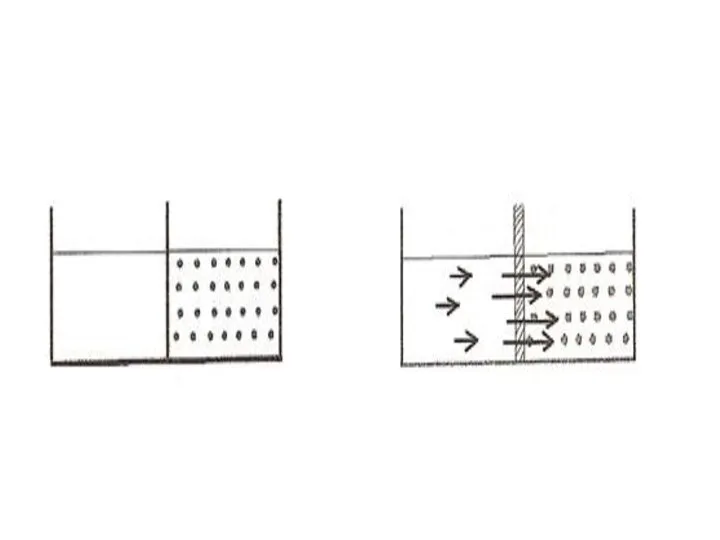
- 17. Осмос. Осмос қысымы. Шала өткізгіш арқылы бір бағытта жүретін диффузияны осмос дейді (осмос-итеру, басу). Осмос ерітінділердің
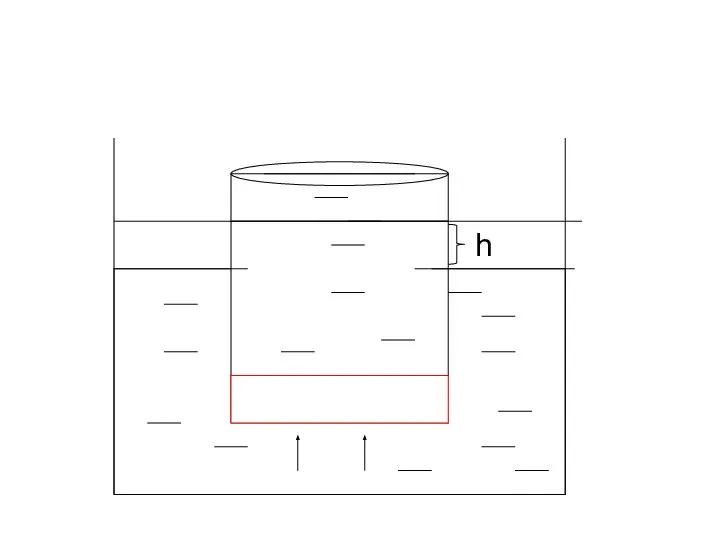
- 18. һ
- 19. Қант ерітіндісінің концентрациясы кемиді, сыртқы ыдыстан енген су ерітіндінің көлемін үлкейтеді, ерітінді түтікпен жоғары көтеріледі. Түтікте
- 20. Якоб Хендрик Вант-Гофф (нидерл. Jacobus Henricus (Henry) van 't Hoff; 30 тамыз1852, Роттердам — 1 наурыз1911,
- 21. Осмос қысымы ерітілген зат бөлшектерінің тегіне емес, олардың санына тәуелді болады. Вант- Гофф ашқан заң бойынша:
- 23. Осмостың мәні Жасушаның, тіннің, ағза түрлерінің серпімділігі ⮚ тағамның қорытылуы, лимфаның, несептің түзілуі ⮚дәрінің әсері ⮚осмостың
- 24. Қанның осмос қысымы Қан плазмасының құрамы: 90 % Н2О, 7 % ақуыздар, 0,9 % эл-т (>
- 25. Бірдей температурада концентрациясы бірдей екі ерітіндінің осмос қысымы да тең болса, олар изотоникалық ерітінділер деп аталады.
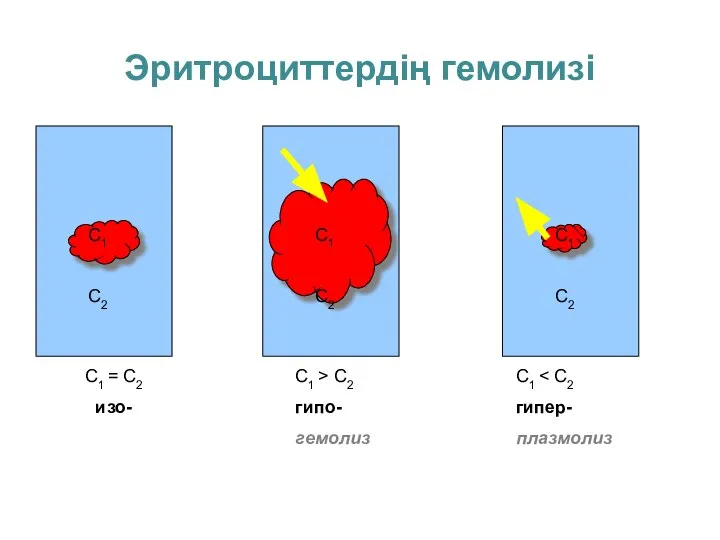
- 26. Эритроциттердің гемолизі
- 27. Электролит ерітінділердің коллигативті қасиеттері Электролит ерітінділерінде диссоциация есебінен бөлшектер саны көп болады. Вант-Гофф электролиттердің диссоциациясын есепке
- 28. Күшті электролиттер үшін (α≈1): i = 1+ α (n – 1) NaCl ↔ Na+ + Cl-
- 29. Кері байланыс: Медициналық аспаптарды залалсыздандыру үшін тұздық ерітінділерді қолдануға болады. Осы әсердің механизмін түсіндіріңіз. Қандай ерітіндінің
- 31. Скачать презентацию























 Хімія в побуті
Хімія в побуті Металлы
Металлы Развитие учебной мотивации на уроках химии через систему урочной и внеурочной деятельности
Развитие учебной мотивации на уроках химии через систему урочной и внеурочной деятельности Кислоты и соли. (8 класс)
Кислоты и соли. (8 класс) Вермикулит. Технические характеристики
Вермикулит. Технические характеристики Минералы и Близнецы
Минералы и Близнецы Биологическое окисление
Биологическое окисление Общая характеристика ферментов как биологических катализаторов
Общая характеристика ферментов как биологических катализаторов Оксиды ангидриды
Оксиды ангидриды Презентация по Химии "ПЛАСТМАССА" - скачать смотреть
Презентация по Химии "ПЛАСТМАССА" - скачать смотреть  Презентация по Химии "Презентація на тему: Природний газ" - скачать смотреть бесплатно
Презентация по Химии "Презентація на тему: Природний газ" - скачать смотреть бесплатно Выращивание кристаллов Выполнил: ученик 8 класса А Алексеев Ден
Выращивание кристаллов Выполнил: ученик 8 класса А Алексеев Ден Хлор. Способы получения хлора
Хлор. Способы получения хлора Положение тугоплавких металлов в Периодической системе элементов
Положение тугоплавких металлов в Периодической системе элементов Фильтрационные свойства.Решение уравнений Стокса для несжимаемой жидкости
Фильтрационные свойства.Решение уравнений Стокса для несжимаемой жидкости Дисперсные системы
Дисперсные системы Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток
Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток Что объединяет эти вещества?
Что объединяет эти вещества?  Щелочноземельные металлы
Щелочноземельные металлы Теория растворов. Растворы электролитов
Теория растворов. Растворы электролитов Металлы 4 группы А подгруппы
Металлы 4 группы А подгруппы Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение МОУ средняя общеобразовательная школа с. Минаевки Асиновского района Томской области урок подготовила : учитель 1 категории Суц
МОУ средняя общеобразовательная школа с. Минаевки Асиновского района Томской области урок подготовила : учитель 1 категории Суц Нефть: состав, свойства, месторождения, применение
Нефть: состав, свойства, месторождения, применение Технология вакуумной перегонки мазута
Технология вакуумной перегонки мазута Метаболизм липидов. Метаболизм глицерофосфолипидов и холестерола. (Лекция 3)
Метаболизм липидов. Метаболизм глицерофосфолипидов и холестерола. (Лекция 3) Органічні сполуки. Вплив на організм людини Учениця 11-Б класу Колчаг Юлія
Органічні сполуки. Вплив на організм людини Учениця 11-Б класу Колчаг Юлія