Содержание
- 2. В металл – водородных (M-H) системах, реализованы все виды химических связей: ионная, ковалентная и металлическая. Но
- 3. 4.1 Введение к фазовым диаграммам Некоторые примеры фазовых диаграмм показаны на рис.. 4.1 - 4. На
- 4. Перед началом обсуждения этих особенностей есть смысл сделать следующий, комментарий по значению и использованию диаграмм x-T.
- 5. Поэтому, при построении фазовой диаграммы системы Pd−D (рис. 4.1), например, мы должны делать ряд изотермических измерений
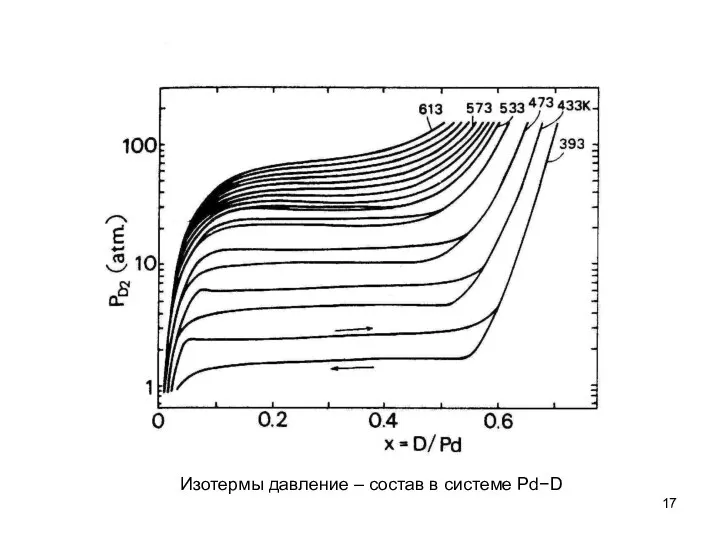
- 6. Изотермы давление – состав в системе Pd−D
- 7. Появление плато на изотерме подразумевает, что два гидрида (дейтерида) сосуществует в этой области. Правило фаз Гиббса
- 8. В большинстве других переходных металлах поверхностные состояния, блокирующие проникновение водорода легко формируются при экспозиции и ограничивают
- 9. Обычная практика для формирования порошковых образцов должна повторять циклы нагревание - охлаждение при 400÷500 °C достаточное
- 10. Введение к фазовым диаграммам Рис.4.1. Фазовая диаграммы Pd−H и Pd−D. Отсутствует информация об упорядоченных фазах с
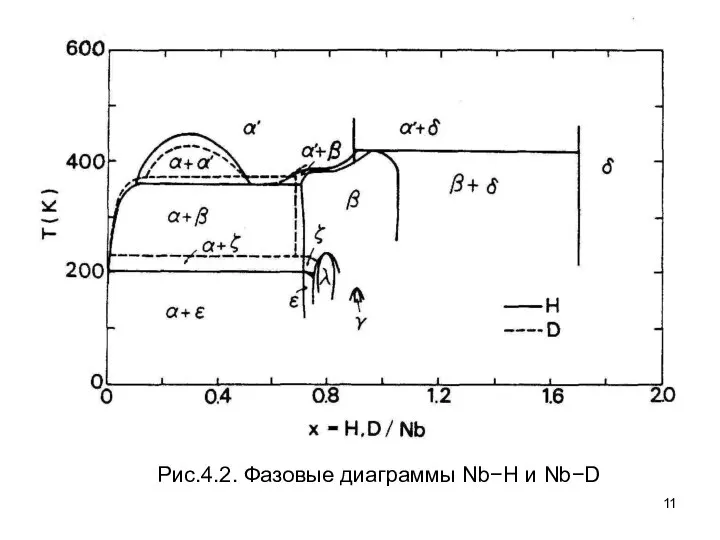
- 11. Рис.4.2. Фазовые диаграммы Nb−H и Nb−D
- 12. Рис.4.3. Фазовые диаграммы V−H, V−D
- 15. Таким образом, при построении фазовой диаграммы системы Pd - D (рис. 4.1), например, мы должны делать
- 16. Правило фаз Гиббса показывает, что в двухкомпонентных системах, существующих в трех различных фазах одновременно (две гидридных
- 17. Изотермы давление – состав в системе Pd−D
- 18. В большинстве других переходных металлах, поверхностные состояния, блокирующие проникновение водорода легко формируются при экспозиции, и ограничивают
- 19. Так как объемная диффузия водорода идет довольно быстро, кинетика твердо - газового насыщения обычно определяется проникновением
- 20. Рис.4.5. Арениусовские кривые для p(1-x)2/x2 для водорода и дейтерия в палладии по данным различных авторов
- 21. 4.2. Образование твердых растворов 4.2.1. Низкие концентрации – идеальные твердые растворы При данной температуре растворимость водорода
- 22. Рассмотрим условие теплового равновесия между твердым раствором и H2 газом, Условие дается равенством химического потенциала водорода
- 23. где μg - химический потенциал газообразного водорода на молекулу, μa является таковым для водорода в твердом
- 32. Закон Сивертса соблюдается, прежде всего, потому, что Н2 молекулы разделяются на атомы при растворении в металлах,
- 33. Арениусовские кривые для p(1-x)2/x2 для водорода и дейтерия в палладии по данным различных авторов
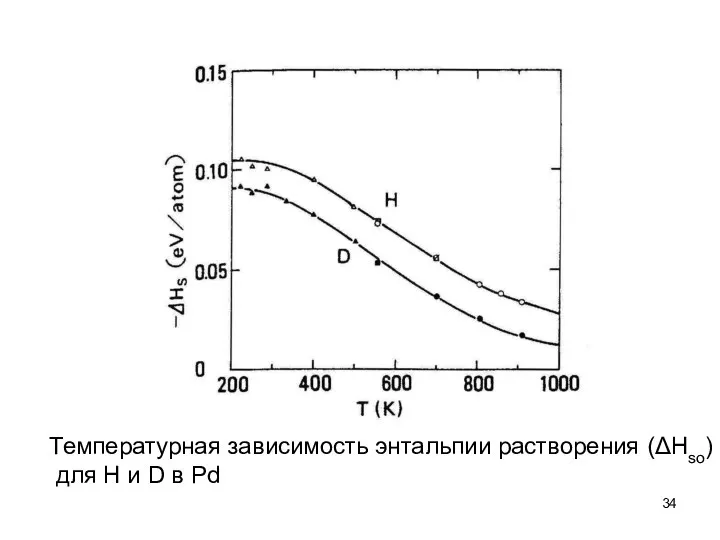
- 34. Температурная зависимость энтальпии растворения (ΔHso) для H и D в Pd
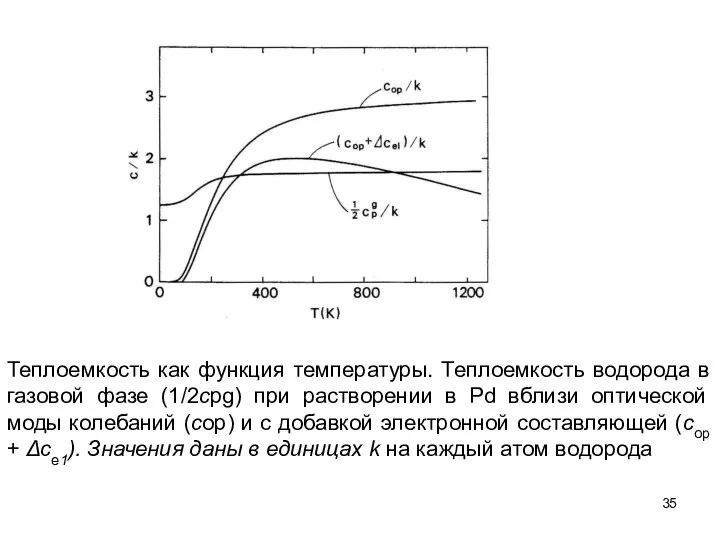
- 35. Теплоемкость как функция температуры. Теплоемкость водорода в газовой фазе (1/2сpg) при растворении в Pd вблизи оптической
- 36. В заключение этого раздела можно сделать некоторый общий комментарий к закону Сивертса. Закон Сивертса соблюдается прежде
- 37. Высокие концентрации. Взаимодействие между атомами водорода Концентрационная зависимость ΔHs должна быть следствием взаимодействий между растворенными H
- 38. Таблица 4.2. Зависимость теплоты растворения от концентрации водорода. Значения коэффициентов даны в линейном приближении Примечание: a
- 39. . Зависимость энтальпии растворения от концентрации водорода в различных металлах
- 40. Избыточная парциальная конфигурационная энтропия как функция концентрации водорода для тетрапор в ОЦК решетке (единицы от k).
- 41. Отметим три обстоятельства, которые указывают на присутствие этого близкодействующего отталкивающего взаимодействия. Во-первых, имеется эмпирическое правило, согласно
- 42. Конфигурационная энтропия меньше, потому что r уменьшается при взаимной блокировке атомов H. Более точно, взаимная блокировка
- 43. Одно из важных последствий дальнего притягивающего H−H взаимодействия – спинодальный распад, как это наблюдается в Pd−H
- 44. Это так называемый закон общей касательной. Критическая точка может быть определена из условия Равновесное состояние для
- 45. Критическая точка может быть определена из условия (4.43) Простая аппроксимация для μa, как и прежде, имеет
- 46. (Для Ni, критическая точка была грубо зафиксирована при xc ~ 0.3, Tc ~ 660 К на
- 47. Рис. 4.10. Фазовая диаграмма Nb-H. Рассчитанная (⎯) и экспериментальная (------)
- 48. Особенность упругих дальнодействующих взаимодействий дает специфическую черту в спинодальном распаде, а именно зависимость формы границ области
- 49. Рис. 4.11. Когерентное и некогерентное состояния
- 50. В когерентном случае, так как напряжение, введенное атомами H, зависит от концентрации H, обычные моды напряжения
- 51. Показано, что когерентные макроскопические волны плотности растут только тогда, когда отожженные образцы имеют почти предельно допустимые
- 52. Таблица 1.1. Теплосодержание и энтропия растворения водорода в металлах в пределе низкой концентрации.
- 53. Таблица 1.1. Теплосодержание и энтропия растворения водорода в металлах в пределе низкой концентрации.
- 55. Скачать презентацию
















































 Титан. Физические свойства титана
Титан. Физические свойства титана Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі Энергетические эффекты реакций
Энергетические эффекты реакций Синтетичні речовини у сільському господарстві, медицині та промисловості Презентація на тему:
Синтетичні речовини у сільському господарстві, медицині та промисловості Презентація на тему:  Биохимия и молекулярная биология. Биосинтез мембранных липидов. Лекция 9
Биохимия и молекулярная биология. Биосинтез мембранных липидов. Лекция 9 Карбонильные соединения (оксосоединения)
Карбонильные соединения (оксосоединения) Углеводы
Углеводы Катализ.Лекция
Катализ.Лекция Тыңайтқыштар
Тыңайтқыштар Урок химии на тему: «Типы химических реакций»
Урок химии на тему: «Типы химических реакций» История мыловарения. Моющее действие мыла
История мыловарения. Моющее действие мыла Презентация по Химии "Открытия и изобретения в химии" - скачать смотреть
Презентация по Химии "Открытия и изобретения в химии" - скачать смотреть  Презентация на тему: Химия и производство
Презентация на тему: Химия и производство Периодическая система химических элементов Д.И. Менделеева и строение атома
Периодическая система химических элементов Д.И. Менделеева и строение атома Щелочные металлы
Щелочные металлы Презентация по Химии "Аммиак" - скачать смотреть
Презентация по Химии "Аммиак" - скачать смотреть  Аналитический скрининг
Аналитический скрининг Дослідження на тему: Повітря Христинівщини За проектом “Екологічна ситуація у рідному місті”
Дослідження на тему: Повітря Христинівщини За проектом “Екологічна ситуація у рідному місті” Растворы
Растворы Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату Адсорбционные взаимодействия
Адсорбционные взаимодействия Презентация по Химии "ГАЛЕРЕЯ РУССКИХ ХИМИКОВ" - скачать смотреть бесплатно
Презентация по Химии "ГАЛЕРЕЯ РУССКИХ ХИМИКОВ" - скачать смотреть бесплатно Презентация по Химии "Знакомство с кислотами" - скачать смотреть
Презентация по Химии "Знакомство с кислотами" - скачать смотреть  Основания. Классификация оснований
Основания. Классификация оснований Бинарные соединения
Бинарные соединения  Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Александрит
Александрит Фенол. Получение и использование, физические и химические свойства. Биологическая роль
Фенол. Получение и использование, физические и химические свойства. Биологическая роль