Содержание
- 2. Самыми распространёнными химическими системами, с которыми мы сталкиваемся в лаборатории и в природе, являются растворы. В
- 3. Более научная формулировка: Растворы могут существовать в любом агрегатном состоянии: твёрдом, жидком или газообразном, но они
- 4. МЕХАНИЗМЫ И ЭНЕРГЕТИКА РАСТВОРЕНИЯ. Всякий раствор состоит из растворённых веществ и растворителя, т.е. среды, в которой
- 5. При достижении равновесия ΔG = 0. Энергетической характеристикой процесса растворения является энтальпия растворения (ΔHраств.). Растворение одних
- 6. Например, 1) растворение твёрдого Al в щёлочи сопровождается химической реакцией – выделением водорода: 2 Al +
- 7. В то же время растворение СsBr, NaI или NH4NO3 в воде сопровождается заметным тепловым эффектом, но
- 8. В общем случае всегда верно это уравнение, где U – энергия решётки. Обычно, чем больше U
- 9. Это означает, что энергия сольватации NaCl в пересчёте на 1 моль ионов Na+ и 1 моль
- 10. Третий механизм растворения (помимо рассмотренных химического и сольватации) обусловлен действием дисперсионных сил, но энергетика и в
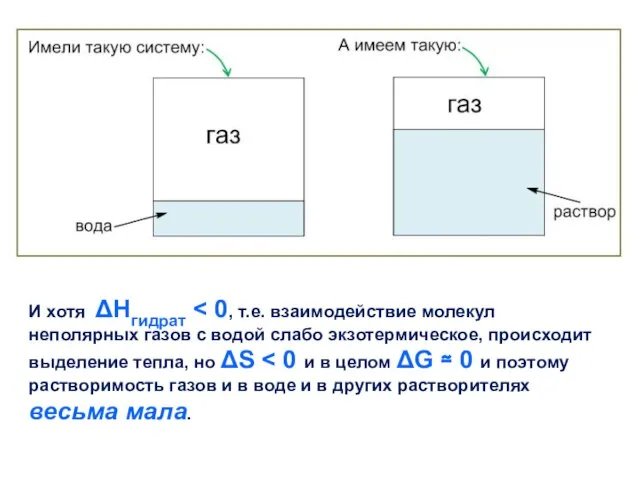
- 11. И хотя ΔHгидрат
- 12. Свойства растворов. Законы Генри, Рауля, Вант Гоффа. Прежде, чем перейти к рассмотрению этих законов мы рассмотрим
- 13. (3) Для вещества 2: для вещества 3: И очевидно, что
- 14. поскольку: Очевидно, что мольные доли представляют собой безразмерные единицы концентрации. Рассмотрим равновесие между жидкостью и растворёнными
- 15. В котором постоянная Генри kг является мерой растворимости газа. Таблица 1. Значения постоянной закона Генри для
- 16. Растворимость газов уменьшается: при повышении температуры; при растворении в воде полярных или ионных веществ – это
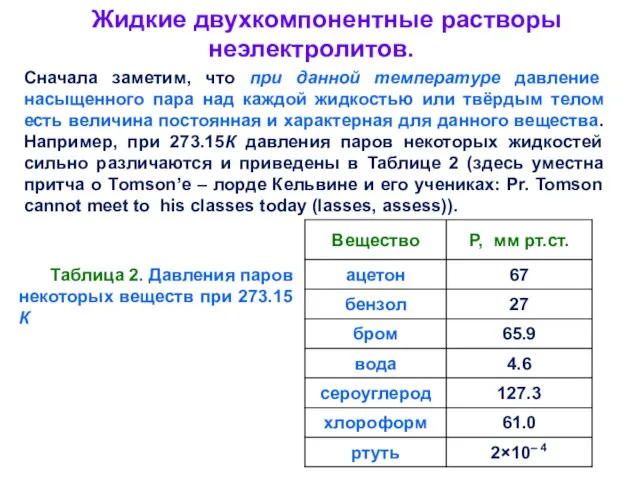
- 17. Жидкие двухкомпонентные растворы неэлектролитов. Сначала заметим, что при данной температуре давление насыщенного пара над каждой жидкостью
- 18. Пусть теперь мы растворили в некотором из этих растворителей нелетучее соединение, например сахарозу в воде, т.е.
- 19. Так вот, Рауль показал, что относительное понижение давления пара растворителя равно мольной доле растворённого вещества. Напомню
- 20. Рассмотрим рисунок: Рис.1. Давление пара растворителя в зависимости от температуры.
- 21. Из рисунка видно, что давление паров растворителя и над чистым растворителем и над раствором растёт при
- 22. ТОЧКА ЗАМЕРЗАНИЯ И ТОЧКА КИПЕНИЯ РАСТВОРОВ. Хорошо известно, что раствор замерзает при более низкой температуре, чем
- 23. Таблица 3. Криоскопические константы (К) чистых жидкостей.
- 24. Пример. Рассчитать, какое количество этилового спирта С2Н5ОН следует добавить к 5л воды, чтобы предотвратить её замерзание
- 25. Рассмотрим, что происходит при охлаждении раствора соли NaCl, скажем, 1М концентрации (например твёрдой СО2). Оказывается, что
- 26. Точно такое же соотношение, как и (6) имеется для повышения температуры кипения при растворении вещества по
- 27. Рис.3. Законы Рауля применительно к воде и водным растворам
- 28. Осмос
- 29. Осмосом называется явление массопереноса растворителя (например, воды) через полупроницаемую мембрану (целлофановую плёнку, пергаментную бумагу, мочевой пузырь
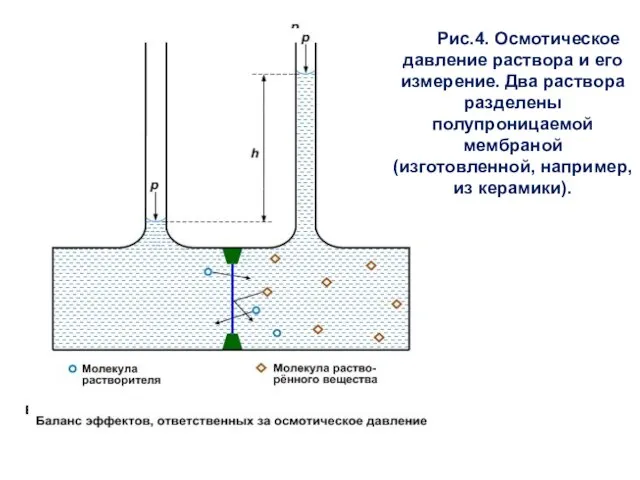
- 30. Рис.4. Осмотическое давление раствора и его измерение. Два раствора разделены полупроницаемой мембраной (изготовленной, например, из керамики).
- 31. В результате объём раствора в правой части сосуда увеличивается, что приводит к подъёму воды в узкой
- 32. πV = n RT , где π – осмотическое давление, V –объём раствора в правой части
- 33. Изучая растворы электролитов, исследователи (Аррениус, Вант-Гофф и др.) заметили, что растворы солей, кислот и оснований проявляют
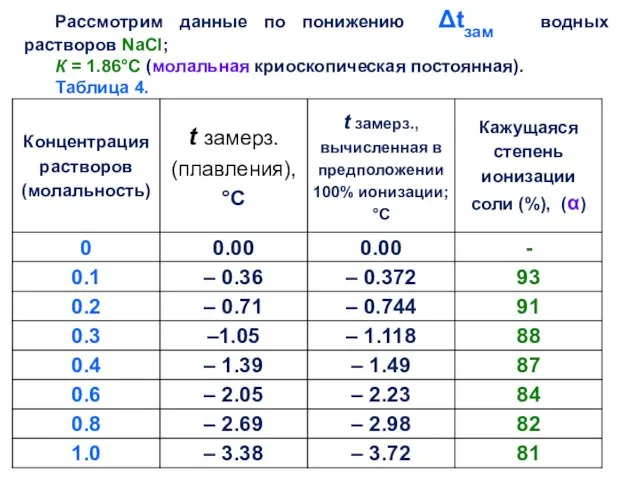
- 34. Рассмотрим данные по понижению Δtзам водных растворов NaCl; К = 1.86°С (молальная криоскопическая постоянная). Таблица 4.
- 35. Из таблицы видно, что при повышении концентрации влияние NaCl на температуру замерзания раствора оказывается таким, как
- 36. Итак, указанные отклонения свойств реальных растворов от свойств «идеальных» растворов с ионизованными на 100% электролитами объясняются
- 37. ИЗОТОНИЧЕСКИЙ КОЭФФИЦИЕНТ Вант-Гоффа Чтобы описать это отклонение от идеальной 100% ионизации или электролитической диссоциации существует несколько
- 38. Физический смысл изотонического коэффициента заключается в следующем: Очевидно, что для электролитов i > 1. Изотонические коэффициенты
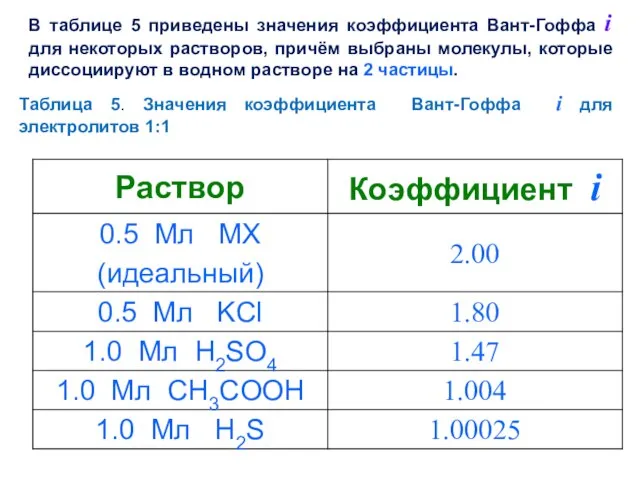
- 39. В таблице 5 приведены значения коэффициента Вант-Гоффа i для некоторых растворов, причём выбраны молекулы, которые диссоциируют
- 40. По существу коэффициент Вант-Гоффа указывает эффективное число ионных или молекулярных частиц, образующихся из единицы молекулярного количества
- 41. Степень диссоциации α Итак, мы видим, что различные электролиты диссоциированы по-разному. Количественной характеристикой способности электролита распадаться
- 42. Таблица 6. Степени диссоциации некоторых кислот (α) в водных растворах при концентрации 0.001 М и при
- 43. Очевидно, что между значениями i и α имеется связь. Пусть число молей электролита в данном объёме
- 44. Итак, в растворах сильных электролитов, у которых α близка к 1, имеются гидратированные ионы и реакции
- 45. КОНСТАНТА ДИССОЦИАЦИИ СЛАБОГО ЭЛЕКТРОЛИТА К динамическому равновесию, которое устанавливается в растворе слабого электролита между молекулами и
- 46. В числителе стоят концентрации продуктов диссоциации, а в знаменателе – концентрация недиссоциированных молекул. Эта величина, называемая
- 47. Равновесие (1) характеризуется константой диссоциации К1: Равновесие (2) характеризуется константой диссоциации К2: и, наконец, равновесие (3)
- 48. Суммарное равновесие: и ему соответствует константа равновесия: (это легко проверить) Аналогичным образом происходит ступенчатая диссоциация оснований
- 49. соответствуют две константы диссоциации: и при этом суммарной диссоциации : соответствует константа:
- 50. При ступенчатой диссоциации распад по каждой следующей ступени происходит в значительно меньшей степени, чем по предыдущей
- 51. Тогда константа равновесия: Это уравнение выражает собой закон разбавления Оствальда. Оно даёт возможность вычислить степень диссоциации
- 52. Следовательно: Степень диссоциации возрастает при разбавлении раствора (т.е. при уменьшении его концентрации С ). Этот вывод
- 53. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ.
- 54. При обычных условиях вода тоже является слабым электролитом. Она в слабой степени ионизована и равновесие её
- 55. Отсюда следует, что в чистой воде при 298 К [Н+] = [OH−] = = 10–7 моль/л.
- 56. Также очевидно, что поскольку всегда [H]·[OH]=10–14, то рН + рОН = 14. Также очевидно, что в
- 57. По определению α есть отношение числа диссоциированных молекул (или молей) NH4OH к числу растворенных молекул (молей)
- 58. ГИДРОЛИЗ Если в водном растворе присутствуют анионы слабой кислоты (например, карбонат – ион СО32– или ацетат
- 59. Говорят, что в этих случаях соли, а точнее ионы подвергаются гидролизу (в приведённых примерах ионы СО32–
- 60. Пусть мы наблюдаем гидролиз соли, содержащей анион А– слабой кислоты НА: А– + НОН ⇄ НА
- 61. Умножим это уравнение на дробь , тогда получим: (15)
- 62. В этом случае константа гидролиза есть отношение ионного произведения воды к константе ионизации слабой кислоты. Очевидно,
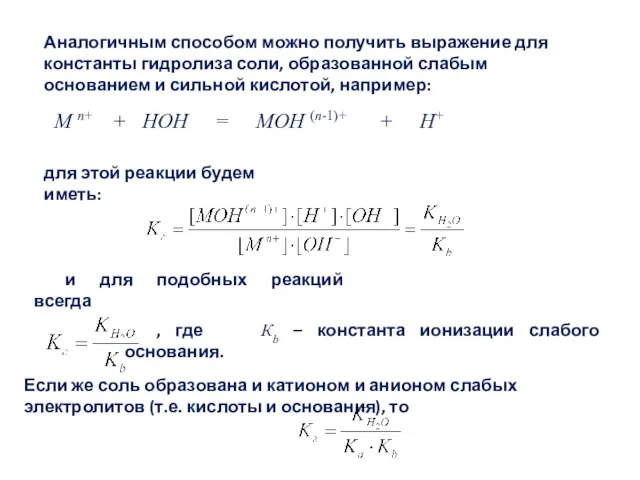
- 63. Аналогичным способом можно получить выражение для константы гидролиза соли, образованной слабым основанием и сильной кислотой, например:
- 64. Степень гидролиза h Степень гидролиза h соли (s) по смыслу очень близка к степени диссоциации слабого
- 65. А– + НОН ⇄ НА + ОН– (13) и И поскольку из (13) очевидно , что
- 66. В огромном числе случаев h очень мало по сравнению с 1, поэтому (h ≪1) Кг ≃
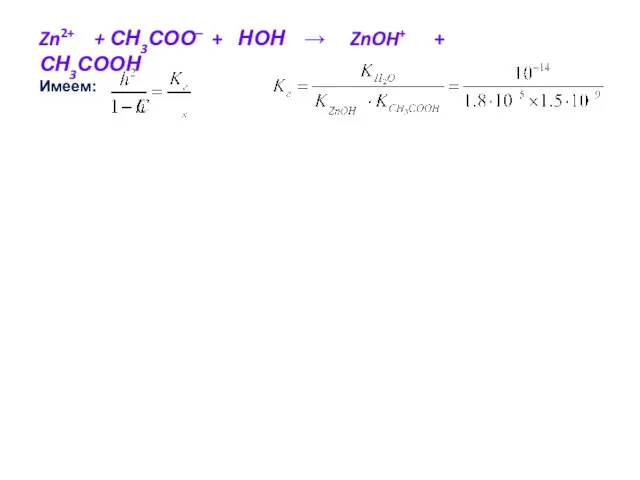
- 67. Пример. Найти степень гидролиза соли Zn(CH3COO)2 в растворе с концентрацией 0.05 моль/л. Эта соль образована слабой
- 68. Zn2+ + СН3СОО– + НОН → ZnOH+ + СН3СООН Имеем:
- 69. Решение задач по теме РАСТВОРЫ
- 70. Задачи 1. Сколько г Ni(HCOO)2 содержится в 11л 0.3M раствора? Найти его нормальность. 2. Написать реакцию
- 71. 7. Рассчитать pOH водного раствора KH2BO3, если Сs = 0.02M и Ka1= 5.83×10−10 6. В двух
- 73. РЕШЕНИЕ ЗАДАЧ
- 74. 1. Задача. Сколько г Ni(HCOO)2 содержится в 11л 0.3M раствора? Найти его нормальность. В 11л 0.3М
- 75. Реакция гидролиза соли NaHCO3 записывается так : 1. Na+ + HCO3‒ + H2O ⇄ Na+ +
- 76. Здесь поставлен верхний индекс (*), потому что далее мы перенесём концентрацию [H2O] (считая её константой) из
- 77. Ранее при рассмотрении темы гидролиза (см. лекцию) мы получили, что Кг = Kw/Ka1 , где Kw
- 78. Задача 3 Связь между изотоническим коэффициентом i и кажущейся степенью диссоциации α. Рассчитать i в 0.02
- 79. Задача 4. Написать реакцию гидролиза соли Sr(ClO)2 и рассчитать рН раствора при растворении 14 г соли
- 80. По аналогии с соображениями, приведёнными в задаче 2, можем записать: (3) [OH‒]2 = Кг · [ClO‒]
- 81. [OH‒] = √(10‒14/3·10‒8)· 0,147 = 2.21·10‒4 ; Следовательно [H+] = 10‒14 /2.21·10‒4 = 4.52·10‒11 и наконец
- 82. Задача 5 Рассчитать молярность 10% раствора H2SO4, если его плотность d =1.18 г/мл, какой объём 0.00268
- 83. Задача 6 Какой должна быть концентрация изопропилового спирта (i-C3H7OH) в водном растворе изотоничным (имеющим такое же
- 84. Найдём i , воспользовавшись уравнением, связывающим i и α: где n - число ионов, на которые
- 85. Решение задач дома по задачнику Н.Л. Глинки Глава VI. РАСТВОРЫ №№ : 397, 398, 400, 401,
- 86. Задача 6 В двух стаканах приготовлены водные растворы 2х солей: в одном Zn(CH3COO)2, в другом ZnBr2
- 87. Нам следует учитывать только гидролиз по первой ступени, т.к. при диссоциации соли Zn(CH3COO)2 образуются ионы Zn2+,
- 88. Найдём теперь степень гидролиза соли ZnBr2 в растворе с концентрацией 0.04 н (0.02 M). Эта соль
- 89. Теперь Получим в результате h = 0,018, т.е. h = 1.8% Задача 7. Рассчитать pOH водного
- 90. Гидролизу подвергается ион H2BO3‒ по реакции: H2BO3‒ + HOH ⇄ H3BO3 + OH‒ По аналогии с
- 91. Задача № 8 Какой водный раствор быстрей замёрзнет 0.1 m1 раствор глюкозы или 0.024 m2 раствор
- 92. Задача № 8 Какой водный раствор быстрей закипит 0.3 m1 раствор сахарозы или 0.08 m2 раствор
- 93. Задача (Глинка) В каком объёме 1М раствора и в каком объёме 1н раствора содержится 114 г
- 94. Задача № 402 (Глинка) К 500 мл 32% - ной (по массе ) HNO3 (ρ =
- 95. Для нейтрализации 20 мл 0.1н раствора кислоты потребовалось 8 мл раствора NaOH. Сколько граммов NaOH содержит
- 97. Скачать презентацию
















































![Отсюда следует, что в чистой воде при 298 К [Н+] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/614486/slide-54.jpg)
![Также очевидно, что поскольку всегда [H]·[OH]=10–14, то рН + рОН =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/614486/slide-55.jpg)






















![[OH‒] = √(10‒14/3·10‒8)· 0,147 = 2.21·10‒4 ; Следовательно [H+] = 10‒14](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/614486/slide-80.jpg)














 Йод. Положение в периодической системе
Йод. Положение в периодической системе Композиты. Полимерные композиционные материалы
Композиты. Полимерные композиционные материалы Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс Термодинамические возможности получения меди с применением программного комплекса АСТРА-4
Термодинамические возможности получения меди с применением программного комплекса АСТРА-4 Презентация по Химии "мінеральні добрива." - скачать смотреть бесплатно_
Презентация по Химии "мінеральні добрива." - скачать смотреть бесплатно_ Етанол (етиловий спирт, винний спирт)
Етанол (етиловий спирт, винний спирт) Органічні сполуки в побуті Виконав Учень 11-Т класу ЗОШ №1 Новак Сергій
Органічні сполуки в побуті Виконав Учень 11-Т класу ЗОШ №1 Новак Сергій  Производство серной кислоты
Производство серной кислоты Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН
Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН Radiation dosimetry
Radiation dosimetry Строение атома
Строение атома Общенаучные методы исследований
Общенаучные методы исследований Закономерности адсорбции ионов и адагуляции коллоидных частиц. Самосборка на поверхности. (Лекция 9)
Закономерности адсорбции ионов и адагуляции коллоидных частиц. Самосборка на поверхности. (Лекция 9) Строение атома. Движение электрона в атоме
Строение атома. Движение электрона в атоме КИСЛОРОД
КИСЛОРОД  Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Робота учениці 11 – А класу Каплун Ірини
Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Робота учениці 11 – А класу Каплун Ірини  Кислотность и основность рганических соединений. Инфракрасная спектроскопия
Кислотность и основность рганических соединений. Инфракрасная спектроскопия Изомерия. Типы изомерии
Изомерия. Типы изомерии Презентация по Химии "Органическая химия" - скачать смотреть бесплатно
Презентация по Химии "Органическая химия" - скачать смотреть бесплатно Алкины. Способы получения
Алкины. Способы получения Уголь. Виды угля
Уголь. Виды угля Щелочные металлы
Щелочные металлы Обмен липидов
Обмен липидов Композиционные материалы – материалы будущего
Композиционные материалы – материалы будущего Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Alkanes. A “family” of hydrocarbons
Alkanes. A “family” of hydrocarbons Презентация тест по химии
Презентация тест по химии Презентация по Химии "Медь." - скачать смотреть бесплатно
Презентация по Химии "Медь." - скачать смотреть бесплатно