Содержание
- 2. Строение и свойства ферментов. По своей химической природе ферменты (энзимы) являются простыми или сложными белками. В
- 3. Особенности структурной организации ферментов. Ферментам присущи все особенности структурной организации белков. Они имеют четыре уровня организации
- 4. Кроме активного центра у ферментов (Е) имеется регуляторный центр, через который обеспечивается регуляция активного центра посредством
- 5. Четвертичная структура фермента Большинство ферментов, имея четыре уровня структурной организации, состоят из нескольких субъединиц (протомеров). Вследствие
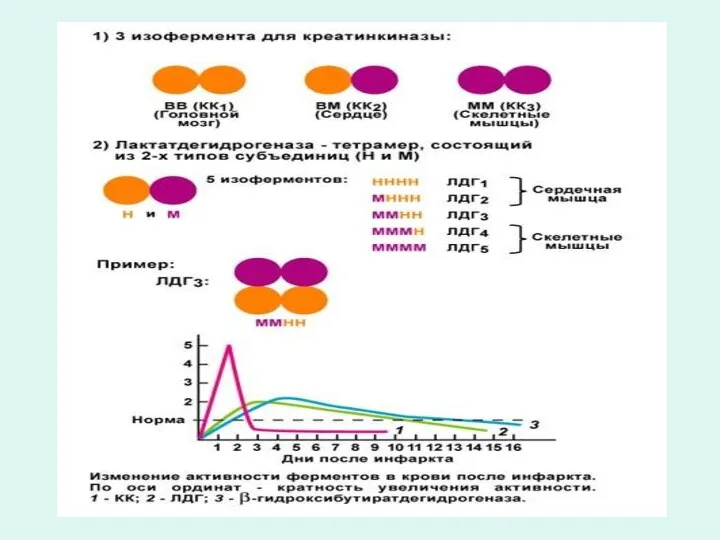
- 6. Каждый орган имеет характерный для него набор ферментов, которые при развитии в этом органе патологического процесса
- 8. Кофакторы ферментов Кофакторы у ферментов бывают двух типов: - ионы металлов - коферменты Металлы, как кофакторы
- 9. Типы коферментов В отличие от ионов металлов, коферменты являются сложными органическими соединениями и по своей химической
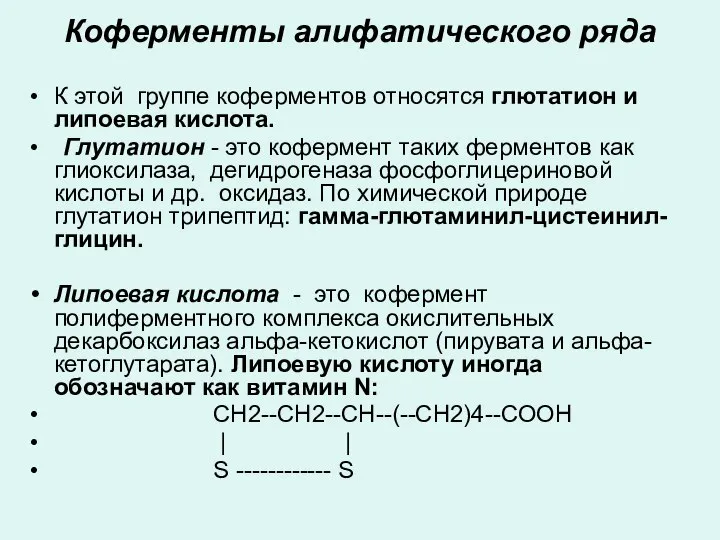
- 10. Коферменты алифатического ряда К этой группе коферментов относятся глютатион и липоевая кислота. Глутатион - это кофермент
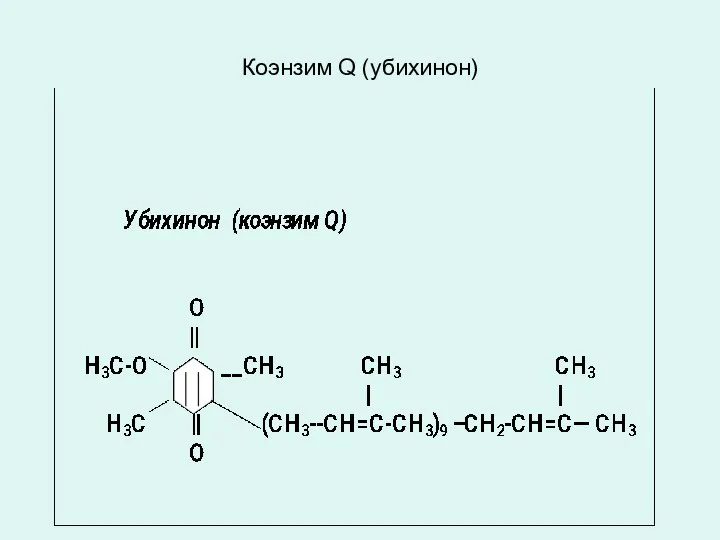
- 11. Коэнзим Q (убихинон)
- 12. КОЭНЗИМ Q10 (УБИХИНОН) от лат. ubiquitous - повсеместный). Коэнзим Q10 (убихинон) по строению и окислительно-восстановительным свойствам
- 13. Биологические эффекты убихинона ( коэнзима Q10) Коэнзим Q10 участвует в трансмембранном переносе электронов от водорода окисляемого
- 14. Коэнзим Q10 усиливает фагоцитарную активность макрофагов, повышает число гранулоцитов в костном мозге и плазме крови, увеличивает
- 15. . Коэнзим Q10 полезен для лечения последствий радиоактивного поражения. Коэнзим Q10 уменьшать токсичность лекарств и поэтому
- 16. Коферменты гетероциклического ряда К коферментам гетроциклического ряда относятся производные водорастворимых витаминов: витамина В1 - тиаминпирофосфат (ТПФ),
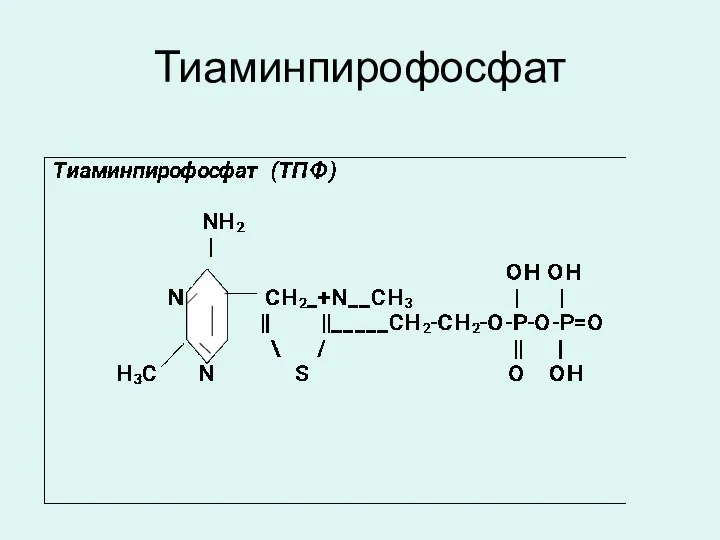
- 17. Тиаминпирофосфат
- 18. Тиаминпирофосфат Тиаминпирофосфат (ТПФ) является коферментом окислительных декарбоксилаз альфа-кетокислот (пирувата, альфа-кетоглутарата) и транскетолаз. ТПФ непосредственно или косвенно
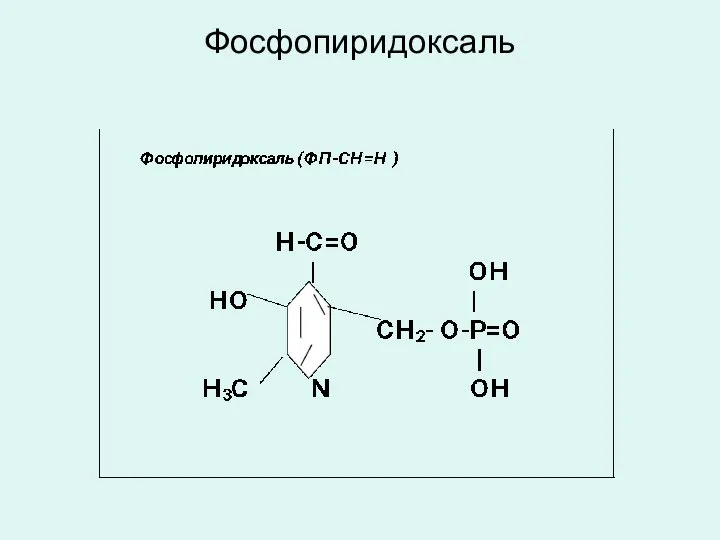
- 19. Фосфопиридоксаль
- 20. Фосфопиридоксаль Фосфопиридоксаль (ФП-СН=О) является коферментом трансаминаз, декарбоксилаз и изомераз аминокислот. Входит в состав моноаминоксидаз и диаминоксидаз
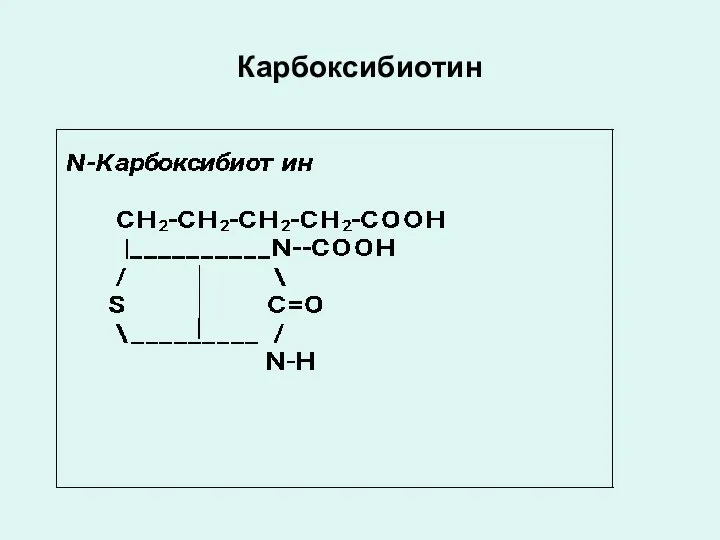
- 21. Карбоксибиотин
- 22. Карбоксибиотин Коферментной формой биотина (витамина Н) является N-карбоксибиотин, который входит в состав ферментов обеспечивающих реакции карбоксилирования:
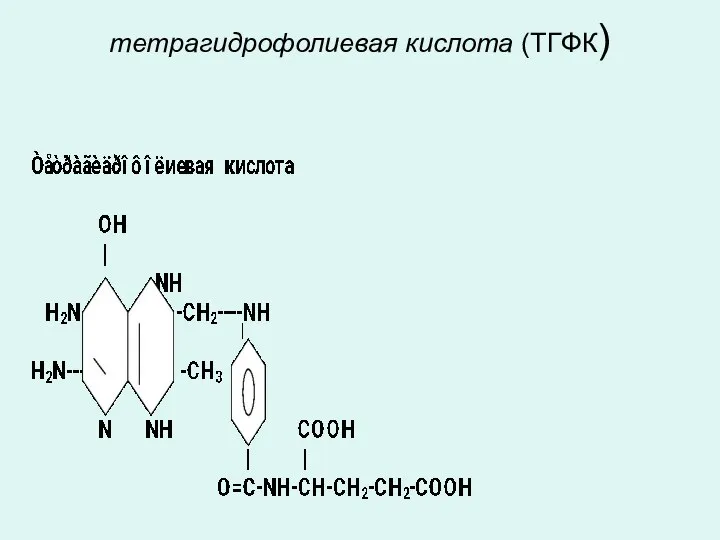
- 23. тетрагидрофолиевая кислота (ТГФК)
- 24. тетрагидрофолиевая кислота (ТГФК) 5,6,7,8- тетрагидрофолиевая кислота (ТГФК) является коферментом ферментов обеспечивающих перенос одноуглеродистых радикалов необходимых для
- 25. Коферменты нуклеотиды Коферменты нуклеотиды можно рассматривать как производные водорастворимых витаминов: витамина РР (В5) - никотинамидадениндинуклеотид (НАД)
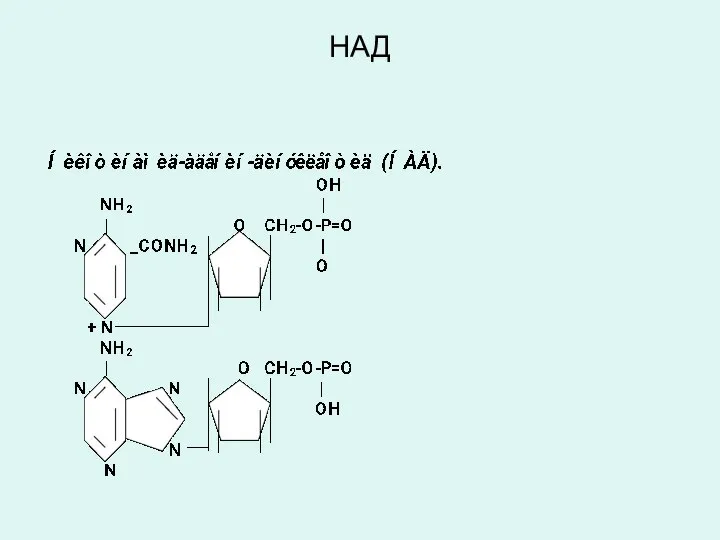
- 26. НАД
- 27. Никотинамид адениндинуклеотид (НАД) и никотинамид адениндинуклеотид фосфат (НАДФ) являются производными витамина РР (В5, никотинамид) и служат
- 28. НАДФ
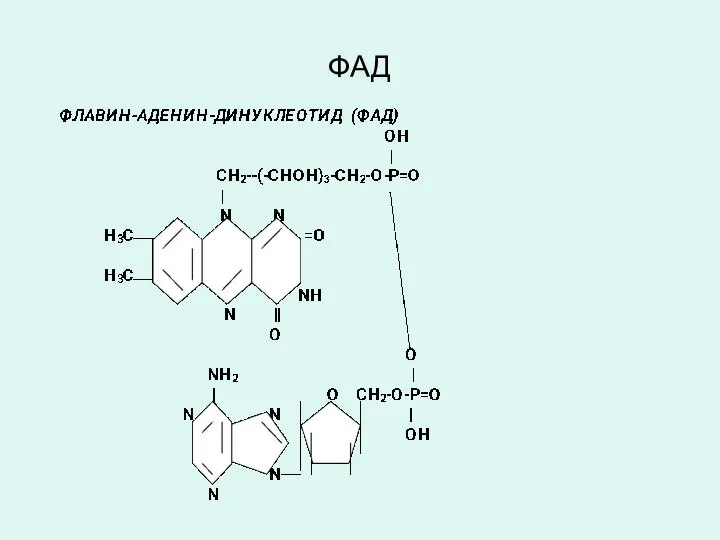
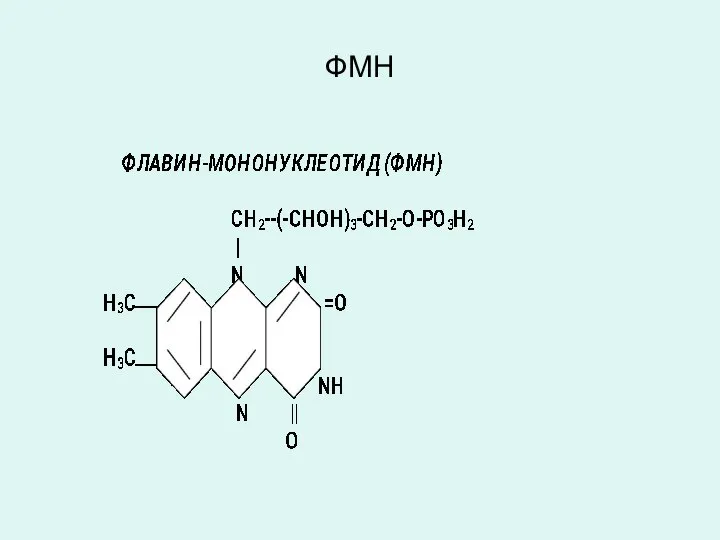
- 29. ФЛАВИН-АДЕНИН-ДИНУКЛЕОТИД (ФАД) ФЛАВИН-МОНОНУКЛЕОТИД (ФМН) Коферменты ФАД и ФМН являются производными витамина В2 (рибофлавин), являются коферментами аэробных
- 30. ФАД
- 31. ФМН
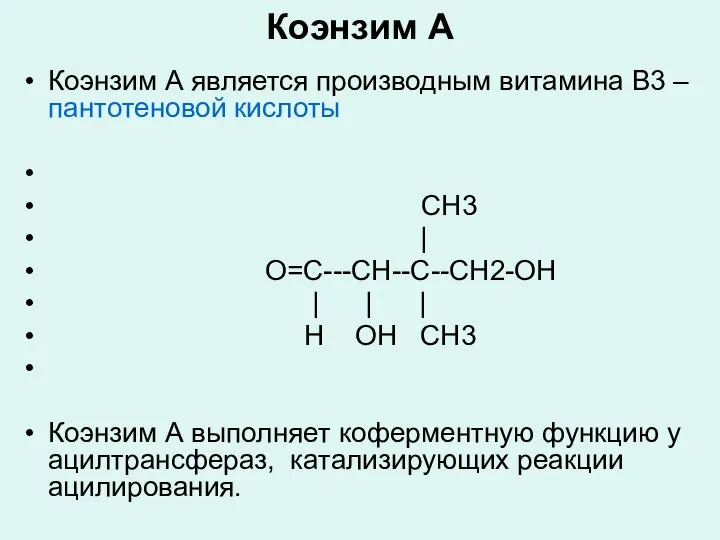
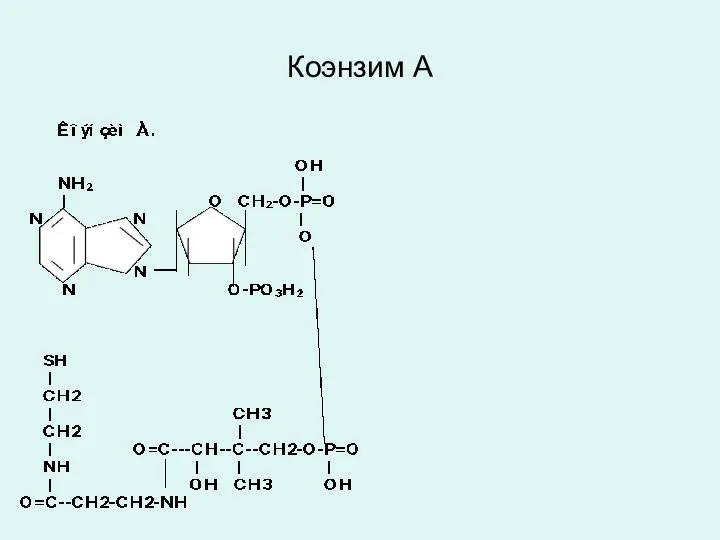
- 32. Коэнзим А Коэнзим А является производным витамина В3 – пантотеновой кислоты CH3 | O=C---CH--C--CH2-OH | |
- 33. Коэнзим А
- 34. Не содержащие витамины нуклеотидные коферменты. Коферменты этого типа можно поделить на пять групп в зависимости от
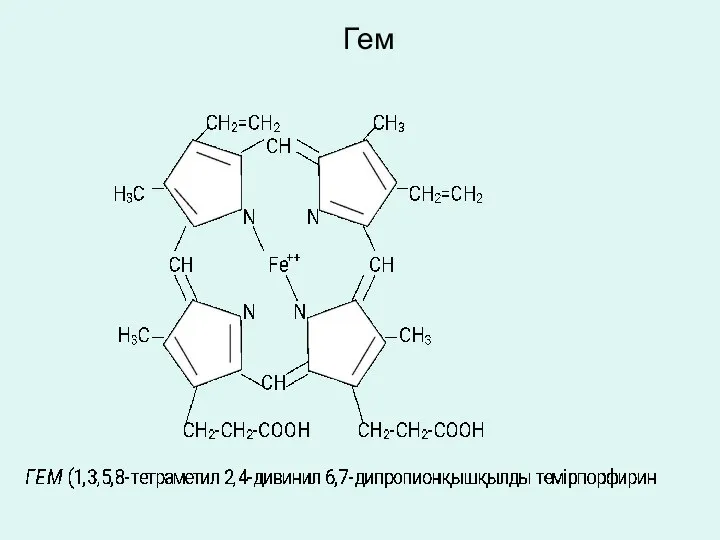
- 35. Металлокоферменты К этой группе коферментов относятся железопорфириновые и колбамидные коферменты. Железопорфириновые гемсодержащие коферменты. Коферменты цитохромов, цитохромоксидазы,
- 36. Гем
- 37. Классификация ферментов Согласно международной классификации ферменты делятся на шесть классов по типу катализируемой реакции: 1. Оксидоредуктазы
- 38. 1 класс - Оксидоредуктазы. Ферменты этого класса катализируют окислительно-восстановительные реакции, лежащие в основе процессов биологического окисления,
- 39. 2 класс - Трансферазы. Ферменты этого класса катализируют перенос функциональных групп и делятся по этому принципу
- 40. 3 класс - Гидролазы. Этот класс ферментов катализирует реакции гидролиза, и в зависимости от типа гидролизируемой
- 41. 4 класс - Лиазы. Ферменты этого класса катализируют не гидролитическое разрушение соединений с отщеплением групп (СО2,
- 42. 5 класс - Изомеразы. Эта группа ферментов катализирует реакции изомеризации, и делятся на 6 подклассов: 5.1.
- 43. 6 класс - Лигазы (синтетазы). Этот класс ферментов катализирует реакции синтеза соединений с использованием энергии АТФ
- 44. В каждом классе для структурной организации молекулы фермента используются свои группы коферментов (коэнзимов): - 1 класс
- 45. Особенности ферментативного катализа. Ферментативный катализ отличается целым рядов отличительных признаков: 1.Ферменты намного активнее чем неорганические катализаторы.
- 46. Специфичность бывает абсолютная и относительная. Абсолютная специфичность - фермент катализирует превращение только одного субстрата. Например, уреаза
- 47. Некоторые ферменты проявляют абсолютную групповую специфичность, катализируя превращение сходной группы субстратов. Например, алкогольдегидрогеназа катализирует превращение не
- 48. Скорость ферментативного катализа зависит от температуры Влияние температуры: Влияние температуры на скорость ферментативной реакции может быть
- 49. Влияние рН-среды: При постоянной температуре любой фермент проявляет наибольшую активность в определённом диапазоне рН среды. Оптимальным
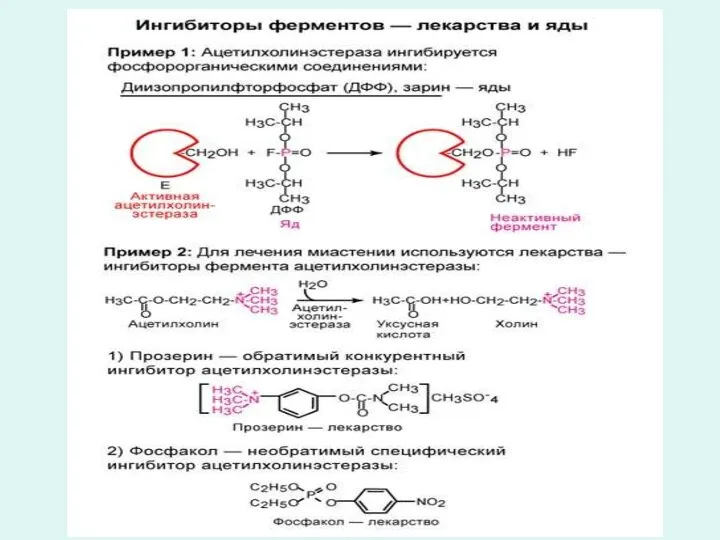
- 50. Влияние активаторов и ингибиторов Вещества, повышающие активность ферментов и, следовательно, скорость ферментативной реакции называются активаторами. Ионы
- 52. Различают обратимое и необратимое ингибирование ферментов. Обратимое ингибирование бывает двух видов: конкурентное и неконкурентное обратимое ингибирование.
- 53. Конкурентное обратимое ингибирование. Примером конкурентного обратимого ингибирования может служить ингибирование сукцинатдегидрогеназы малоновой или щавелевоуксусной кислотой, соединениями
- 54. Неконкурентное обратимое ингибирование Некоторые ингибиторы образуют комплекс не со свободным ферментом, а с фермент субстратным комплексом:
- 55. Необратимое ингибирование Необратимое ингибирование вызывается малыми концентрациями ионов тяжелых металлов, например ионов ртути, серебра и мышьяка
- 56. Влияние концентрация субстрата
- 57. Влияние концентрации фермента
- 58. Регуляция активности ферментов. Метаболические процессы, протекающие в клетке находятся в постоянном равновесии, одновременны, подчинены и определяют
- 59. Единицы измерения активности ферментов За международную единицу активности фермента принимается такое его количество, которое катализирует превращение
- 60. Номенклатура ферментов. В 1961 году специальной комиссией Международного биохимического союза была предложена систематическая номенклатура ферментов. Каждый
- 61. Современные подходы к диагностике заболеваний При любых заболеваниях всегда имеет место нарушения различных звеньев обмена веществ,
- 62. 1.Ферменты углеводного обмена Дихотомическимй путь катаболизма глюкозы: гексокиназа (фосфоглюкокиназа) фосфорилаза фосфоглюкоизомераза фосфофруктокиназа альдолаза фосфотриозоизомераза глицеральдегид-дегидрогеназа фосфоглицераткиназа
- 63. Ферменты общих путей катаболизма окислительная декарбоксилаза пирувата цитратсинтетаза аконитаза изоцитратдегидрогеназа α-кетоглутарат дегидрогеназа сукцинаттиокиназа сукцинатдегирогеназа фумараза малатдегидрогеназа
- 64. Метаболизм гликогена Синтез гликогене и глюконеогенез: УДФ-глюкозилпирофосфорилаза гликогенсинтетаза (гликозилтрансфераза) амило-гликозилтрансфераза пируваткарбоксилаза Фосфоенолпируваткарбоксикиназа Мобилизация гликогена : аденилатциклаза
- 65. Превращения олигосахаридов и гликозамингликанов мальтаза лактаза сахараза амилаза глюкуронидаза альдозоредуктаза сорбитдегирогеназа УДФ-глюкозилтрансфераза УДФ-глюкуронилтрансфераза
- 66. Ферменты дыхательной цепи митохондрий Биоэнергетика клетки окислительная декарбоксилаза пирувата изоцитратдегидрогеназа α-кетоглутарат дегидрогеназа сукцинаттиокиназа сукцинатдегирогеназа малатдегидрогеназа НАДН-дегидрогеназа
- 67. Катаболизм триациглицеридов и жирных кислот триацилглицеридлипаза липопротеидлипаза диглицеридлипаза моноглицеридлипаза липопротеинлипаза глицераткиназа α-глицерофосфатдегидрогеназа ацил КоА-синтетаза трансацетилаза карнитин-ацилтрансфераза
- 68. Анаболизм липидов и биосинтез кетоновых тел и холестерина Анаболизм липидов ацетил КоА-карбоксилаза малонитрансацетилаза цитратлиаза β-кетоацил-синтетаза β-кетоацил-редуктаза
- 69. Катаболизм белков и аминокислот пептидазы пищеварительных соков (пепсин, трипсин, химотрипсин) тканевые катепсины трансаминазы глутаматдегидрогеназа АМФ-аминогидролаза гистидаза
- 70. Обезвреживание аммиака и синтез мочевины глутаминсинтетаза глутаминаза карбомоилфосфат-синтетаза карбомоилтрансфераз аргининосукцинасинтетаза аргининосукциназа аргиназа
- 71. Ферменты обмен нуклеотидов и нуклеиновых кислот нуклеазы (ДНК-аза, РНК-аза) 5`-нуклеотидаза нуклеозидазы АМФ дезаминаза аденозиндезаминаза гуаниндезаминаза цитозиндезаминаза
- 73. Скачать презентацию
























































 Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс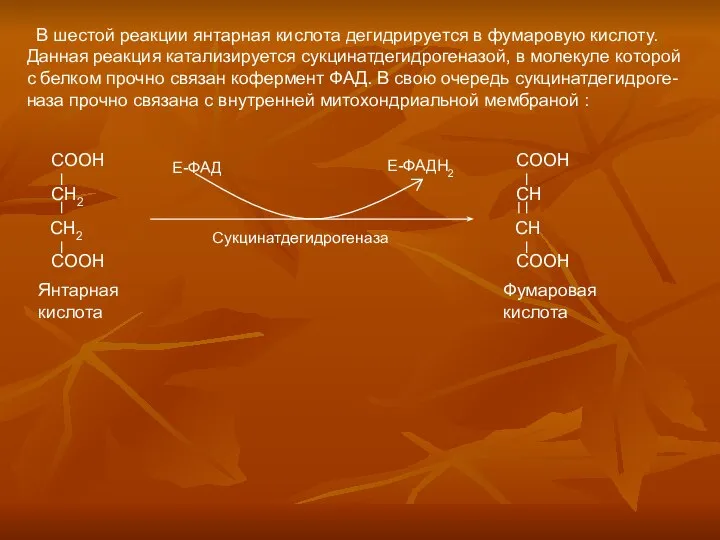 Аэробное окисление углеводов. (Часть 2)
Аэробное окисление углеводов. (Часть 2) Оксиды азота
Оксиды азота Классификация кислот
Классификация кислот Қатты күйдегі препараттар
Қатты күйдегі препараттар Полиамиды. Классификация по методу получения
Полиамиды. Классификация по методу получения Химический элемент платина
Химический элемент платина Щелочные металлы
Щелочные металлы Растворы (дисперсные системы)
Растворы (дисперсные системы) Тақырыпқа байланысты білімді жүйелеу
Тақырыпқа байланысты білімді жүйелеу II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Генетичний зв'язок
Генетичний зв'язок Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно
Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно Органічні розчинники. Їх застосування
Органічні розчинники. Їх застосування Получение этилена и опыты с ним. (Практическая работа 2)
Получение этилена и опыты с ним. (Практическая работа 2) Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно Основы химической термодинамики
Основы химической термодинамики Определение свободной поверхностной энергии тонких пленок оксидов
Определение свободной поверхностной энергии тонких пленок оксидов Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение Азотная кислота
Азотная кислота Жоғары температурағы асқын өткізгіштер
Жоғары температурағы асқын өткізгіштер Введение в биоорганическую химию. Пространственное и электронное строение органических соединений
Введение в биоорганическую химию. Пространственное и электронное строение органических соединений Исследовательская работа на тему: Удивительные свойства воды
Исследовательская работа на тему: Удивительные свойства воды “Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.
“Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.  Степень окисления
Степень окисления Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Количества вещества
Количества вещества