Содержание
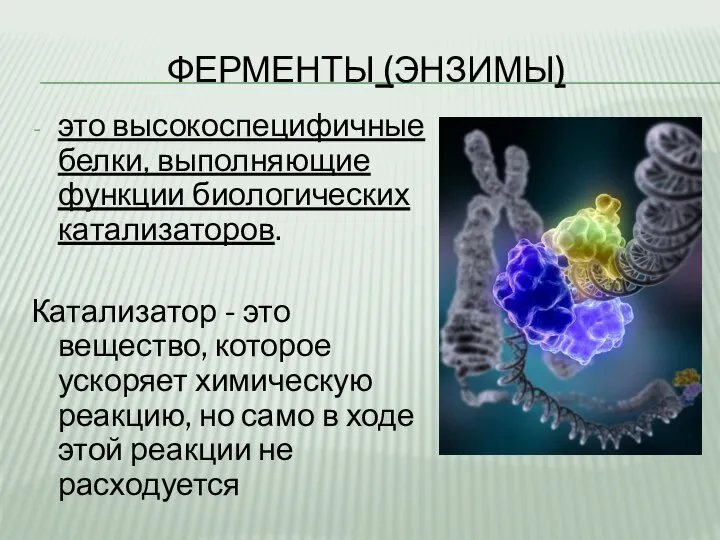
- 2. ФЕРМЕНТЫ (ЭНЗИМЫ) это высокоспецифичные белки, выполняющие функции биологических катализаторов. Катализатор - это вещество, которое ускоряет химическую
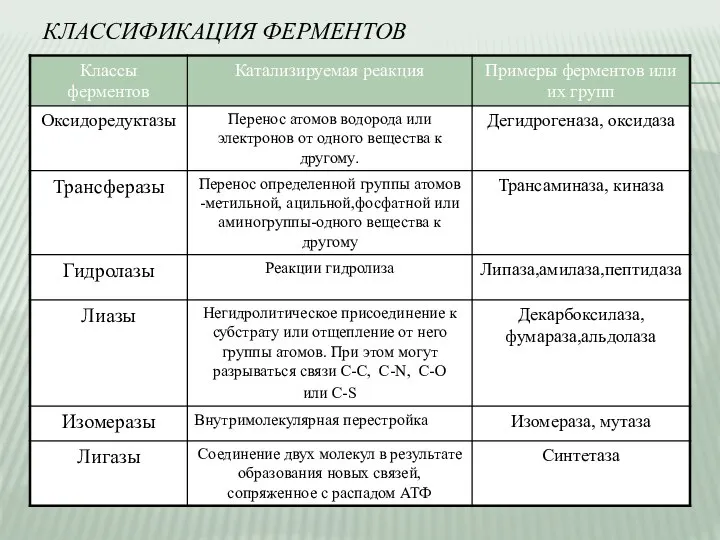
- 3. КЛАССИФИКАЦИЯ ФЕРМЕНТОВ
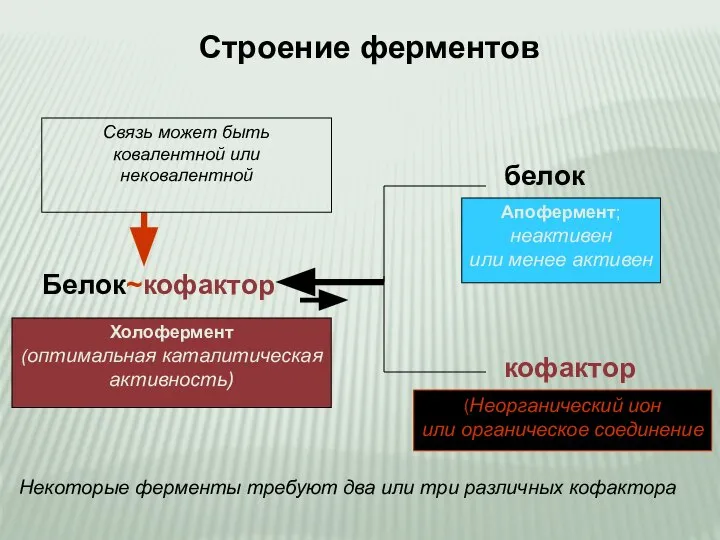
- 4. Белок~кофактор белок кофактор Связь может быть ковалентной или нековалентной Холофермент (оптимальная каталитическая активность) Апофермент; неактивен или
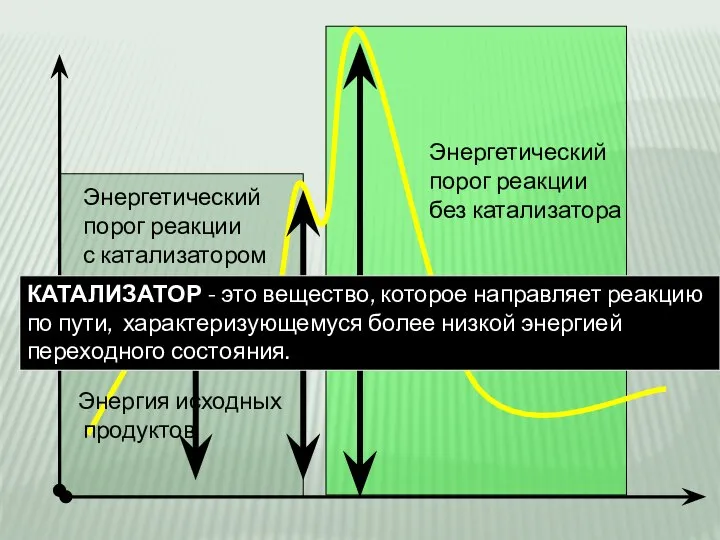
- 5. Энергия исходных продуктов Энергетический порог реакции без катализатора Энергетический порог реакции с катализатором КАТАЛИЗАТОР - это
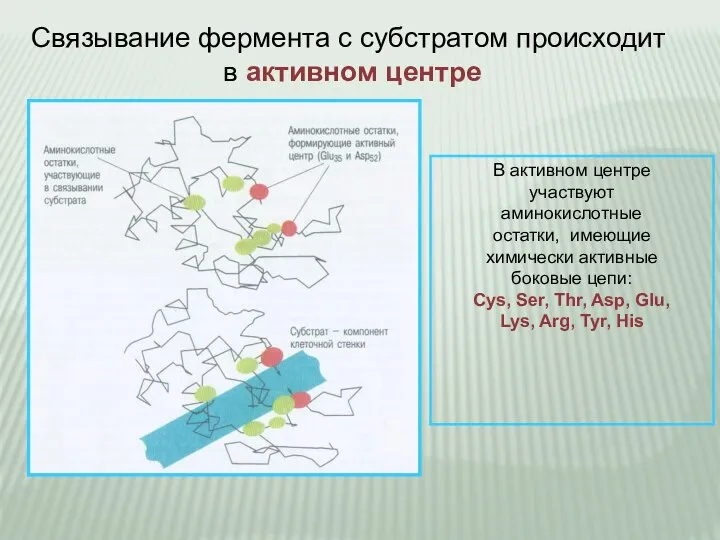
- 6. Связывание фермента с субстратом происходит в активном центре В активном центре участвуют аминокислотные остатки, имеющие химически
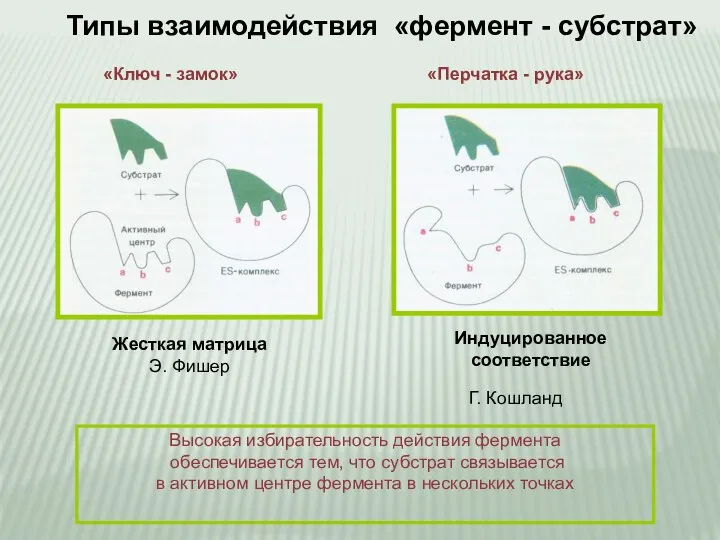
- 7. Высокая избирательность действия фермента обеспечивается тем, что субстрат связывается в активном центре фермента в нескольких точках
- 8. Способы регуляции: 1. Аллостерическая регуляция 2. Ковалентная модификация 3. Диссоциация неактивного предшественника (зимогена), на активный фермент
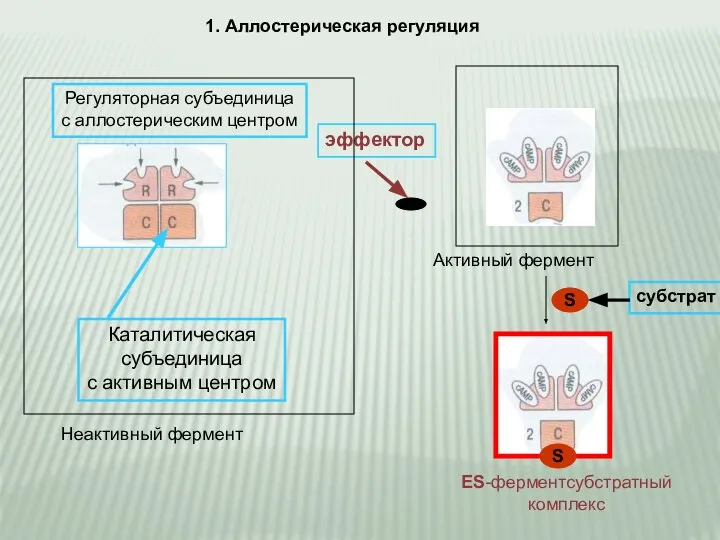
- 9. 1. Аллостерическая регуляция эффектор Каталитическая субъединица с активным центром Неактивный фермент Регуляторная субъединица с аллостерическим центром
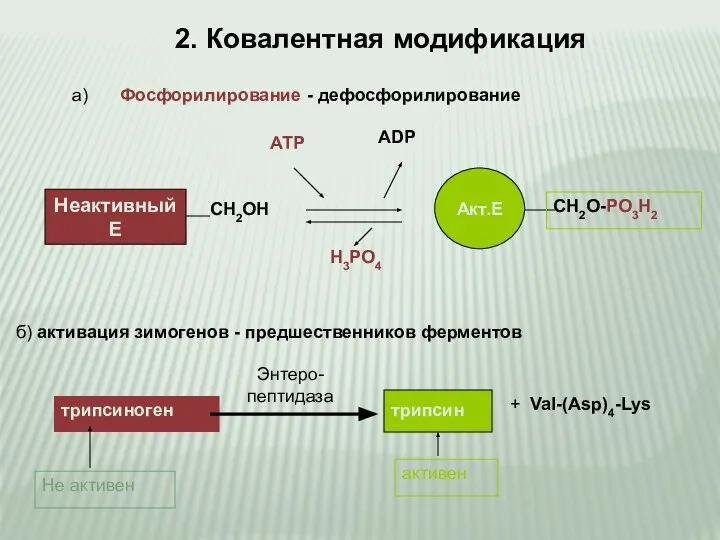
- 10. 2. Ковалентная модификация Неактивный Е СН2ОН Акт.Е СН2О-РО3Н2 АТР АDP Н3РО4 Фосфорилирование - дефосфорилирование a) б)
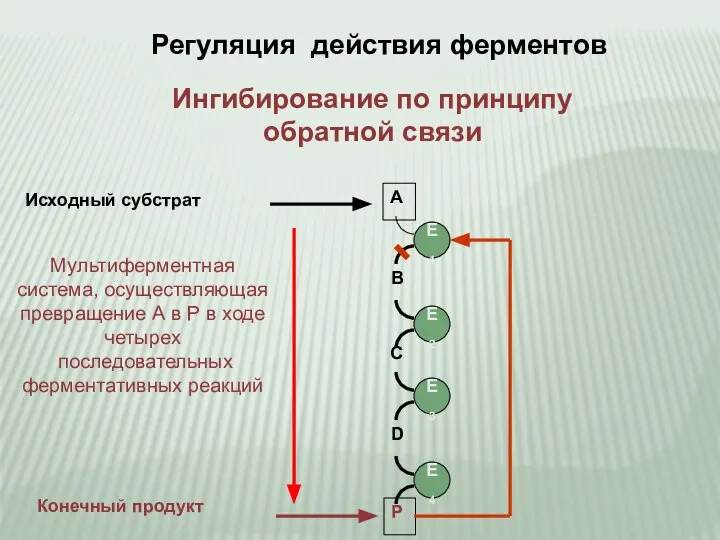
- 11. Регуляция действия ферментов E4 E3 E2 E1 A B C D P Ингибирование по принципу обратной
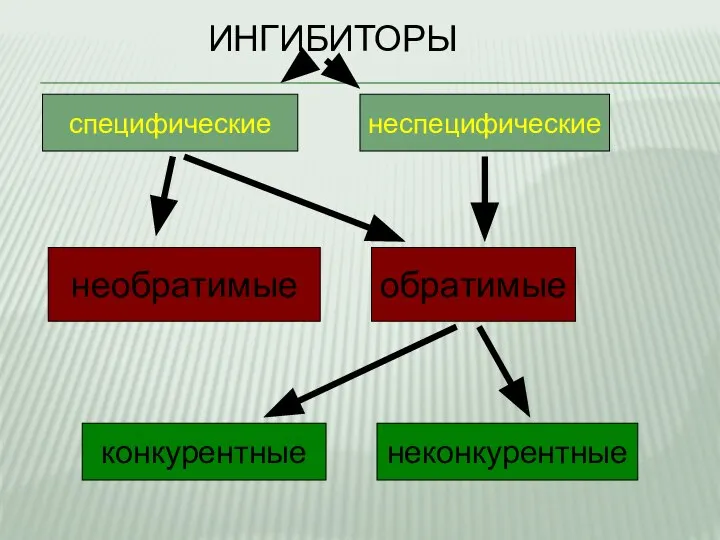
- 12. ИНГИБИТОРЫ специфические неспецифические обратимые необратимые конкурентные неконкурентные
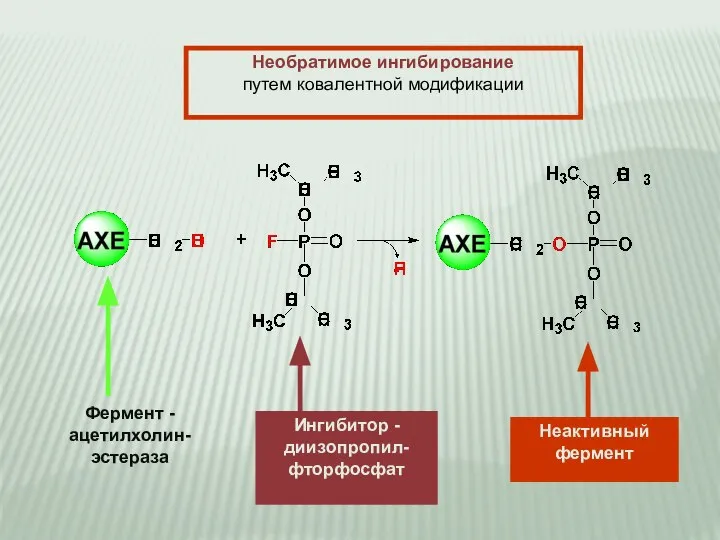
- 13. Необратимое ингибирование путем ковалентной модификации Фермент - ацетилхолин- эстераза Ингибитор - диизопропил- фторфосфат Неактивный фермент
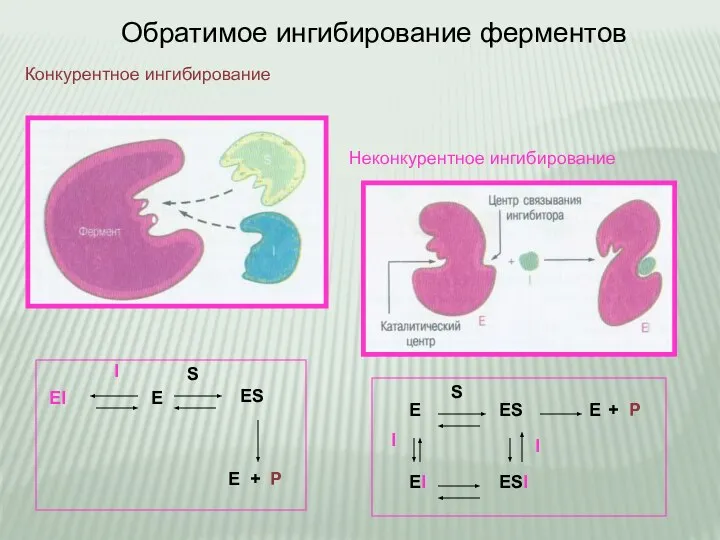
- 14. Обратимое ингибирование ферментов Конкурентное ингибирование Неконкурентное ингибирование E EI ES E + P I E ES
- 15. Иммобилизация фермента - закрепление на полимерном носителе (полистироле) Иммобилизованный фермент не смешивается с продуктами реакции, более
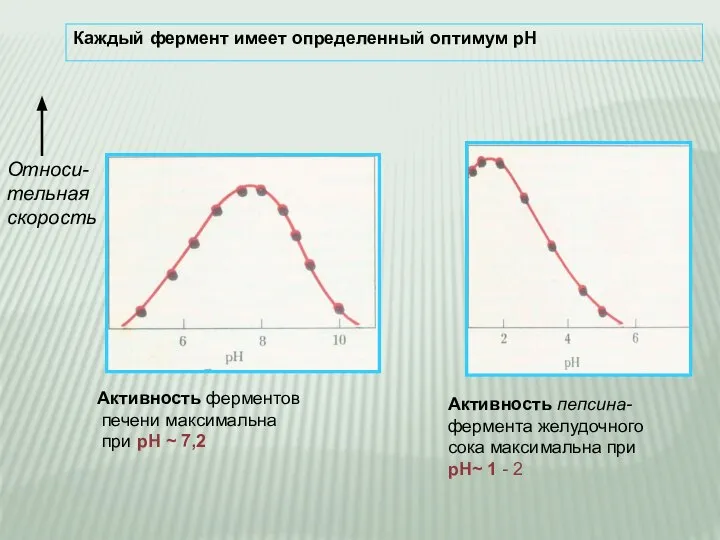
- 16. Каждый фермент имеет определенный оптимум рН Относи- тельная скорость Активность пепсина- фермента желудочного сока максимальна при
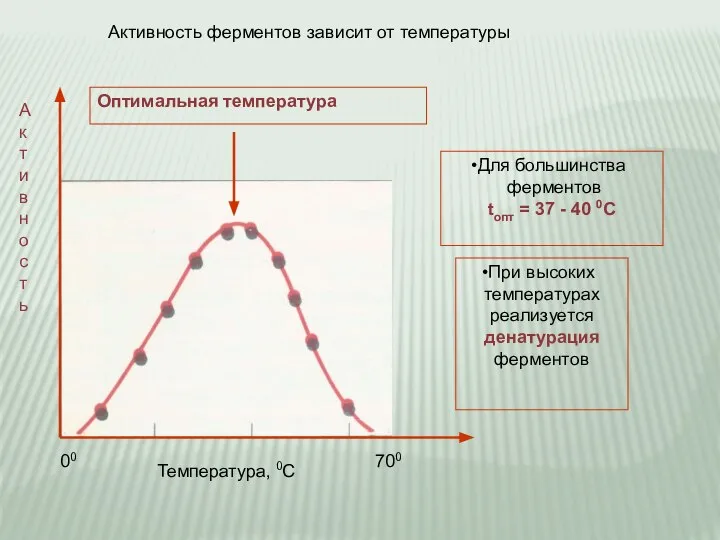
- 17. Оптимальная температура 00 700 Активность ферментов зависит от температуры А к т и в н о
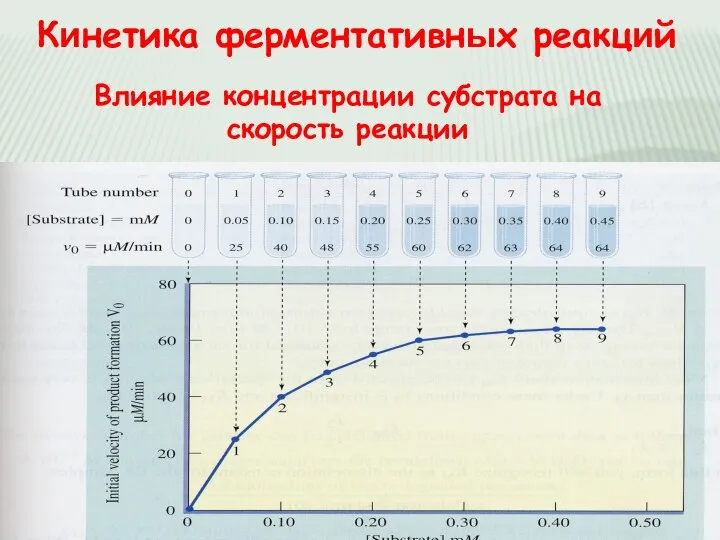
- 18. Кинетика ферментативных реакций Влияние концентрации субстрата на скорость реакции
- 19. УРАВНЕНИЕ МИХАЭЛИСА-МЕНТЕН В чем его смысл? — Позволяет получить формальные характеристики скорости ферментативной реакции вида Уравнение
- 20. Анализ уравнения Михаэлиса -Ментен 3. Km = [S], тогда V0 = 1/2 Vmax Vmax [S] Km
- 21. СМЫСЛ KM Km выводится из констант скоростей Km в условиях Михаэлиса-Ментен определяет скорость распада фермент-субстратного комплекса
- 23. Скачать презентацию



![Анализ уравнения Михаэлиса -Ментен 3. Km = [S], тогда V0 =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405743/slide-19.jpg)

 Термическая переработка газов, нефтяных фракций и остатков нефтепереработки
Термическая переработка газов, нефтяных фракций и остатков нефтепереработки Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Жирорастворимые витамины. (Лекция 12)
Жирорастворимые витамины. (Лекция 12) Презентация по Химии "Значение химии" - скачать смотреть бесплатно
Презентация по Химии "Значение химии" - скачать смотреть бесплатно Газообразное состояние вещества
Газообразное состояние вещества Радиофармацевтическая химия
Радиофармацевтическая химия Влияние нанокомпозитов платина/Нафион на электрокаталитическую активность реакции восстановления водорода и окисления кислорода
Влияние нанокомпозитов платина/Нафион на электрокаталитическую активность реакции восстановления водорода и окисления кислорода Периодический закон Д.И. Менделеева. Строение атома
Периодический закон Д.И. Менделеева. Строение атома Крем
Крем  Кристаллические решетки
Кристаллические решетки Растворы. Основные понятия. Концентрация. Законы Рауля
Растворы. Основные понятия. Концентрация. Законы Рауля Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов
Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов Nucleic acids
Nucleic acids Коррозия металла
Коррозия металла Викторина. Химический Элементариум
Викторина. Химический Элементариум Полимеры
Полимеры Химическое сопротивление алюминий и его сплавов
Химическое сопротивление алюминий и его сплавов Непредельные, ненасыщенные, ацетиленовые алкины
Непредельные, ненасыщенные, ацетиленовые алкины Химический элемент медь. (11 класс)
Химический элемент медь. (11 класс) Характеристика липидов. Углеводы. Моносахариды. Дисахариды. Полисахариды
Характеристика липидов. Углеводы. Моносахариды. Дисахариды. Полисахариды Radiation dosimetry
Radiation dosimetry Насыщенные (предельные) углеводороды. Алканы (парафины)
Насыщенные (предельные) углеводороды. Алканы (парафины)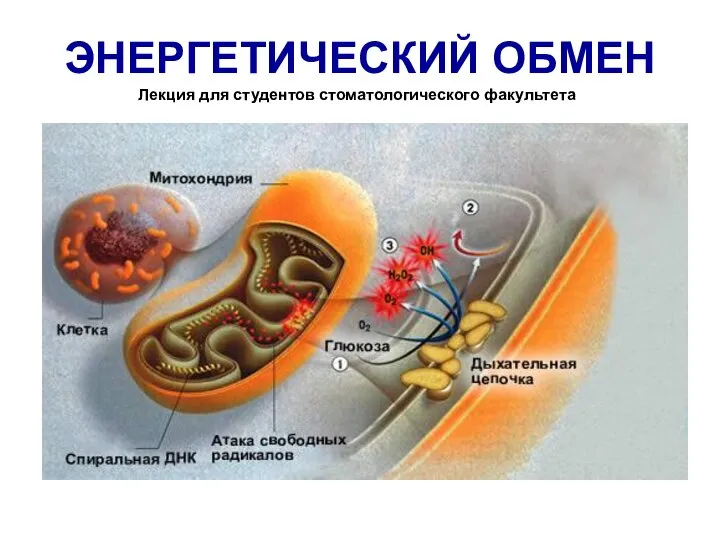 Энергетический обмен. Биологическое окисление
Энергетический обмен. Биологическое окисление Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс) Катализатор Уилкинсона
Катализатор Уилкинсона Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Презентация Щелочные металлы
Презентация Щелочные металлы  Марганец и его свойства
Марганец и его свойства