Содержание
- 2. План лекции I. Основные понятия и определения II. Структура и классификация дисперсных систем III. Мицеллярные коллоидные
- 3. Структура и классификация дисперсных систем Дисперсные системы (д.с.) - это гетерогенные системы, в которых одна из
- 4. Структура и классификация дисперсных систем Основной характеристикой д.с. и мерой раздробленности вещества является дисперсность и степень
- 5. Классификация: а) по степени дисперсности частиц дисперсной фазы
- 6. От размеров частиц дисперсной фазы зависят свойства дисперсных систем Микрогетерогенные системы задерживаются ультрафильтрами (целлофан, пергамент); гетерогенные;
- 7. б) по агрегатному состоянию дисперсной фазы и дисперсионной среды
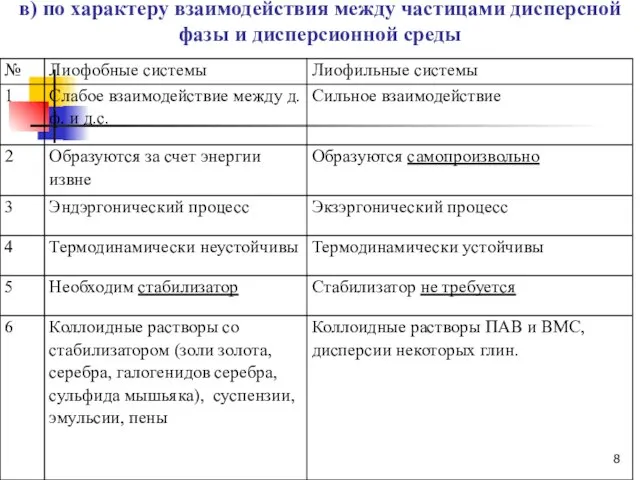
- 8. в) по характеру взаимодействия между частицами дисперсной фазы и дисперсионной среды
- 9. Мицеллярные коллоидные системы Строение мицеллы В гидрозолях дисперсионной средой является вода, а твердая дисперсная фаза распределяется
- 10. Строение мицеллы Основную часть мицеллы составляет агрегат: атомы, ионы, молекулы нерастворимого в воде вещества, имеющие кристаллическое
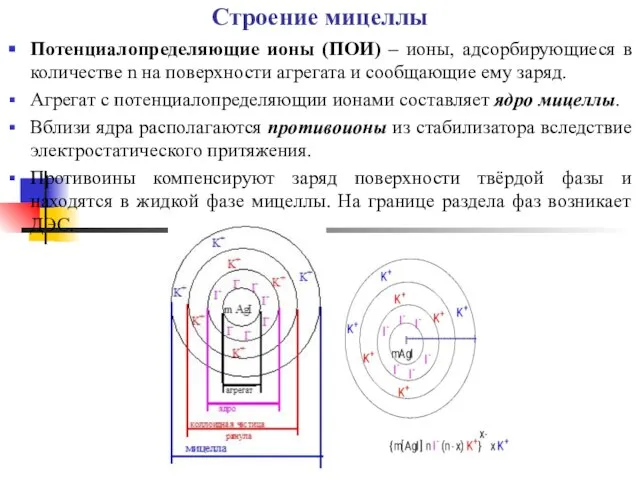
- 11. Строение мицеллы Потенциалопределяющие ионы (ПОИ) – ионы, адсорбирующиеся в количестве n на поверхности агрегата и сообщающие
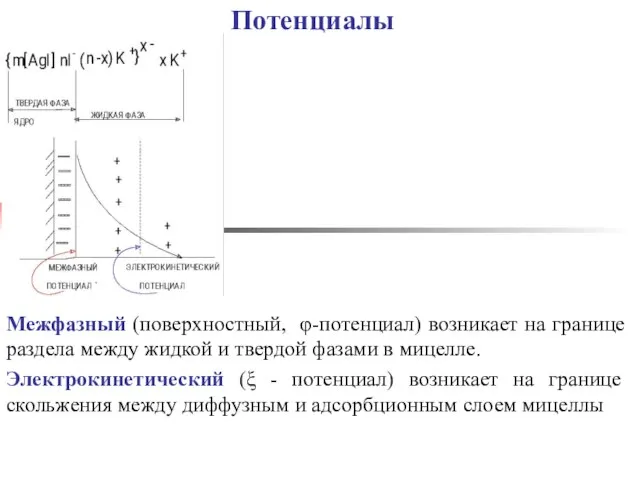
- 12. Потенциалы Межфазный (поверхностный, φ-потенциал) возникает на границе раздела между жидкой и твердой фазами в мицелле. Электрокинетический
- 13. Устойчивость коллоидных растворов Характеризует способность д.ф. сохранять состояние равномерного распределения частиц д.ф. во всем объеме дисперсионной
- 14. Устойчивость коллоидных растворов Агрегативная устойчивость коллоидных растворов обусловлена наличием на поверхности частиц «рыхлой» ионной атмосферы из
- 15. Коагуляция Коагуляция – это процесс слипания коллоидных частиц с образованием крупных агрегатов из-за потери коллоидным раствором
- 16. Коагуляция под действием электролитов Порог коагуляции – минимальное количество электролита, которое надо добавить к коллоидному раствору,
- 17. Коагуляция под действием электролитов Механизм коагуляции Роль электролита – уменьшение расклинивающего давления между сближающимися коллоидными частицами.
- 18. Коагуляция под действием электролитов Нейтрализационная коагуляция Происходит при действии электролита, который химически взаимодействует с потенциалопределяющими ионами,
- 19. Коагуляция под действием электролитов Концентрационная коагуляция Нет химического взаимодействия электролита с ионами стабилизатора. ПРИМЕР: к золю
- 20. Коагуляция под действием электролитов Изоэлектрическое состояние – состояние коллоидных частиц, при котором электрокинетический потенциал равен 0
- 21. Гетерокоагуляция. Взаимная коагуляция Гетерокоагуляция – коагуляция коллоидных растворов, содержащих разнородные частицы, отличающиеся по химической природе, знаку
- 22. Коллоидная защита Коллоидная защита – это повышение устойчивости лиофобных золей по отношению к электролитам. Достигается добавлением
- 23. Коллоидная защита Количественная характеристика защитного действия (Р. Зигмонди) – “Защитное число”. “Защитное число” – такое количество
- 24. СИСТЕМЫ С ЖИДКОЙ И ГАЗООБРАЗНОЙ ДИСПЕРСИОННОЙ СРЕДОЙ Суспензии – это дисперсные системы с твердой дисперсной фазой
- 25. Стабилизация суспензий Суспензии агрегативно и кинетически неустойчивые системы. Стабилизаторы: 1) ЭЛЕКТРОЛИТЫ. Механизм стабилизации: ионы электролита избирательно
- 26. Эмульсии Эмульсия – это дисперсная система, состоящая из двух взаимно нерастворимых жидкостей, одна из которых в
- 27. Классификация эмульсий В зависимости от природы образующих жидкостей: - Эмульсии масла в воде (М/В) или эмульсии
- 28. Эмульсии Эмульсии термодинамически неустойчивые системы. Самопроизвольное слияние капелек дисперсной фазы – коалесценция. Этот процесс приводит к
- 29. Стабилизация эмульсий Стабилизация эмульсий ионогенными коллоидными ПАВ связана с адсорбцией и определенной ориентацией молекул ПАВ на
- 30. Эмульгирующее действие ПАВ Поверхностная активность определяется соотношением между гидрофильной и гидрофобной частями молекул ПАВ. Уравновешивание гидрофильного
- 31. Инверсия b) Твердые эмульгаторы (порошки). Гидрофильные эмульгаторы, которые хорошо смачиваются водой (глина, мел, гипс), стабилизируют эмульсии
- 32. Характеристики эмульсий c) Обращение эмульсии может быть вызвано длительным механическим воздействием. d) Обращение фаз эмульсии при
- 33. СИСТЕМА С ГАЗООБРАЗНОЙ ДИСПЕРСИОННОЙ СРЕДОЙ. АЭРОЗОЛИ Аэрозоли – грубодисперсные системы, у которых дисперсная фаза – частички
- 34. АЭРОЗОЛИ 2) Методами диспергирования. Твердое или жидкое вещество измельчают механическим путем, а затем распыляют в газовой
- 35. Порошки Порошки — это свободно – дисперсные системы, у которых дисперсионная среда – газ, а дисперсная
- 36. Разрушение эмульсий и аэрозолей Химические методы: 1. добавление в эмульсии или пены минеральных кислот или солей
- 37. Список литературы Физическая химия: учебник / Ю.Я. Харитонов. – М.: ГЭОТАР - Медиа, 2013. – 608
- 39. Скачать презентацию

































 Мұнайлардың жіктелуі
Мұнайлардың жіктелуі Типы химических реакций в органической химии. Типы реакций в органике
Типы химических реакций в органической химии. Типы реакций в органике Синтез полимерных комплексонов на основе аминокислот
Синтез полимерных комплексонов на основе аминокислот Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010
Работу выполнила: Пьянкова Елена Руководитель: Баранова Алевтина Владимировна 2010 Деление ядер урана
Деление ядер урана  Физические и химические явления
Физические и химические явления Моделирование электронной структуры и сенсорных свойств наноструктурированных смешанных оксидов
Моделирование электронной структуры и сенсорных свойств наноструктурированных смешанных оксидов Отношение масс элементов в веществе. Массовые доли элементов в веществе
Отношение масс элементов в веществе. Массовые доли элементов в веществе Витамины и коферменты
Витамины и коферменты Түймедақ гүлімен құрғақ теріге арналған ылғалдандырушы крем дайындау
Түймедақ гүлімен құрғақ теріге арналған ылғалдандырушы крем дайындау Алкены
Алкены Моносахариды
Моносахариды Предмет химии. Вещества
Предмет химии. Вещества Карбоновые кислоты и их производные
Карбоновые кислоты и их производные Моделирование химико-технологической системы. Эмпирические, физические, математические методы моделирования
Моделирование химико-технологической системы. Эмпирические, физические, математические методы моделирования Метод изолирования Васильевой
Метод изолирования Васильевой Галогены
Галогены Хімія в побуті
Хімія в побуті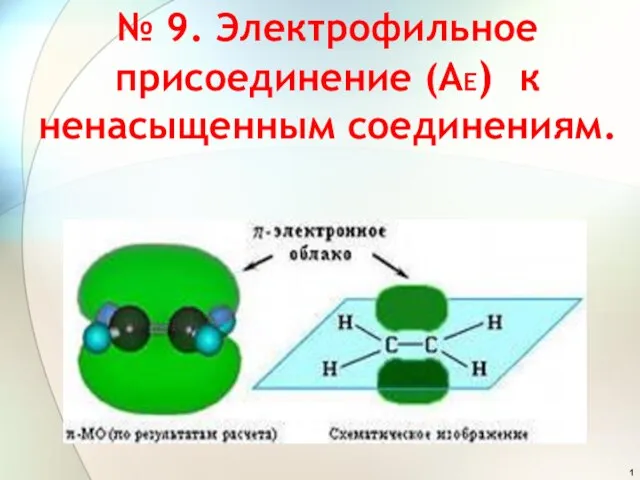 Презентация по химии Электрофильное присоединение (АЕ) к ненасыщенным соединениям.
Презентация по химии Электрофильное присоединение (АЕ) к ненасыщенным соединениям.  Электрохимические анализаторы медицинского назначения
Электрохимические анализаторы медицинского назначения Изопроцессы в идеальном газе
Изопроцессы в идеальном газе Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Получение и применение порфиринов и их аналогов
Получение и применение порфиринов и их аналогов Використання вуглеводнів
Використання вуглеводнів Дәрілік препараттардың синтезі мен олардың классификациясы
Дәрілік препараттардың синтезі мен олардың классификациясы Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Алканы: изомерия и номенклатура
Алканы: изомерия и номенклатура Презентация по Химии "Закон збереження маси" - скачать смотреть
Презентация по Химии "Закон збереження маси" - скачать смотреть