Содержание
- 2. Соединения, содержащие в своем составе различные функциональные группы, называются гетерофункциональными соединениями. Подавляющее большинство веществ, участвующих в
- 3. Химические свойства гетерофункциональных соединений сочетают в себе свойства тех функциональных групп, которые входят в молекулу. Однако
- 4. Соединения, содержащие в молекуле гидроксильные и карбоксильные группы делятся на: оксикарбоновые (содержат ОН-группу, связаны с алифатической
- 5. Гидрокси(окси) кислоты.
- 6. Гидрокси(окси) кислоты. CH3 СOOH СOOH СOOH CHOH CH2 CHOH CH2 CHOH CHOH CHOH C OH Молочная
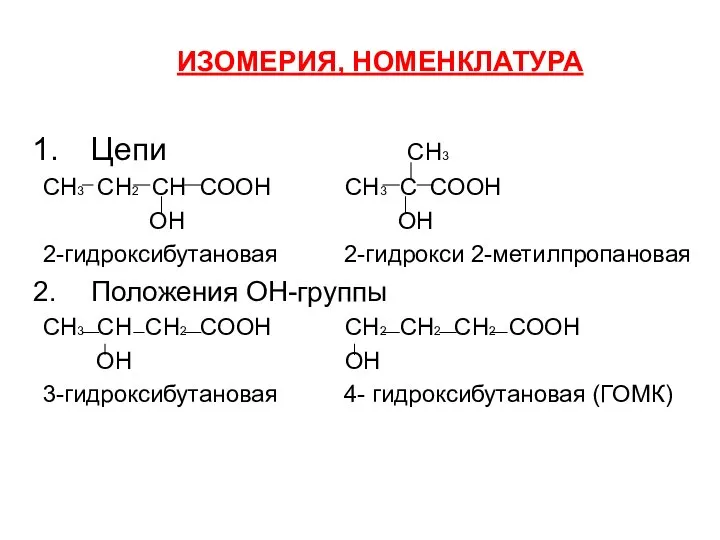
- 7. ИЗОМЕРИЯ, НОМЕНКЛАТУРА Цепи СН3 СН3 СН2 СН СООН СН3 С СООН ОН ОН 2-гидроксибутановая 2-гидрокси 2-метилпропановая
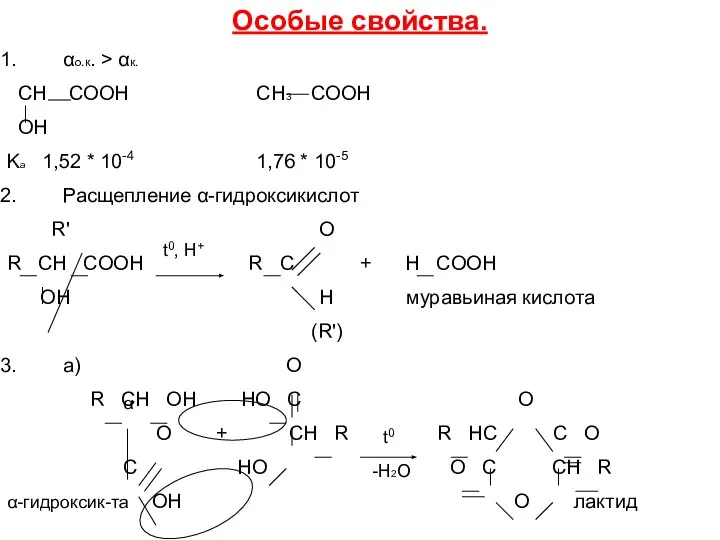
- 8. Особые свойства. αо.к. > αк. CH COOH СH3 COOH OH Ka 1,52 * 10-4 1,76 *
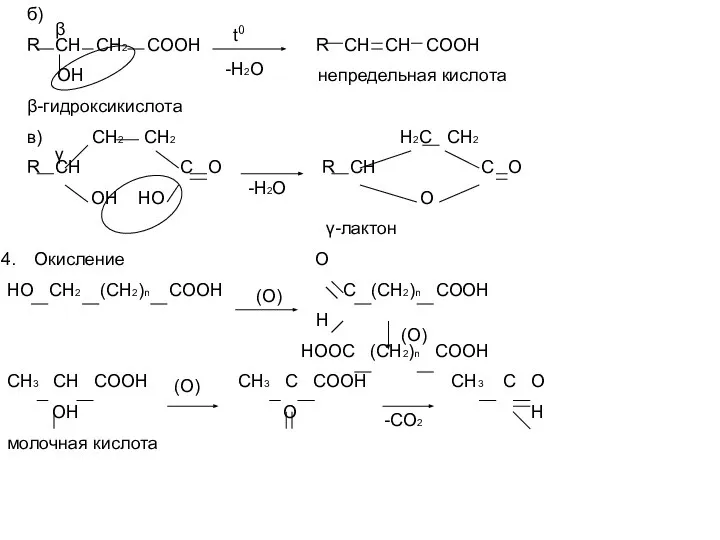
- 9. б) R CH CH2 COOH R CH CH COOH ОН непредельная кислота β-гидроксикислота в) CH2 CH2
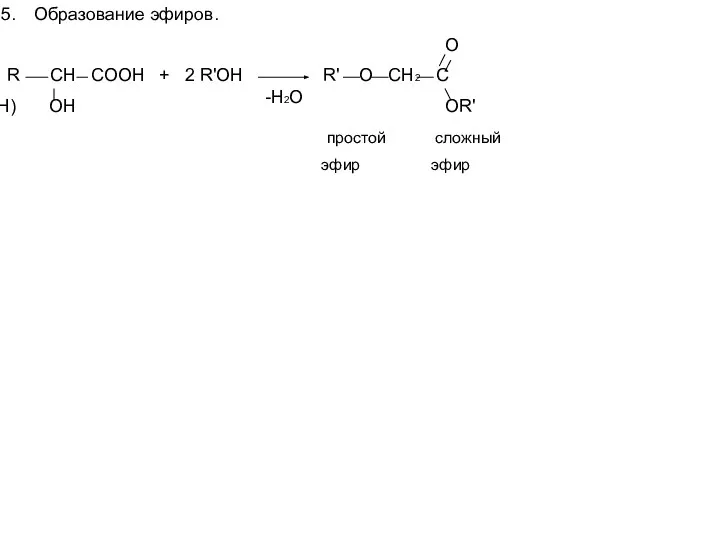
- 10. Образование эфиров. O R CH COOH + 2 R'OH R' O CH2 C OH OR' простой
- 11. ВАЖНЕЙШИЕ ПРЕДСТАВИТЕЛИ СН2 С ОН О ОН гликолевая кислота в недозрелых фруктах, свекле (гидроксиэтановая) tпл.=79ºС СН3
- 12. L (+) – мясомолочная кислота СООН СООН С О + Н+ + НАDН НО Н +
- 13. СООН НО С СН2 СООН СН2 СООН лимонная кислота Н2SO4(к) tº Н С О ОН +
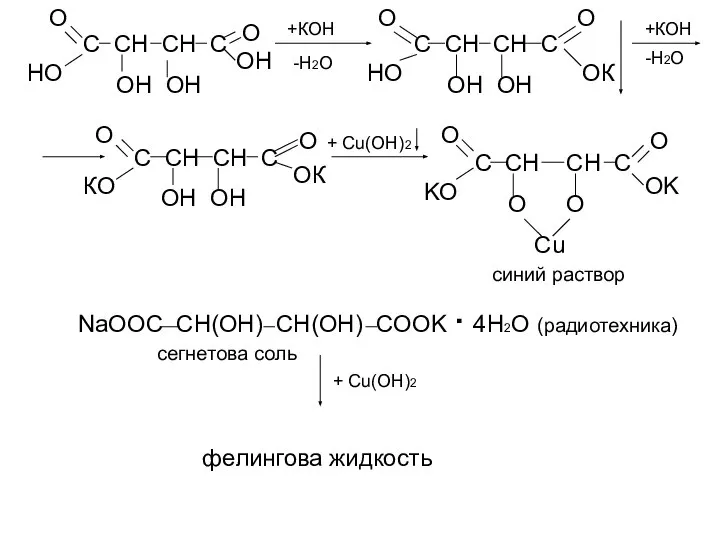
- 14. С СН СН С ОН ОН О ОН О НО +КОН -Н2О С СН СН С
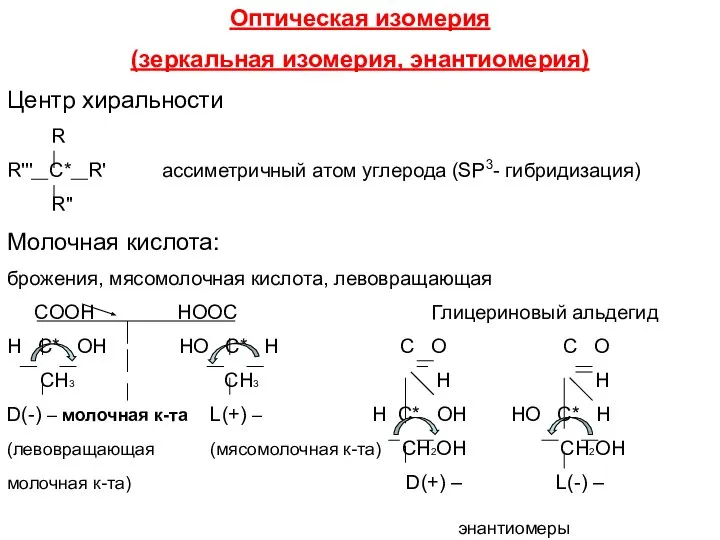
- 15. Оптическая изомерия (зеркальная изомерия, энантиомерия) Центр хиральности R R''' C* R' ассиметричный атом углерода (SP3- гибридизация)
- 16. Хиральные объекты
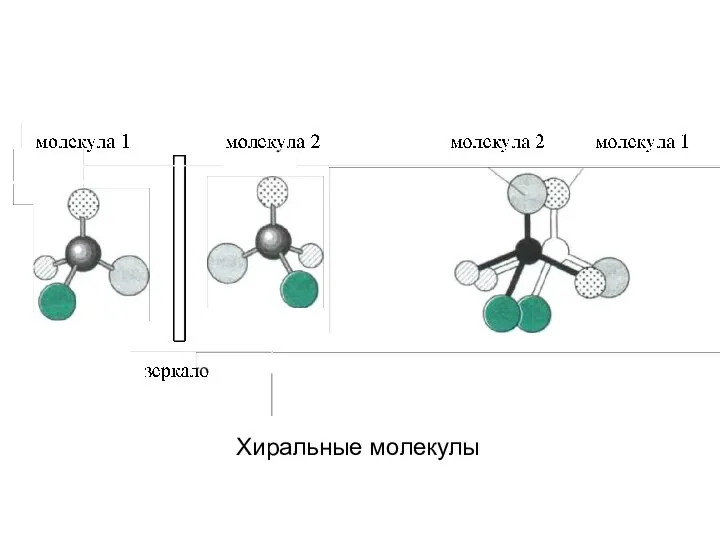
- 17. Хиральные молекулы
- 20. X=2n, n-число хиральных центров Количество стереоизомеров COOH COOH COOH COOH H C* OH НО C* H
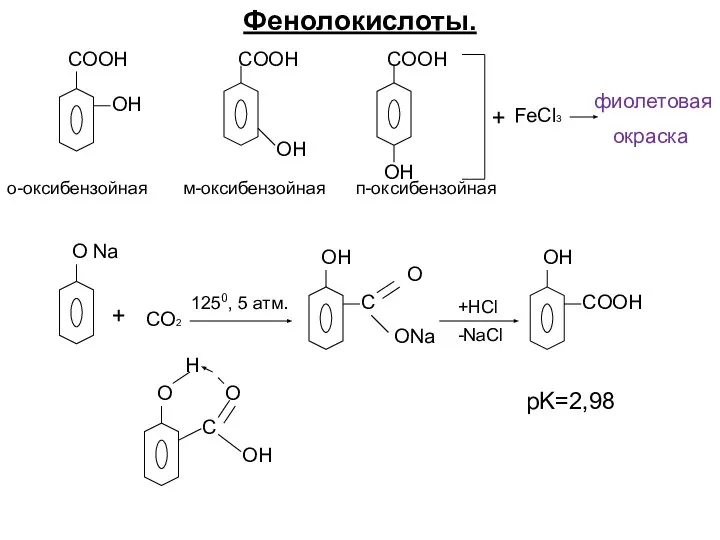
- 21. Фенолокислоты. COOH COOH COOH OH OH OH + FeCl3 фиолетовая окраска о-оксибензойная м-оксибензойная п-оксибензойная O Na
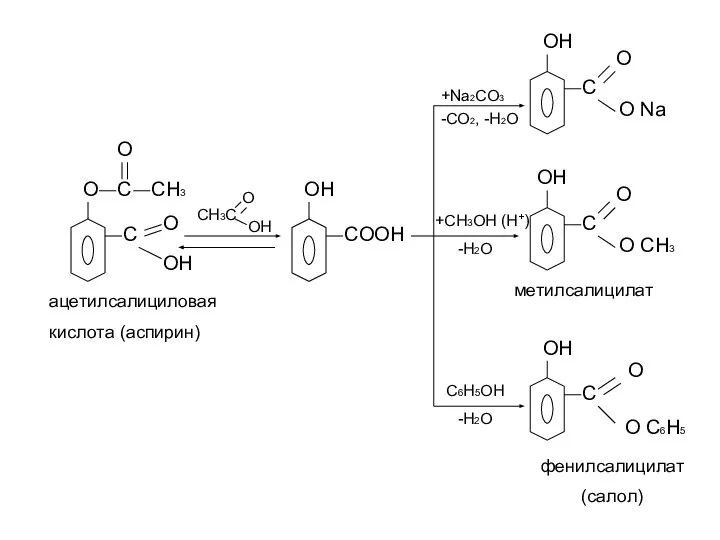
- 22. O C O CH3 C O OH CH3C O OH OH COOH ацетилсалициловая кислота (аспирин) +Na2CO3
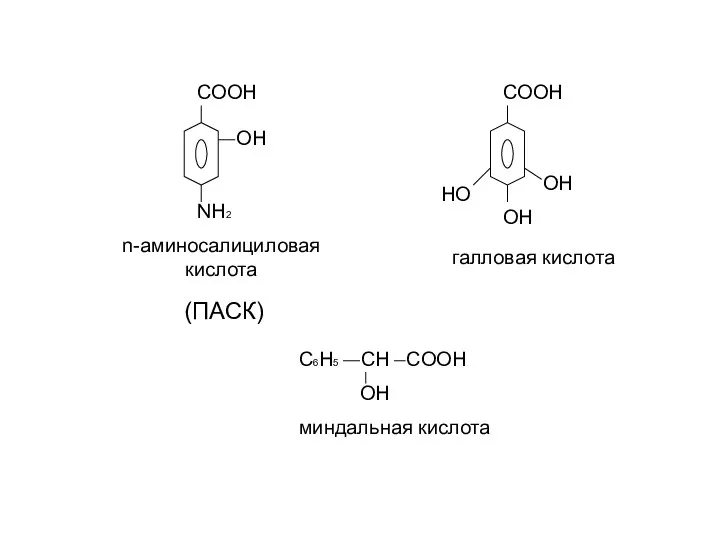
- 23. COOH COOH OH OH HO OH NH2 n-аминосалициловая кислота галловая кислота (ПАСК) С6H5 CH COOH OH
- 24. Важнейшие природные оксокислоты
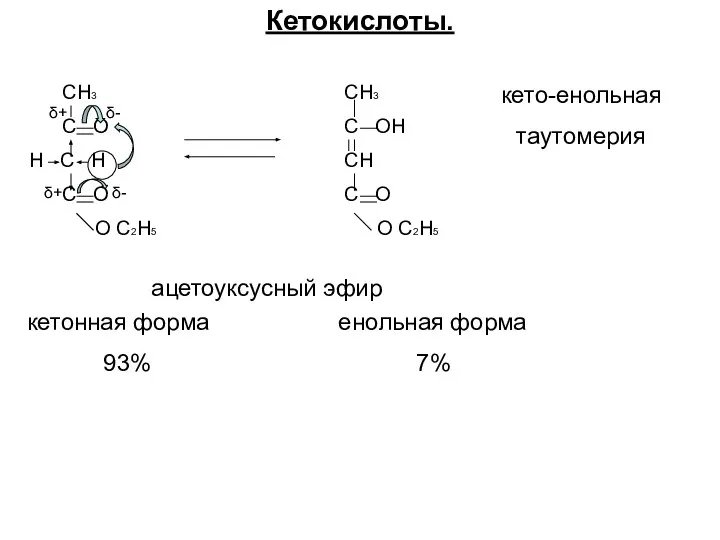
- 25. Кетокислоты. СH3 C O H C H C O O C2H5 δ+ δ+ δ- δ- CH3
- 27. Скачать презентацию












 Термодинамическое равновесие
Термодинамическое равновесие Оксид металлов
Оксид металлов Легированные конструкционные стали. Инструментальные легированные стали
Легированные конструкционные стали. Инструментальные легированные стали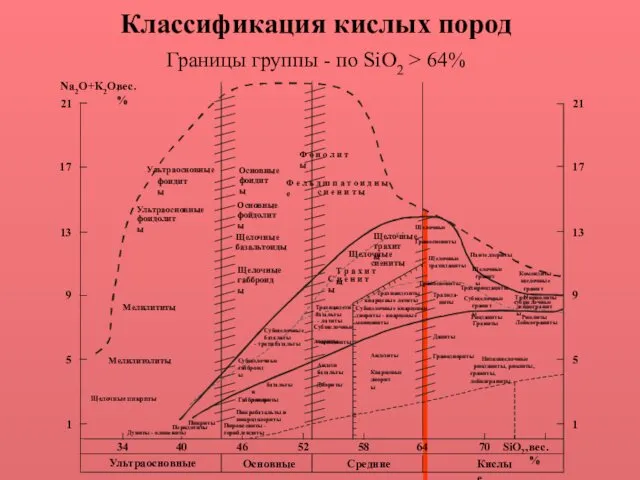 Классификация кислых пород
Классификация кислых пород Хімія та побут
Хімія та побут Биогенные элементы. Классификация. Топография биогенных элементов в организме человека
Биогенные элементы. Классификация. Топография биогенных элементов в организме человека Методы разделения и очистки биомолекул. Ультрацентрифугирование (седиментация)
Методы разделения и очистки биомолекул. Ультрацентрифугирование (седиментация) Презентация по Химии "Способы получения металлов" - скачать смотреть
Презентация по Химии "Способы получения металлов" - скачать смотреть  Аміак
Аміак  Анионно-координационная полимеризация
Анионно-координационная полимеризация Металл серебро
Металл серебро Растворы неэлектролитов и электролитов
Растворы неэлектролитов и электролитов Organic molecules
Organic molecules Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Технология производства простых полиэфиров
Технология производства простых полиэфиров Литье под давлением реактопластов
Литье под давлением реактопластов Химия функциональных материалов. Адсорбционные материалы. Цеолиты
Химия функциональных материалов. Адсорбционные материалы. Цеолиты Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно
Презентация по Химии "«Тверда вода»" - скачать смотреть бесплатно Физиологические эффекты активных форм кислорода
Физиологические эффекты активных форм кислорода Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра
Поліетилен Фенолформальдегідна смола Фторопласт Поліамід Поліметилакрилат Поліпропілен Полівінілхлорид Гетинакс політетра Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Межмолекулярные силы (силы Ван дер Ваальса)
Межмолекулярные силы (силы Ван дер Ваальса) Углеводы. Глюкоза. ЗНАНИЯ, НЕПРОВЕРЕННЫЕ ОПЫТОМ, МАТЕРЬЮ ВСЯКОЙ ДОСТОВЕРНОСТИ, БЕСПЛОДНЫ И ПОЛНЫ ОШИБОК ЛЕОНАРДО ДА ВИНЧИ
Углеводы. Глюкоза. ЗНАНИЯ, НЕПРОВЕРЕННЫЕ ОПЫТОМ, МАТЕРЬЮ ВСЯКОЙ ДОСТОВЕРНОСТИ, БЕСПЛОДНЫ И ПОЛНЫ ОШИБОК ЛЕОНАРДО ДА ВИНЧИ  Метаморфизм
Метаморфизм Катаболизм фенилаланина, тирозина
Катаболизм фенилаланина, тирозина Живая и мертвая вода
Живая и мертвая вода Главная подгруппа V группы..Азот
Главная подгруппа V группы..Азот