Содержание
- 2. История открытия Считается, что фосфор открыл в 1669 году алхимик из Гамбурга Хеннинг Бранд. Он был
- 3. История открытия Он собрал около тонны мочи из солдатских казарм и выпаривал ее до образования сиропообразной
- 4. Природные соединения Из-за большой химической активности встречается в природе только в виде соединений. Важнейшими минералами фосфора
- 5. Природные соединения Крупнейшее месторождение апатитов находится на Кольском полуострове, в районе Хибинских гор. Залежи фосфоритов находятся
- 6. Нахождение в природе Фосфор входит в состав всех живых организмов. А именно он встречается в соединениях:
- 7. Получение Фосфор производят в электрических печах, восстанавливая апатит углем в присутствии кремнезема: Ca3(PO4)2+3SiO2+5C=3CaSiO3+5CO+P2 Пары фосфора при
- 8. Важнейшие соединения Н3РО4 фосфорная кислота Р2О5 оксид фосфора (V)
- 9. Аллотропные модификации фосфора
- 10. Физические свойства Элементарный фосфор в обычных условиях представляет собой несколько устойчивых аллотропических модификаций; вопрос аллотропии фосфора
- 12. Аллотропные модификации Горение белого фосфора Белый фосфор окисляется кислородом уже при обычных условиях, а в тонкоизмельченном
- 13. Химические свойства В химических реакциях проявляет окислительно-восстановительную двойственность. Как окислитель взаимодействует со многими металлами, образуя фосфиды.
- 14. Химические свойства При длительном нагревании белого фосфора без доступа воздуха он желтеет и постепенно превращается в
- 15. Оксид фосфора (V) Р2О5 – белый порошок, очень гигроскопичен (самый эффективный осушитель). Является типичным кислотным оксидом.
- 16. Физические свойства P2O5 Белый, рыхлый порошок, гигроскопичный. Хранят в герметически закрытых сосудах.
- 17. Химические свойства P2O5 Проявляет свойства кислотного оксида. 1) реагирует с водой: P2O5 + H2O 2HPO3 P2O5
- 18. Ортофосфорная кислота Получение. Р О + Н О 2 2 5 ↔ 3 4 Р Н
- 19. Ортофосфорная кислота Получение. Ca PO4 + H SO4 ↔ 3 2 2 + ( ) Ca
- 20. Ортофосфорная кислота Ортофосфорная кислота – кристаллическое, нелетучее, твердое, бесцветное вещество. Смешивается с водой в любых отношениях.
- 21. Круговорот фосфора в природе
- 22. Применение фосфора
- 23. Применение фосфора Около 80% от всего производства белого фосфора идет на синтез чистой ортофосфорной кислоты. Она
- 24. Применение фосфора: спички Первые фосфорные спички – с головкой из белого фосфора – были созданы лишь
- 25. Применение фосфора: спички Зажигательная поверхность спичечного коробка покрыта смесью красного фосфора и порошка стекла. В состав
- 26. Применение фосфора Немало ортофосфорной кислоты потребляет пищевая промышленность. Дело в том, что на вкус разбавленная ортофосфорная
- 27. Применение фосфора Интересны и другие применения ортофосфорной кислоты в промышленности. Например, было замечено, что пропитка древесины
- 28. Необходим ли фосфор человеку?
- 29. Значение фосфора Фосфор является основой скелета человека и зубов. Живые организмы не могут обходиться без фосфора.
- 30. Биологическая роль фосфора Суточная потребность для взрослого человека 1 грамм Входит в состав скелета Входит в
- 31. Реакция организма на недостаток и избыток фосфора Недостаток фосфора Развивается заболевание рахит, снижается умственная и мышечная
- 33. Скачать презентацию






























 Презентация по Химии "Ярмарок професій" - скачать смотреть
Презентация по Химии "Ярмарок професій" - скачать смотреть  Требования, предъявляемые к дизельным топливам
Требования, предъявляемые к дизельным топливам Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т
Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т Тесты для самопроверки
Тесты для самопроверки Позднемеловая трубка взрыва щелочных базальтов Красноозерная
Позднемеловая трубка взрыва щелочных базальтов Красноозерная Растворы. Первичные понятия
Растворы. Первичные понятия Как сделать духи для любимой мамочки? Выполнил: Причина Алексей Учащийся 3 класса Б МОУ СОШ № 64
Как сделать духи для любимой мамочки? Выполнил: Причина Алексей Учащийся 3 класса Б МОУ СОШ № 64 Acizi, baze, oxizi, săruri. Caracteristica generală, proprietă ți fizice și chimice
Acizi, baze, oxizi, săruri. Caracteristica generală, proprietă ți fizice și chimice Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна
Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна  Тест по теме: «Алканы» Автор: учитель химии МОУСОШ № 6 Ким Н. В.
Тест по теме: «Алканы» Автор: учитель химии МОУСОШ № 6 Ким Н. В. Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон
Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон Отдельные классы дисперсных систем
Отдельные классы дисперсных систем Воздушные и тепловые свойства почв
Воздушные и тепловые свойства почв Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Своя игра по химии
Своя игра по химии Алкены
Алкены Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Открытие периодического закона Д.И. Менделеева
Открытие периодического закона Д.И. Менделеева Органическая химия 10 класс А.А.Карцовой и А.Н.Лёвкина
Органическая химия 10 класс А.А.Карцовой и А.Н.Лёвкина Применение циклической вольтамперометрии для определения истинной Sпов платины и оценки стабильности
Применение циклической вольтамперометрии для определения истинной Sпов платины и оценки стабильности Коррозия металлов
Коррозия металлов Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн
Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Презентация по Химии "Классификация углеводородов" - скачать смотреть
Презентация по Химии "Классификация углеводородов" - скачать смотреть  Силикаты. Пироксены. Амфиболы. Полевые шпаты
Силикаты. Пироксены. Амфиболы. Полевые шпаты Мыс айналымы
Мыс айналымы Хроматографический анализ
Хроматографический анализ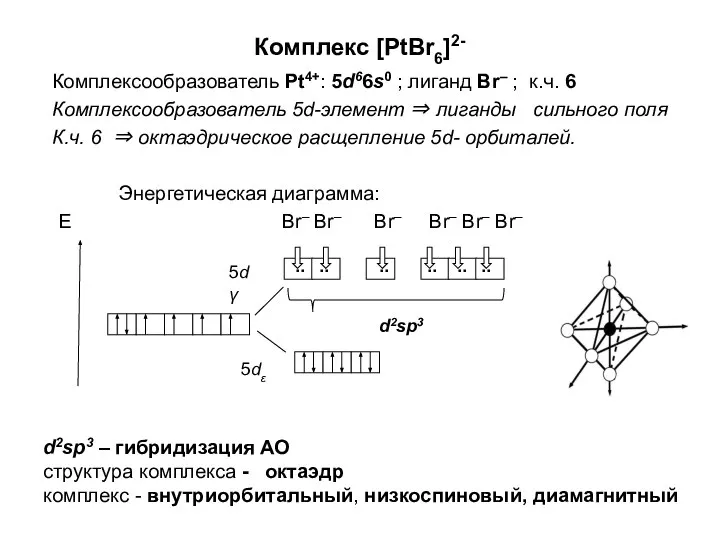 Комплексообразователь. (Лекция 5)
Комплексообразователь. (Лекция 5)