Содержание
- 2. Галогены — химические элементы фтор F, хлор Cl, бром Br, иод I и астат At, составляющие
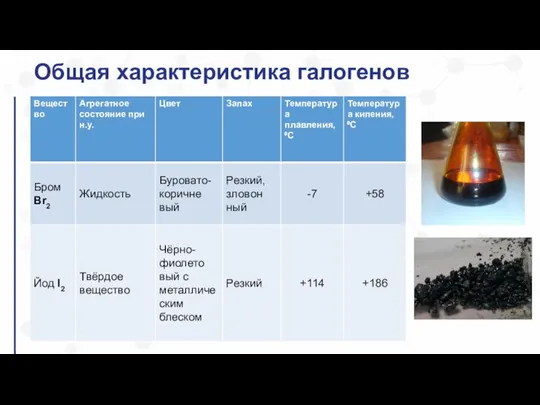
- 3. Общая характеристика галогенов
- 4. Общая характеристика галогенов
- 5. История открытия галогенов Термин «галогены» в отношении всей группы элементов (на тот момент были известны фтор,
- 6. История открытия фтора “Фторос” – разрушение, гибель (греч.). В 1771 г. Карл Шееле получил HF. Сам
- 7. История открытия хлора Впервые хлор был получен и описан К. Шееле в 1774 г. Получен он
- 8. История открытия хлора Однако ни сам Шееле, ни его современники не считали этот газ самостоятельным химическим
- 9. История открытия брома Впервые был получен Ю. Либихом, но он “проглядел” открытие, приняв бром за смесь
- 10. История открытия йода Открыт в 1811 г. французским химиком-селитроваром Б. Куртуа. Согласно легенде, на заводе, где
- 11. История открытия йода Новое вещество привлекло внимание двух знаменитых ученых – французского Ж. Л. Гей-Люссака и
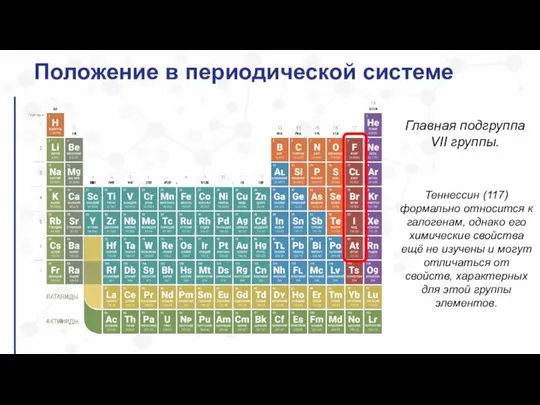
- 12. Положение в периодической системе Главная подгруппа VII группы. Теннессин (117) формально относится к галогенам, однако его
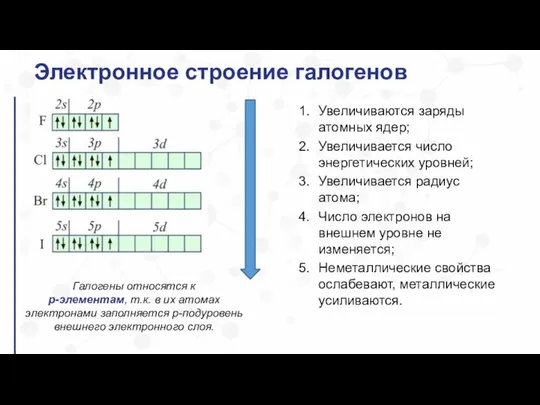
- 13. Электронное строение галогенов Галогены относятся к р-элементам, т.к. в их атомах электронами заполняется р-подуровень внешнего электронного
- 14. Возбуждённое состояние на примере хлора В = 1 В = 3 В = 5 В =
- 15. Валентность хлора в соединениях
- 16. Задание №1 Нарисуйте электронную оболочку фтора. Сделайте вывод о валентных возможностях данного элемента. Ответ: Фтор не
- 17. Задание №2 Определите, в каких соединениях хлор обладает валентностью, равной 3. Нарисуйте строение молекул этих веществ.
- 18. Фтор в соединениях проявляет только одну степень окисления: -1. Это элемент с самой высокой электроотрицательностью. Важнейшие
- 19. Для хлора характерен целый спектр степеней окисления, среди которых есть как положительные, так и отрицательные. Важнейшие
- 20. Задание №3 Установите, как изменяется степень окисления галогенов в следующих реакциях: 1. HCl + O2 =
- 21. Важными неорганическими соединениями хлора являются хлористый водород (HCl) и хлориды (NaCl, KCl и др.). Важнейшие соединения
- 22. В природе галогены встречаются только в виде соединений. Галогены в природе Фтор встречается в виде флюорита
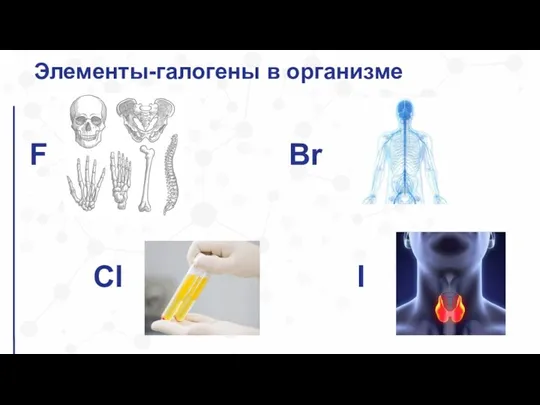
- 23. Элементы-галогены в организме F Br Cl I
- 24. Хлор используется для обеззараживания воды, производство соляной кислоты, а также пластмасс, каучуков, растворителей, красителей. Поваренная соль
- 26. Скачать презентацию



















 Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола
Метаболизм липидов. Липолиз. Окисление жирных кислот и глицерола Закон сохранения массы веществ Омельянчук Т.Е. учитель химии МАОУ ДСОШ №2 г. Домодедово
Закон сохранения массы веществ Омельянчук Т.Е. учитель химии МАОУ ДСОШ №2 г. Домодедово Получение и исследование свойств хромата калия
Получение и исследование свойств хромата калия Конфигурация макромолекулы
Конфигурация макромолекулы Презентация по Химии "Техника безопасности в кабинете химии" - скачать смотреть
Презентация по Химии "Техника безопасности в кабинете химии" - скачать смотреть  Валентность
Валентность Нафта, сланцевий газ, екологія середовища Підготувала учениця 11 Б класу Кандибка Ольга
Нафта, сланцевий газ, екологія середовища Підготувала учениця 11 Б класу Кандибка Ольга  Алкины
Алкины Алюминий
Алюминий Основные классы неорганических соединений
Основные классы неорганических соединений неметаллы Общая характеристика
неметаллы Общая характеристика Нуклеин қышқылдары
Нуклеин қышқылдары Поверхностные явления. Уравнение Гиббса
Поверхностные явления. Уравнение Гиббса Защита металлов от коррозии
Защита металлов от коррозии Дисахариды Ширяева София ХБ-4 г.Липецк 2012
Дисахариды Ширяева София ХБ-4 г.Липецк 2012 Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки Обозначения химического состава и пищевой ценности продовольственных товаров
Обозначения химического состава и пищевой ценности продовольственных товаров Ископаемое топливо
Ископаемое топливо Химическая термодинамика
Химическая термодинамика ПОРТФОЛІО вчителя хімії та біології Турбівської загальноосвітньої школи І – ІІІ ступенів 2014 рік
ПОРТФОЛІО вчителя хімії та біології Турбівської загальноосвітньої школи І – ІІІ ступенів 2014 рік ФИЗИОЛОГИЯ ПИТАНИЯ. Урок по кулинарии. 7 класс. Разработал: учитель технологии Дятлова Елена Владимировна
ФИЗИОЛОГИЯ ПИТАНИЯ. Урок по кулинарии. 7 класс. Разработал: учитель технологии Дятлова Елена Владимировна  Нуклеиновые кислоты
Нуклеиновые кислоты Строение атома
Строение атома Теория строения химических веществ
Теория строения химических веществ Презентация по Химии "АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА" - скачать смотреть бесплатно
Презентация по Химии "АЗОТНАЯ КИСЛОТА И ЕЕ СВОЙСТВА" - скачать смотреть бесплатно Кислородсодержащие органические соединения. Предельные одноатомные спирты
Кислородсодержащие органические соединения. Предельные одноатомные спирты Обмен холестерола
Обмен холестерола Электролиз
Электролиз