Содержание
- 2. Гидролиз солей (разложение водой)-химическое взаимодействие ионов соли с ионами воды , приводящее к образованию слабого электролита
- 3. В зависимости от того какой ион соли вступает во взаимодействие с водой , различают 3 типа
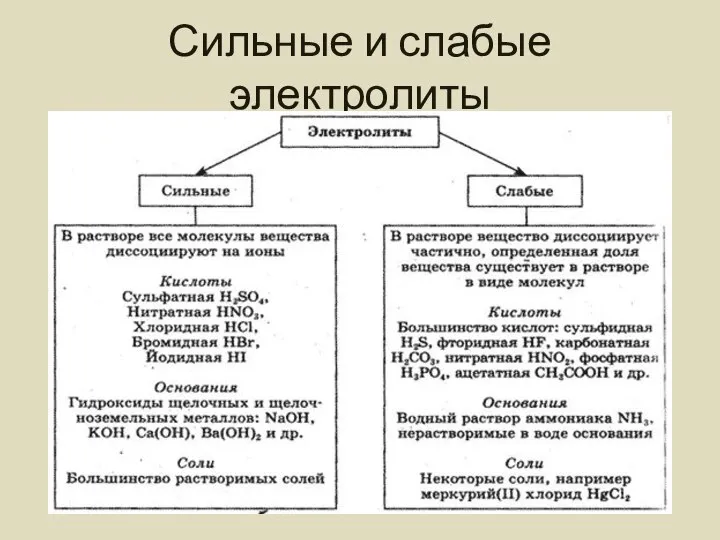
- 4. Сильные и слабые электролиты
- 5. Соли , образованные сильной кислотой и слабым основанием Среда раствора-кислая Гидролиз по катиону При гидролизе солей,
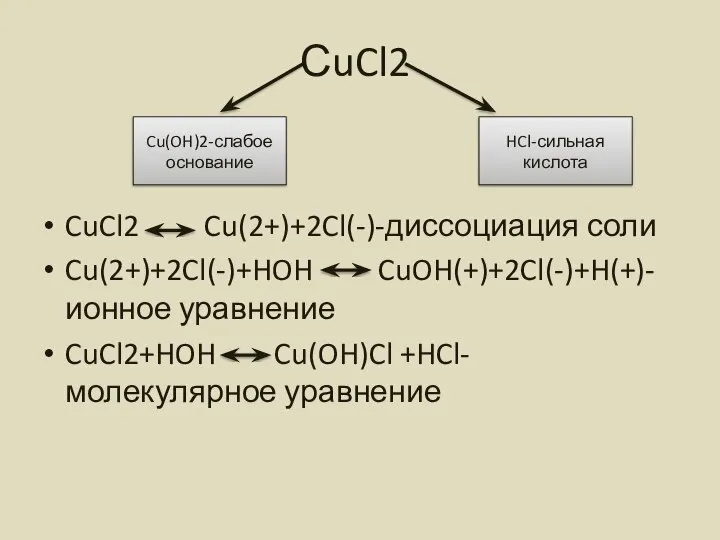
- 6. СuCl2 CuCl2 Cu(2+)+2Cl(-)-диссоциация соли Cu(2+)+2Cl(-)+HOH CuOH(+)+2Cl(-)+H(+)-ионное уравнение CuCl2+HOH Cu(OH)Cl +HCl- молекулярное уравнение Cu(OH)2-слабое основание HCl-сильная кислота
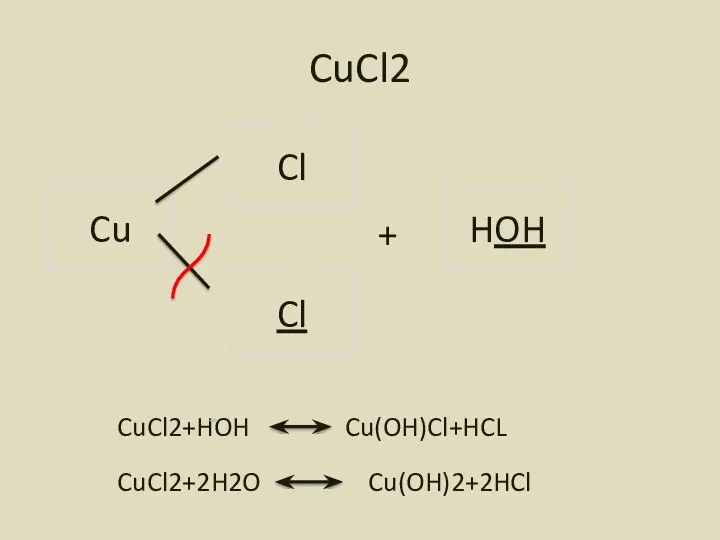
- 7. CuCl2 Cu Cl Cl + HOH CuCl2+HOH Cu(OH)Cl+HCL CuCl2+2H2O Cu(OH)2+2HCl
- 8. Соли , образованные слабой кислотой и сильным основанием Среда раствора-щелочная Гидролиз по аниону При гидролизе солей
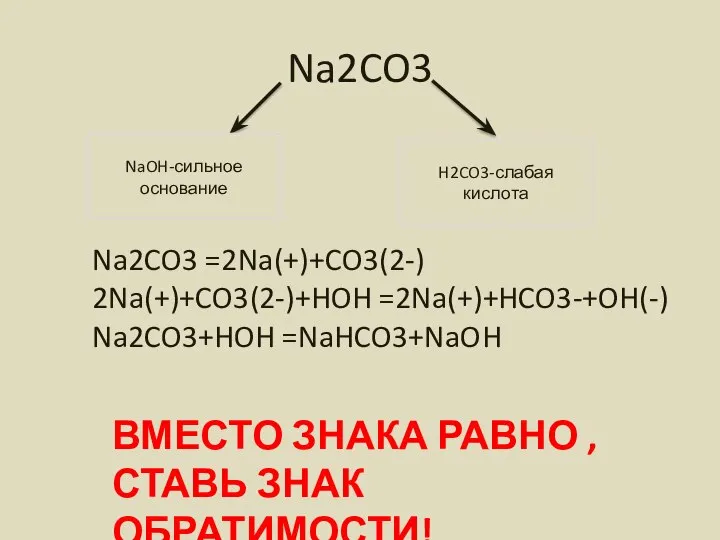
- 9. Na2CO3 NaOH-сильное основание H2CO3-слабая кислота Na2CO3 =2Na(+)+CO3(2-) 2Na(+)+CO3(2-)+HOH =2Na(+)+HCO3-+OH(-) Na2CO3+HOH =NaHCO3+NaOH ВМЕСТО ЗНАКА РАВНО ,СТАВЬ ЗНАК
- 10. Соли , образованные слабой кислотой и слабым основанием Среда раствора зависит от степени диссоциации продуктов. Если
- 12. Zn(2+)S(2-)+H(+)OH(-)=По законам физики плюс идет к минусу , минус к плюсу Zn(OH)2+H2S
- 14. Скачать презентацию







 Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Металлы и сплавы. История цивилизаций
Металлы и сплавы. История цивилизаций Многоатомные спирты. Фенол.
Многоатомные спирты. Фенол. Из чего оно сделано молоко
Из чего оно сделано молоко Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь
Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР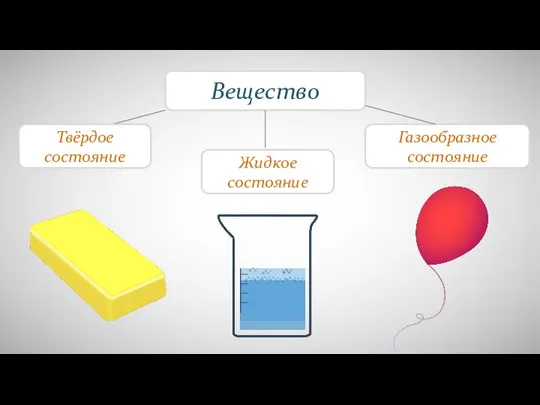 Различия в молекулярном строении газов, жидкостей и твердых тел
Различия в молекулярном строении газов, жидкостей и твердых тел Презентация по химии Введение в биоорганическую химию
Презентация по химии Введение в биоорганическую химию  160198375
160198375 Методы контроля и анализа веществ
Методы контроля и анализа веществ Чистые вещества и смеси
Чистые вещества и смеси Приборы для измерения температуры
Приборы для измерения температуры Химические реакции. Реакции по фазовому составу
Химические реакции. Реакции по фазовому составу Викторина. Дмитрий Иванович Менделеев
Викторина. Дмитрий Иванович Менделеев Viscoelasticity
Viscoelasticity Фолиевая кислота
Фолиевая кислота  Менделєєв Дмитро Іванович Роботу виконав: Учень 11 - Б класу Вдовіченко І. Вчитель інформатики: Трибко О.Б.
Менделєєв Дмитро Іванович Роботу виконав: Учень 11 - Б класу Вдовіченко І. Вчитель інформатики: Трибко О.Б.  Щелочноземельные металлы
Щелочноземельные металлы Воронежская область п.г.т. Анна, МОУ Аннинская средняя общеобразовательная школа №1 Выполнила: учитель химии высшей квалифика
Воронежская область п.г.т. Анна, МОУ Аннинская средняя общеобразовательная школа №1 Выполнила: учитель химии высшей квалифика Углеводы: простые и сложные. Строение, свойства и биологическая роль
Углеводы: простые и сложные. Строение, свойства и биологическая роль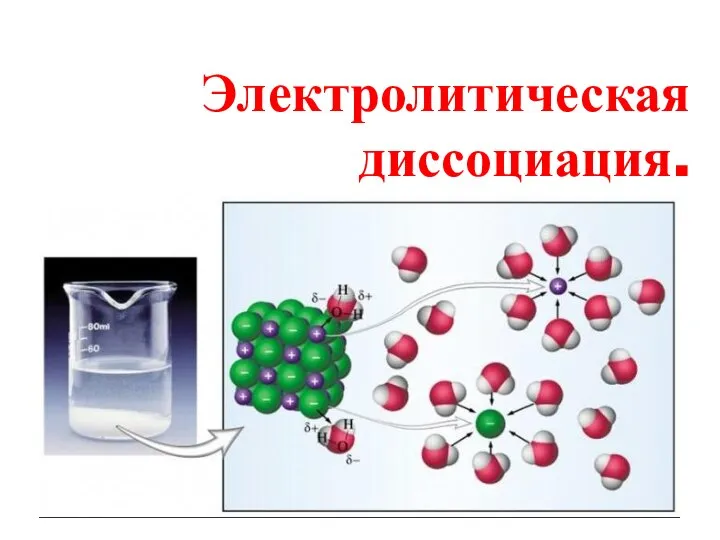 Электролитическая диссоциация
Электролитическая диссоциация Опал
Опал Презентация по Химии "Глюкоза - альдегідоспирт" - скачать смотреть бесплатно
Презентация по Химии "Глюкоза - альдегідоспирт" - скачать смотреть бесплатно Лекарственные растения и сырье, содержащие гликозиды. (Лекция 7)
Лекарственные растения и сырье, содержащие гликозиды. (Лекция 7) Защитные покрытия поверхности металла от коррозии
Защитные покрытия поверхности металла от коррозии Автомобильные бензины и дизельное топливо
Автомобильные бензины и дизельное топливо Адсорбционные равновесия и процессы на подвижных и неподвижных границах раздела
Адсорбционные равновесия и процессы на подвижных и неподвижных границах раздела Степень диссоциации. 9 класс
Степень диссоциации. 9 класс