Содержание
- 2. N 2e 5e – – Азот может принимать степени окисления: –3, +1, +2, +3, +4, +5
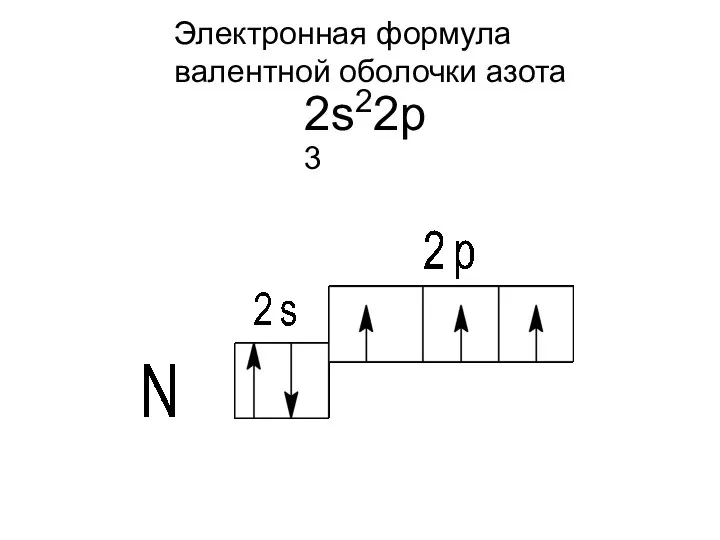
- 3. Электронная формула валентной оболочки азота 2s22p3
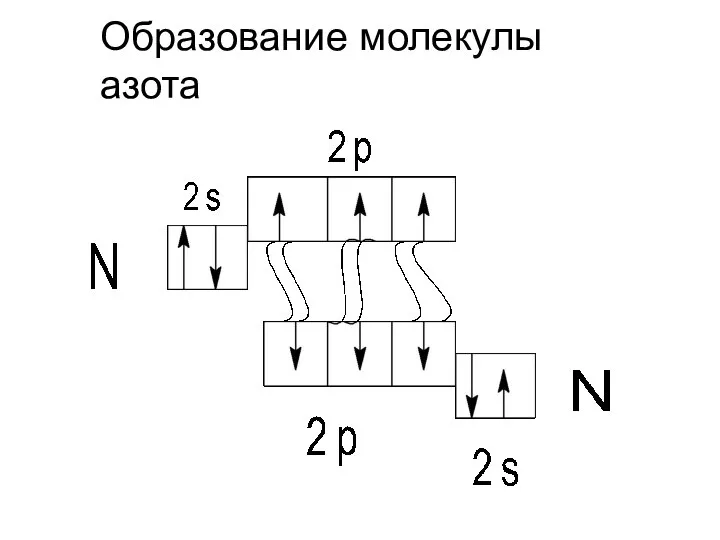
- 4. Образование молекулы азота
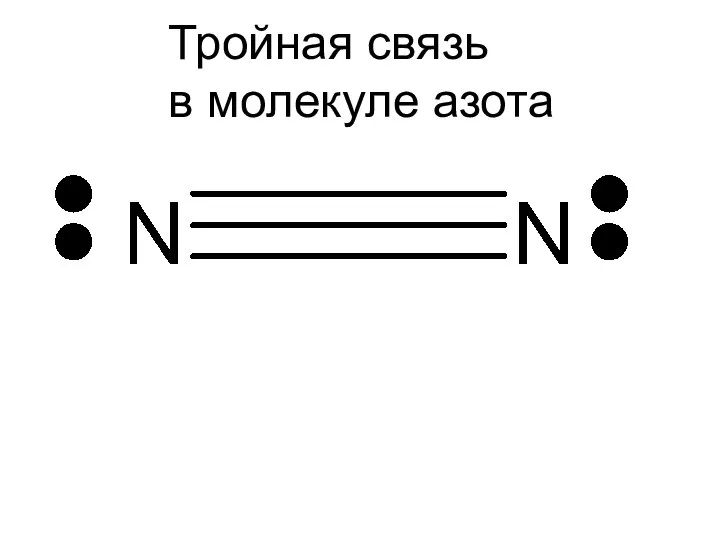
- 5. Тройная связь в молекуле азота
- 6. Азот David.Monniaux N N N2 Физические свойства Азот – газ без цвета, запаха и вкуса, немного
- 7. Д. Резерфорд 1749–1819 гг. К. Шееле 1742–1786гг. Впервые газ, который не поддерживает дыхание и горение, получили
- 8. А. Лавуазье 1778–1825 гг. В 1787 году этот же газ обнаружил в воздухе А. Лавуазье, который
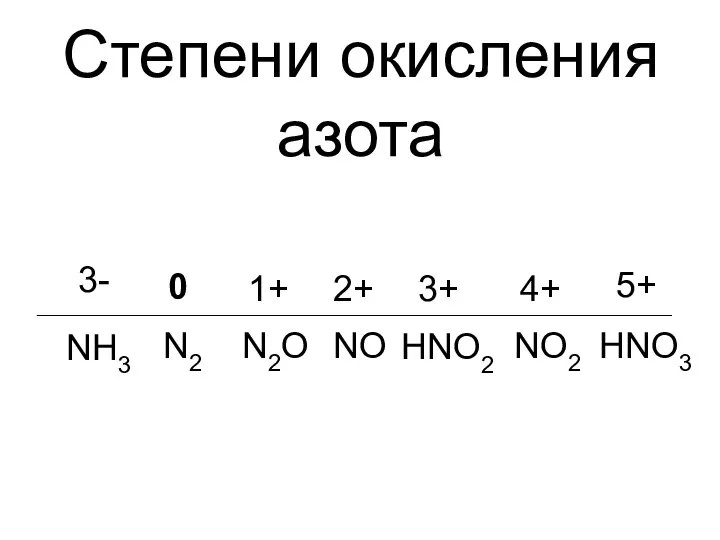
- 9. Степени окисления азота 0 N2 1+ N2O 3+ NO 2+ HNO3 4+ 5+ HNO2 NO2 3-
- 10. Чилийская селитра (NaNO3)
- 11. Химические свойства При взаимодействии с металлами и водородом азот является окислителем. 6Li + N2 = 2Li3N
- 12. Азот взаимодействует с водородом при высоких температурах, наличии катализатора и высоком давлении с образованием аммиака. Азот
- 13. N2 + O2 = 2NO – Q При взаимодействии с кислородом азот является восстановителем.
- 14. В природе азот содержится в основном в атмосфере — 78% по объёму или 75,5% по массе.
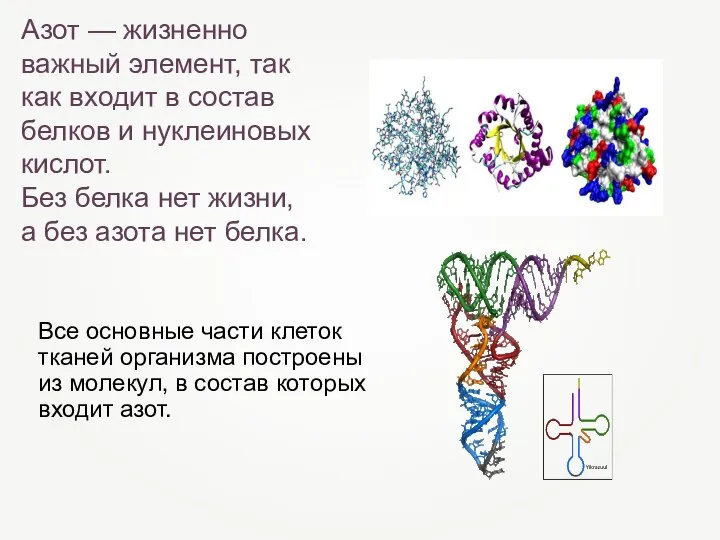
- 15. Азот — жизненно важный элемент, так как входит в состав белков и нуклеиновых кислот. Без белка
- 16. Организм животного содержит 1–10% азота от общей массы тела, больше всего азота содержится в шерсти, волосах,
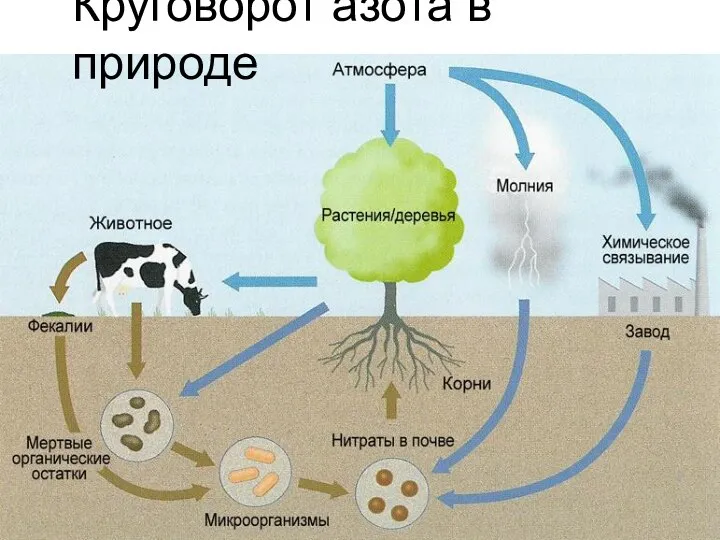
- 17. Круговорот азота в природе
- 18. В производстве азот получают из воздуха, переведённого в жидкое состояние.
- 19. Получение азота В лабораториях его можно получать 1. По реакции разложения нитрита аммония: NH4NO2 → N2↑
- 20. Применение азота Производство аммиака и производство азотной кислоты Холодильные установки, производство удобрений, в медицине, в быту
- 21. Аммиак Физические свойства Аммиа́к — NH3, нитрид водорода — бесцветный газ с резким характерным запахом (запах
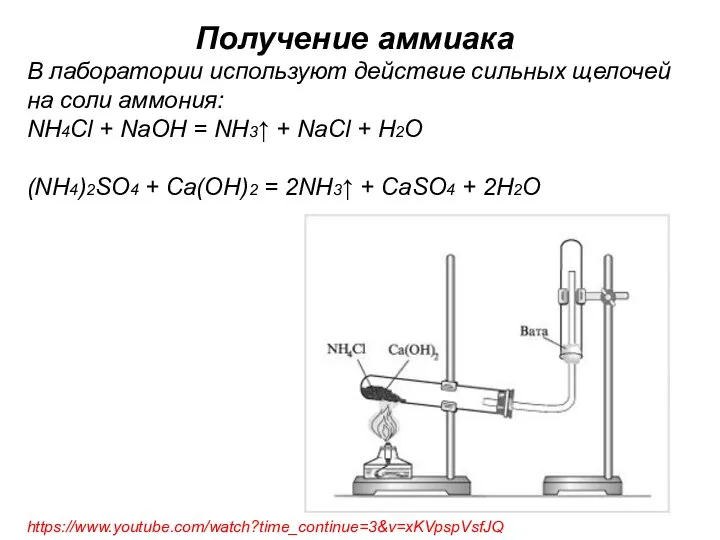
- 22. Получение аммиака В лаборатории используют действие сильных щелочей на соли аммония: NH4Cl + NaOH = NH3↑
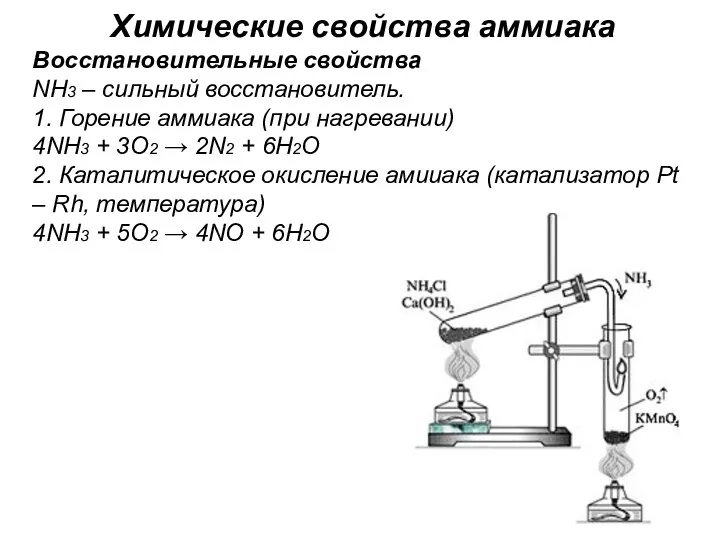
- 23. Химические свойства аммиака Восстановительные свойства NH3 – сильный восстановитель. 1. Горение аммиака (при нагревании) 4NH3 +
- 24. Взаимодействие с водой и кислотами NH3 + Н2О ↔ NН4 ОН NH3 + HCl = NH4Cl
- 25. Соли аммония 1. Вступают в обменную реакцию с кислотами и солями: (NH4)2SO4 + Ba(NO3)2 → BaSO4
- 26. Азотная кислота
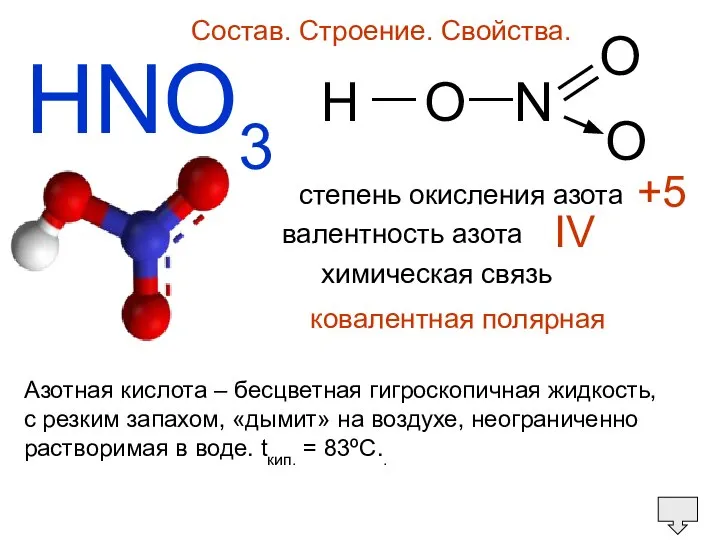
- 27. HNO3 Состав. Строение. Свойства. H O N O O — — степень окисления азота валентность азота
- 28. Азотная кислота – бесцветная гигроскопичная жидкость, c резким запахом, «дымит» на воздухе, неограниченно растворимая в воде.
- 29. При хранении на свету разлагается на оксид азота (IV), кислород и воду, приобретая желтоватый цвет: 4HNO3
- 30. Химические свойства азотной кислоты Азотная кислота проявляет все типичные свойства кислот. Кислоты взаимодействуют с основными и
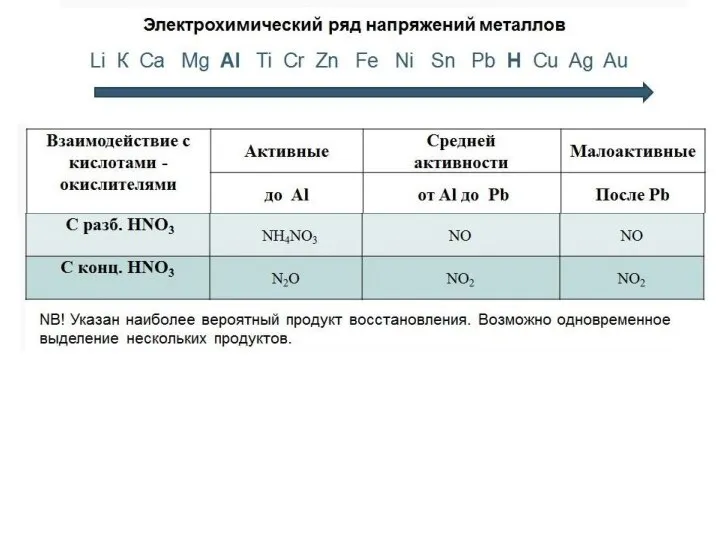
- 31. Особенности взаимодействия азотной кислоты с металлами: 1. Водород не выделяется. . Выделяются разнообразные соединения азота: N+4O2,
- 33. Применение азотной кислоты 1 5 4 6 2 3 Производство азотных и комплексных удобрений. Производство взрывчатых
- 34. Соли азотной кислоты Как называются соли азотной кислоты? нитраты Нитраты K, Na, NH4+ называют селитрами Составьте
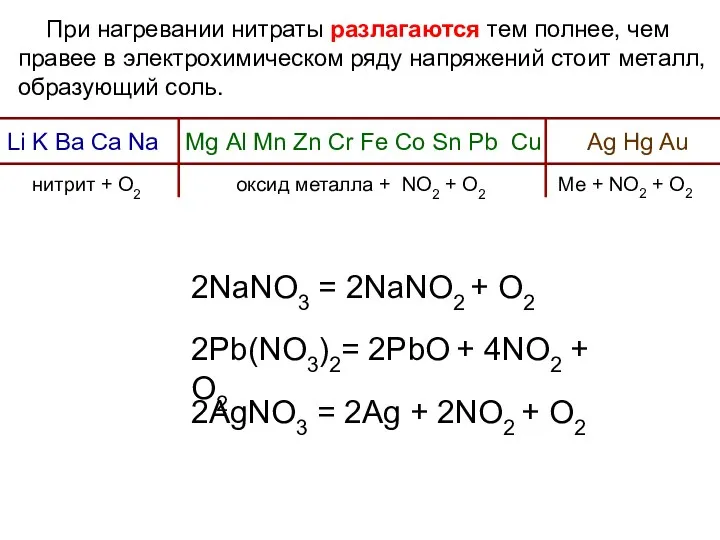
- 35. При нагревании нитраты разлагаются тем полнее, чем правее в электрохимическом ряду напряжений стоит металл, образующий соль.
- 36. Нитрат калия (калиевая селитра) Бесцветные кристаллы Значительно менее гигроскопична по сравнению с натриевой, поэтому широко применя-ется
- 37. Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение
- 38. СПАСИБО ЗА ВНИМАНИЕ!
- 40. Скачать презентацию


























 Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ»
Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ» Решение задач по химической формуле
Решение задач по химической формуле Кинетическое уравнение математическая запись закона действующих масс
Кинетическое уравнение математическая запись закона действующих масс Классификация металлов
Классификация металлов Diamonds
Diamonds Продукты - рекордсмены по содержанию различных минеральных компонентов
Продукты - рекордсмены по содержанию различных минеральных компонентов Ионообменная хроматография и ее применение
Ионообменная хроматография и ее применение Почему мыло пенится
Почему мыло пенится Массообменные процессы
Массообменные процессы Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ
Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ Автомобильные бензины и дизельные топлива. Характеристика и классификация автомобильных топлив
Автомобильные бензины и дизельные топлива. Характеристика и классификация автомобильных топлив Союз химии и медицины
Союз химии и медицины Граниты. Происхождение гранитов
Граниты. Происхождение гранитов Презентация к дистанционному уроку, уроку, внеклассному мероприятию, по химии «Предельные одноатомные спирты»
Презентация к дистанционному уроку, уроку, внеклассному мероприятию, по химии «Предельные одноатомные спирты» Стероиды - производные углеводорода стерана
Стероиды - производные углеводорода стерана Золото Aurum
Золото Aurum Изменение агрегатных состояний вещества_
Изменение агрегатных состояний вещества_ Модифицирование структуры хитозана аллильными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры хитозана аллильными заместителями: твердофазный синтез, исследование структуры и свойств Топливо и его свойства
Топливо и его свойства Жиры (триглицериды)
Жиры (триглицериды) Фазовые равновесия «раствор-пар» в двухкомпонентных системах из двух летучих жидкостей
Фазовые равновесия «раствор-пар» в двухкомпонентных системах из двух летучих жидкостей Валериановая кислота
Валериановая кислота Плазменное состояние вещества
Плазменное состояние вещества Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини та використання продуктів її переробки
Охорона навколишнього середовища від забруднень при переробці вуглеводневої сировини та використання продуктів її переробки  Железы внутренней секреции
Железы внутренней секреции  Основные понятия и законы химии
Основные понятия и законы химии Нефть. Способы её переработки. Продукты переработки нефти
Нефть. Способы её переработки. Продукты переработки нефти Стехиометрия и классификация твердых веществ
Стехиометрия и классификация твердых веществ