Содержание
- 2. 1. Идеальные растворы из неограниченно смешивающихся жидкостей Жидкие вещества при обычных условиях могут смешиваться с друг
- 3. 1. Идеальные растворы из неограниченно смешивающихся жидкостей С практической точки зрения наиболее интересна зависимость давления насыщенного
- 4. 1. Идеальные растворы из неограниченно смешивающихся жидкостей Неограниченно растворимые жидкости разделяют на три типа: Идеальные бинарные
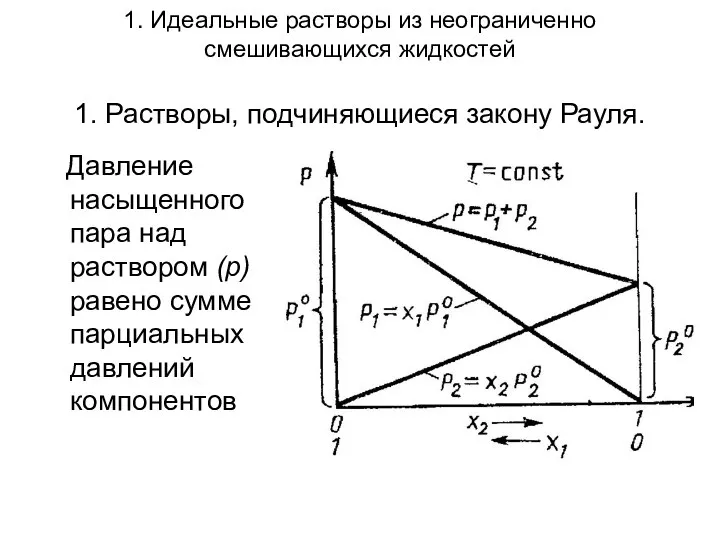
- 5. 1. Идеальные растворы из неограниченно смешивающихся жидкостей 1. Растворы, подчиняющиеся закону Рауля. Давление насыщенного пара над
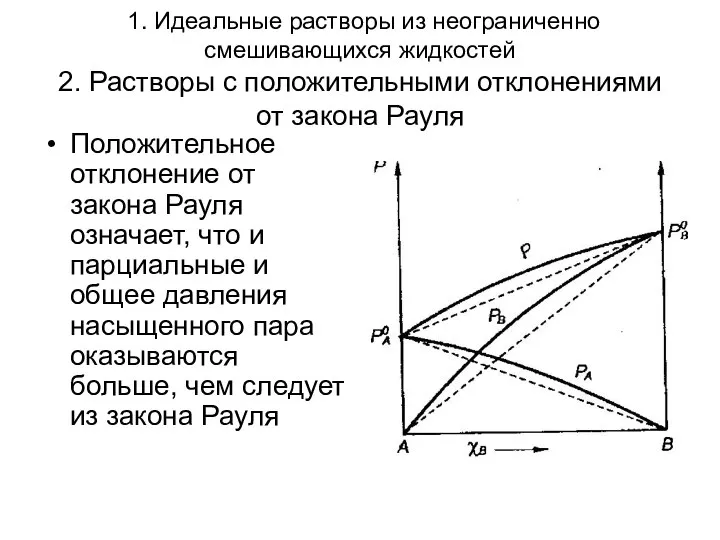
- 6. 1. Идеальные растворы из неограниченно смешивающихся жидкостей 2. Растворы с положительными отклонениями от закона Рауля Положительное
- 7. 1. Идеальные растворы из неограниченно смешивающихся жидкостей Положительные отклонения от закона Рауля наблюдаются в том случае,
- 8. 1. Идеальные растворы из неограниченно смешивающихся жидкостей Растворы с отрицательными отклонениями от закона Рауля Отрицательные отклонения
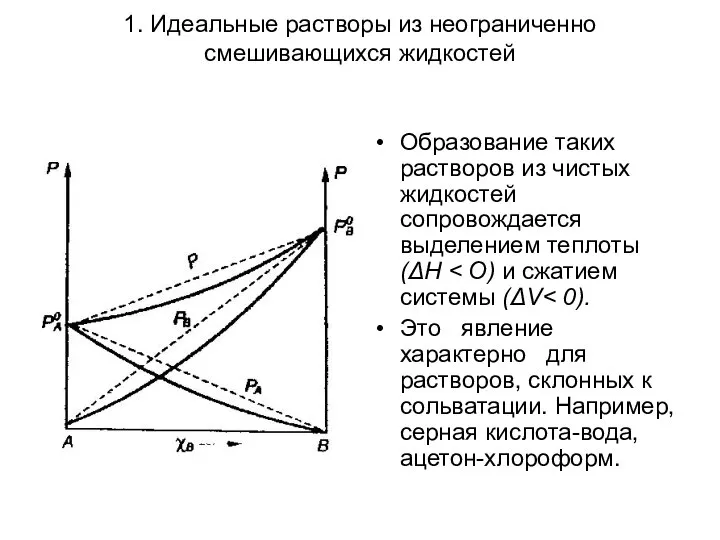
- 9. 1. Идеальные растворы из неограниченно смешивающихся жидкостей Образование таких растворов из чистых жидкостей сопровождается выделением теплоты
- 10. 1. Идеальные растворы из неограниченно смешивающихся жидкостей 3. В некоторых системах, где компоненты очень сильно отличаются
- 11. 1. Идеальные растворы из неограниченно смешивающихся жидкостей Жидкие смеси, состав которых соответствует экстремумам, называются азеотропными смесями,
- 12. 2. Законы Коновалова Состав жидкого раствора и пара в момент равновесия можно установить экспериментально. По результатам
- 14. 2. Законы Коновалова Проведем фазовый анализ диаграммы «температура - состав» Линия кипения - зависимость температуры кипения
- 15. 2. Законы Коновалова Линия конденсации отделяет область ненасыщенного пара от области сосуществования пара и жидкости. Она
- 16. 2. Законы Коновалова Область ниже линии кипения, соответствует некипящей жидкости (жидкости без пара). Любая фигуративная точка,
- 17. 2. Законы Коновалова Область выше линии конденсации, соответствует ненасыщенному пару (пару без жидкости). Любая фигуративная точка,
- 18. 2. Законы Коновалова Область между кривыми, соответствует сосуществованию пара и жидкости (кипящая жидкость или насыщенный пар).
- 19. 2. Законы Коновалова Чтобы определить состав сосуществующих фаз в системе, надо через данную фигуративную точку провести
- 20. 2. Законы Коновалова Соотношение между составами равновесных жидкости и пара, влияние добавления того или другого из
- 21. 2. Законы Коновалова Формулировка второго закона Коновалова: точки максимума или минимума на кривой давление пара -
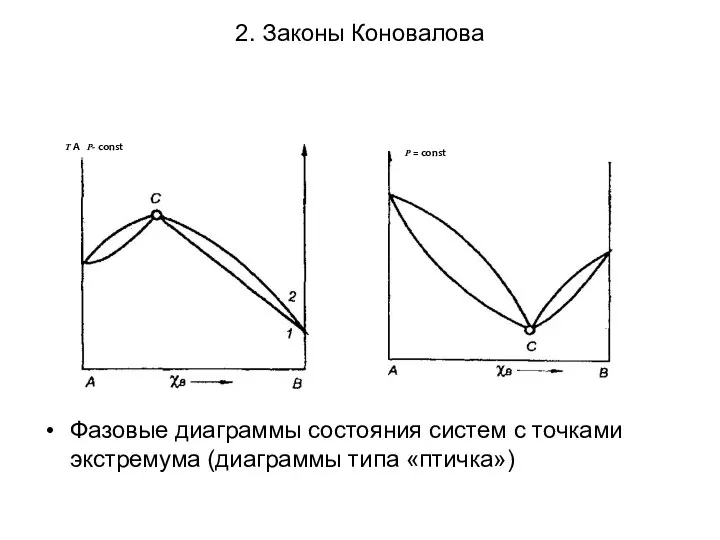
- 22. 2. Законы Коновалова Фазовые диаграммы состояния систем с точками экстремума (диаграммы типа «птичка»)
- 23. 2. Законы Коновалова Применение правила фаз Гиббса показывает, что для любой точки, отвечающей двухфазной системе, кроме
- 24. 3. Перегонка растворов Перегонка - процесс разделения жидких смесей, основанный на разнице температур их кипения. Этот
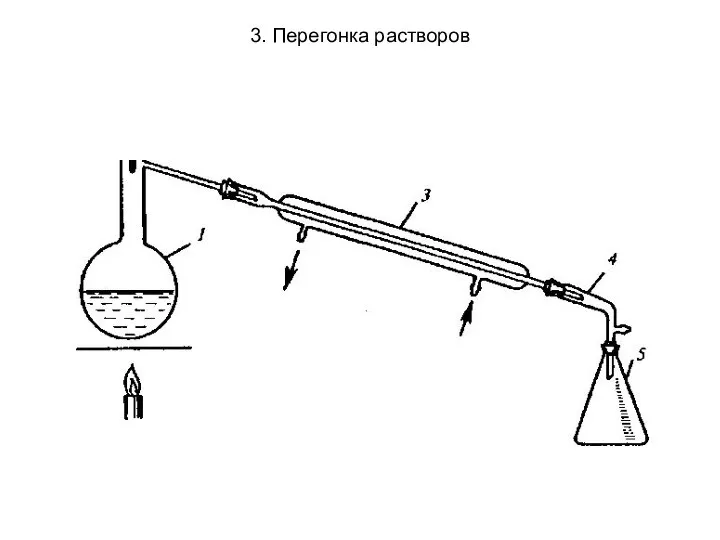
- 25. 3. Перегонка растворов Виды перегонок: Простая перегонка заключается в непрерывном нагревании жидкого раствора с отводом образующегося
- 26. 3. Перегонка растворов
- 27. 3. Перегонка растворов 2. Фракционная перегонка применяется для разделения смесей жидкостей, которые отличаются температурой кипения на
- 28. 3. Перегонка растворов
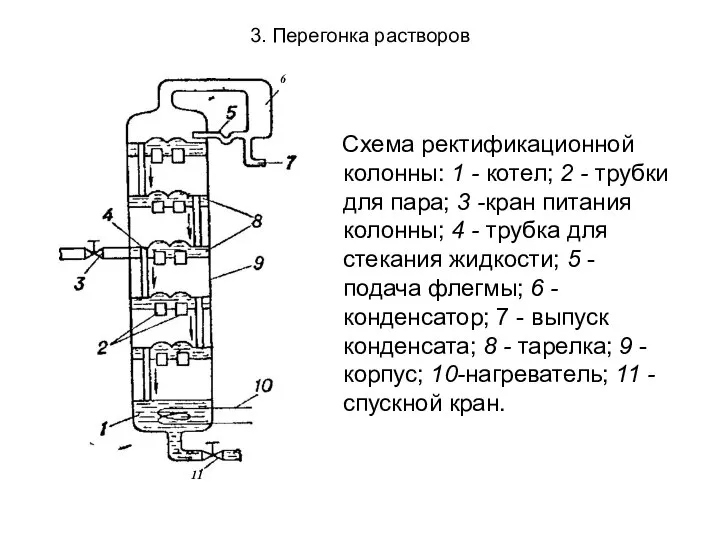
- 29. 3. Перегонка растворов 3. Ректификация - непрерывная фракционная перегонка, осуществляемая в специальных аппаратах - ректификационных колонах.
- 30. 3. Перегонка растворов Схема ректификационной колонны: 1 - котел; 2 - трубки для пара; 3 -кран
- 31. 3. Перегонка растворов Поступающая в колонку жидкость (А+В) быстро доводится до кипения и попадает на одну
- 32. 3. Перегонка растворов Методы разделения азеотропных смесей: • Химическое связывание одного из компонентов азеотропной смеси. Для
- 33. 3. Перегонка растворов Разделение азеотропной смеси путем добавления третьего компонента. Абсолютный спирт можно получить перегонкой азеотропной
- 35. Скачать презентацию


























 Олигосахариды и полисахариды
Олигосахариды и полисахариды Презентация по Химии "Волокнистые материалы вокруг нас" - скачать смотреть
Презентация по Химии "Волокнистые материалы вокруг нас" - скачать смотреть  Рефолдинг миниантител
Рефолдинг миниантител Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева Составил: учитель хим
Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева Составил: учитель хим Методические рекомендации по изучению курса «Коррозия и защита металлов»
Методические рекомендации по изучению курса «Коррозия и защита металлов» Бромды метил буының концентрациясын анықтау тәсілдемесі
Бромды метил буының концентрациясын анықтау тәсілдемесі Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і Соли в свете теории ЭД
Соли в свете теории ЭД Строение твердых и жидких металлов. Зональная ликвация
Строение твердых и жидких металлов. Зональная ликвация Презентация Подгруппа углерода и азота
Презентация Подгруппа углерода и азота Сульфаттар және эфирсульфаттар
Сульфаттар және эфирсульфаттар Устойчивое развитие
Устойчивое развитие Обмен белков, жиров и углеводов
Обмен белков, жиров и углеводов Основы общей химии
Основы общей химии Вдоль по радуге
Вдоль по радуге Машиностроительные материалы
Машиностроительные материалы The alkali metals
The alkali metals Устойчивость и коагуляция коллоидных систем
Устойчивость и коагуляция коллоидных систем Правила безпечного використання засобів побутової хімії.
Правила безпечного використання засобів побутової хімії.  Электролитическая диссоциация веществ
Электролитическая диссоциация веществ Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон
Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Аргентум, или серебро
Аргентум, или серебро Chemistry of life
Chemistry of life Алюминий
Алюминий  Гетерогенный катализ
Гетерогенный катализ Драгоценные камни
Драгоценные камни ОВР в гетерогенных системах
ОВР в гетерогенных системах