Содержание
- 2. 1. Что такое молекула? Молекула – это совокупность атомов, обладающая набором характерных отличительных свойств. Как можно
- 3. Молекула, далее, может быть устойчивой, но реакционноспособной или нереакционноспособной. Например, NO и СН3 устойчивы (т.е. не
- 4. За счёт чего же образуется химическая связь? Ответ: химические связи должны образоваться в результате понижения энергии
- 5. г) Экспериментальное определение порядка связи Ранее мы уже использовали энергию связи для определения порядка связи. При
- 7. На рис. можно заметить и другую характерную особенность химической связи. Более прочная связь в Н2 стягивает
- 8. Итак, мы рассмотрели образование связи в простейшей молекуле Н2. Однако, здесь имеется одна тонкость. Оказывается, что
- 9. Такая двухэлектронная двухцентровая связь называется ковалентной связью. Так же как и в атомах, движение электронов в
- 10. ОБЩИЕ ПРИНЦИПЫ ОБРАЗОВАНИЯ ХИМИЧЕСКИХ СВЯЗЕЙ. Связи образуются, если один или несколько электронов могут находиться около двух
- 11. Рассмотрим простейшие примеры. С помощью электронов – точек образование молекулы водорода можно представить следующим образом: В
- 12. Два 1s электрона не изображены, они включены в символ атома F , т.к. не участвуют в
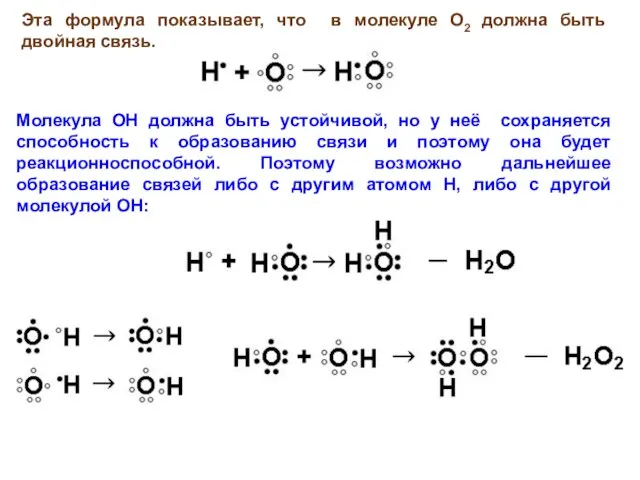
- 13. Эта формула показывает, что в молекуле О2 должна быть двойная связь. Молекула ОН должна быть устойчивой,
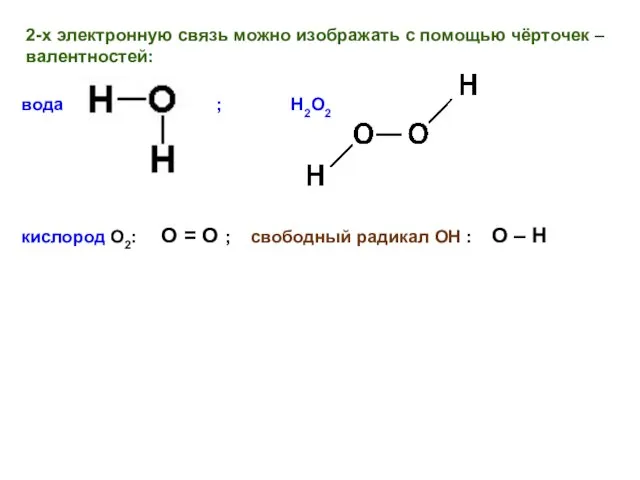
- 14. 2-х электронную связь можно изображать с помощью чёрточек – валентностей: вода ; Н2О2 кислород О2: О
- 15. Молекула, в которой имеется неспаренный валентный электрон, называется радикалом. Число общих электронных пар, связывающих атом данного
- 16. Характеристики связи Итак, более прочная связь в Н2 стягивает два протона ближе друг к другу, чем
- 17. Энергией связи двух атомов называется та энергия, которая выделяется при образовании этой связи, т.е. то уменьшение
- 18. ГОМОЯДЕРНЫЕ ДВУХАТОМНЫЕ МОЛЕКУЛЫ Очевидно, что кроме молекулы Н2 имеются и другие гомоядерные двухатомные молекулы. Например, в
- 19. Уменьшение потенциальной энергии, происходящее при обобществлении электронов в гомоядерных двухатомных молекулах, сильно зависит от положения атомов
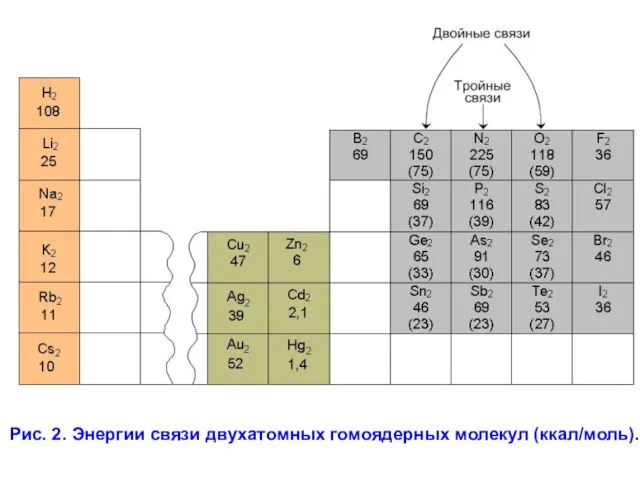
- 20. Рис. 2. Энергии связи двухатомных гомоядерных молекул (ккал/моль).
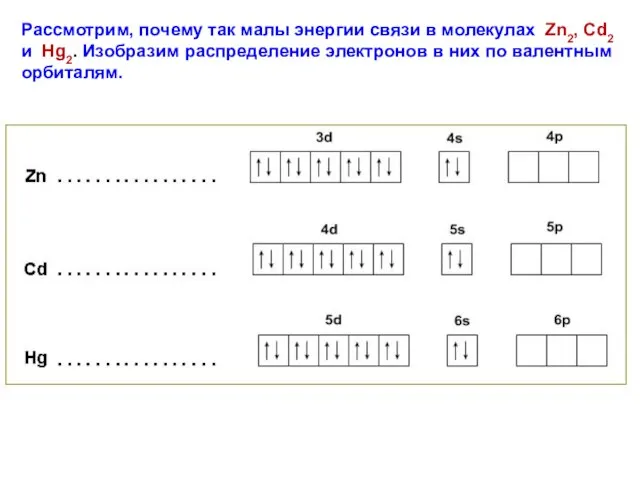
- 21. Рассмотрим, почему так малы энергии связи в молекулах Zn2, Cd2 и Hg2. Изобразим распределение электронов в
- 22. Гомоядерные связи имеются естественно не только в двухатомных молекулах. Мы уже рассматривали молекулу О2. Связь в
- 23. Но гораздо большее количество связей образованы атомами различных элементов. Такие связи называются гетерополярными и мы теперь
- 24. Вспомним, что для Li2 Do = 25 ккал/моль, а для Н2 Do = 108 ккал/моль. Очевидно,
- 25. Откуда же взялись эти избыточные 6 ккал/моль? Происхождение их связано с несимметричным распределением электронной плотности. Она
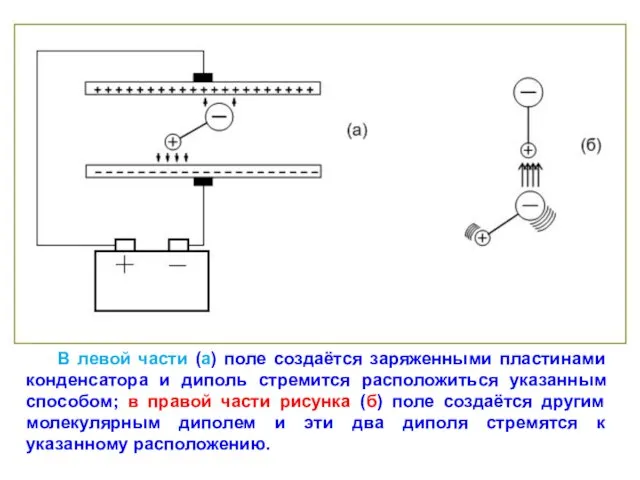
- 26. В левой части (а) поле создаётся заряженными пластинами конденсатора и диполь стремится расположиться указанным способом; в
- 27. Такая реакция – стремление расположиться наиболее выгодным образом позволяет нам измерить величину электрического диполя. Величина ориентирующего
- 28. Итак, связь Li – H имеет дипольный момент. В этом случае мы говорим, что связь имеет
- 29. При этом можно считать, что на всю длину связи r0 от одного атома к другому смещена
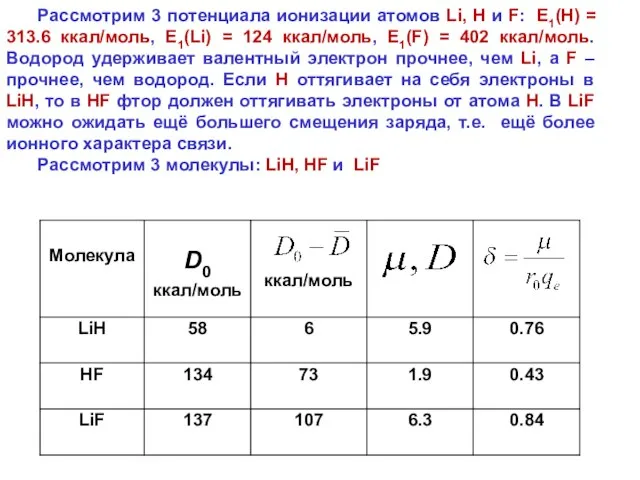
- 30. Рассмотрим 3 потенциала ионизации атомов Li, H и F: E1(H) = 313.6 ккал/моль, E1(Li) = 124
- 31. Симметричное распределение электронов не вызывает смещения заряда и поэтому δ = 0 и ионный характер связи
- 32. ГЕОМЕТРИЯ И ДИПОЛЬНЫЕ СВОЙСТВА МОЛЕКУЛ Оказывается, что химические свойства молекул почти так же сильно зависят от
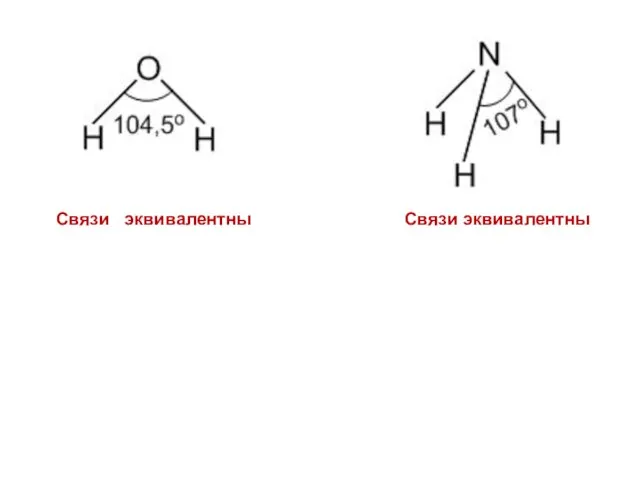
- 33. Под геометрией молекулы подразумеваются величины углов между связями в ней и её форма. Рассмотрим молекулы Н2О
- 34. Связи эквивалентны Связи эквивалентны
- 35. ГИБРИДИЗАЦИЯ СВЯЗЕЙ Рассмотрим молекулу (радикал) СН2. Эта молекула весьма устойчива, но чрезвычайно реакционноспособна. Вы помните, мы
- 36. Теперь у атома С остаются ещё 2 неспаренных электрона: по одному на 2py и 2pz орбиталях.
- 37. Эти три гибридные орбитали расположены в одной плоскости.
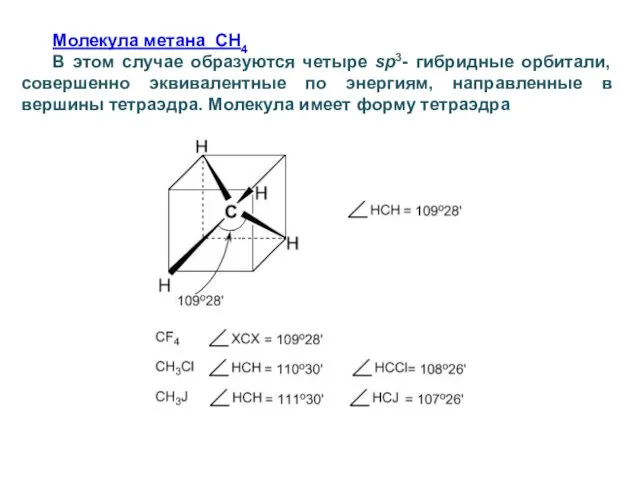
- 38. Молекула метана СН4 В этом случае образуются четыре sp3- гибридные орбитали, совершенно эквивалентные по энергиям, направленные
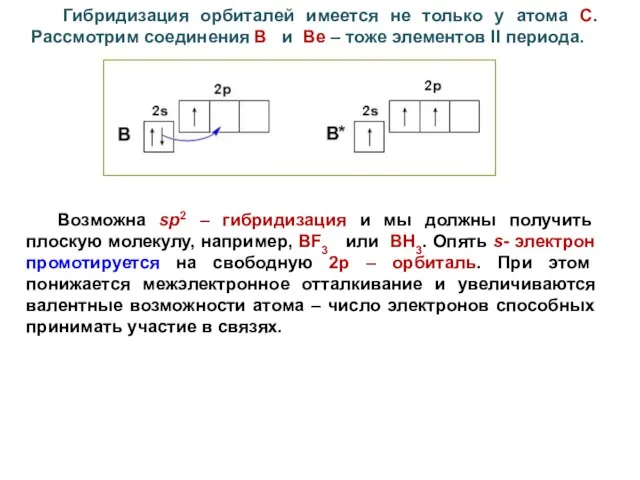
- 39. Гибридизация орбиталей имеется не только у атома С. Рассмотрим соединения В и Ве – тоже элементов
- 40. Но ВН3 отличается от BF3 принципиально. В ВН3 валентная 2pz – орбиталь В остаётся пустой. Она
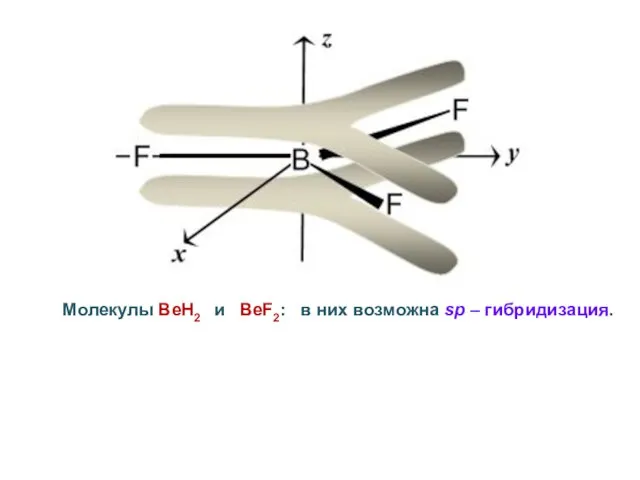
- 41. Молекулы BeH2 и BeF2: в них возможна sp – гибридизация.
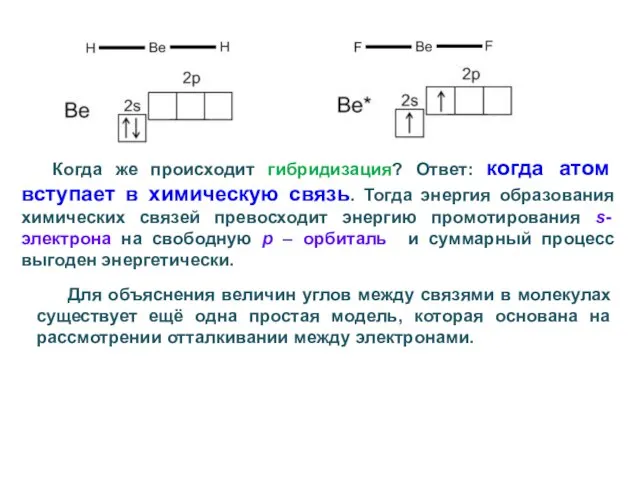
- 42. Когда же происходит гибридизация? Ответ: когда атом вступает в химическую связь. Тогда энергия образования химических связей
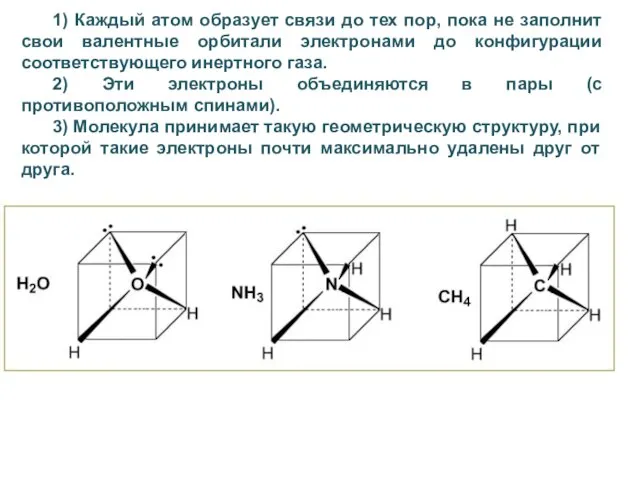
- 43. 1) Каждый атом образует связи до тех пор, пока не заполнит свои валентные орбитали электронами до
- 44. Вспомним, что если ковалентная связь образована между 2-мя атомами разных элементов, то она является гетерополярной, т.е.
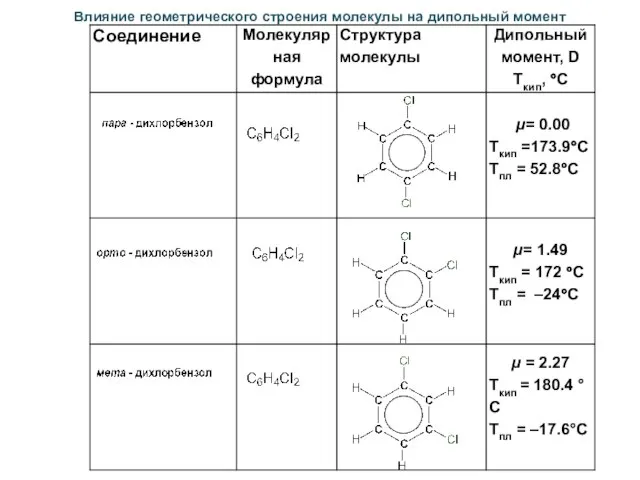
- 45. Влияние геометрического строения молекулы на дипольный момент
- 47. Как же определить, на каком из атомов, образующих связь какой избыточный заряд находится? Для этого служит
- 48. где ro – длина связи, qe –заряд электрона. Эта гипотетическая величина δ представляет собой некоторую часть
- 49. По данным таблицы находим: Таким образом, 1) связь Mg – O более полярна, т.е. характеризуется большей
- 50. ДОНОРНО - АКЦЕПТОРНЫЕ СВЯЗИ Независимо от степени ионности ковалентные связи образуются только при сближении двух атомов,
- 51. Мы уже видели такие примеры: СН2, который вступает в реакцию едва ли не при первом же
- 52. В обоих случаях возможно дальнейшее понижение энергии, если только электроны смогут занять эту рz – орбиталь,
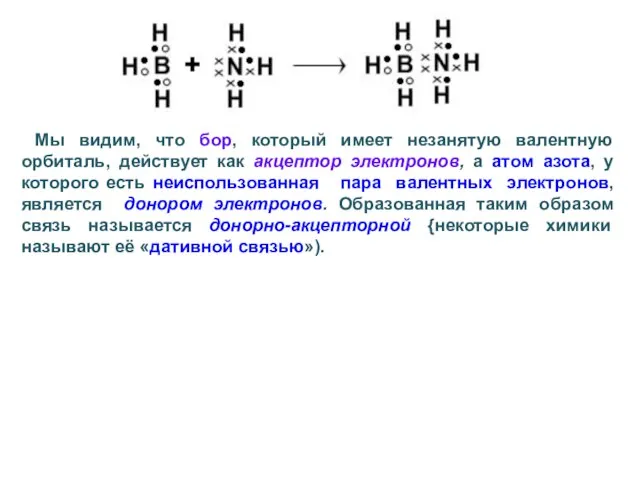
- 53. После образования трех связей с атомами водорода у азота на валентной орбитали остается еще одна пара
- 54. Мы видим, что бор, который имеет незанятую валентную орбиталь, действует как акцептор электронов, а атом азота,
- 55. Свойства некоторых соединений ВН3, с донорно-акцепторными связями достаточно хорошо изучены, хотя сам ВН3 еще не получен.
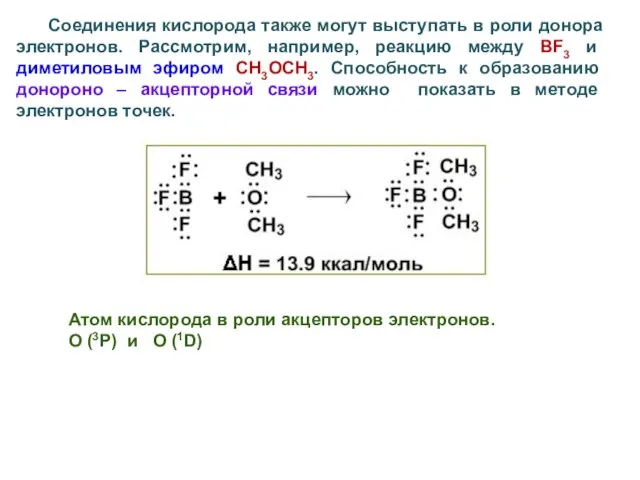
- 56. Соединения кислорода также могут выступать в роли донора электронов. Рассмотрим, например, реакцию между ВF3 и диметиловым
- 59. Скачать презентацию









































 Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура
Термическая обработка. Превращения в стали при нагревании. Перегрев и пережег стали. Видманштеттовая струкрура Викторина по химии
Викторина по химии Алканы. Гомологический ряд
Алканы. Гомологический ряд Презентация по химии Химические уравнения Реакции обмена
Презентация по химии Химические уравнения Реакции обмена  Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Минералы и горные породы
Минералы и горные породы Сложные вещества Выполнил ученик 8 класса КГООУ «Железногорская санаторно-лесная школа» Москальчук Павел Учитель химии и биол
Сложные вещества Выполнил ученик 8 класса КГООУ «Железногорская санаторно-лесная школа» Москальчук Павел Учитель химии и биол История возникновения химии
История возникновения химии Основные понятия, классификация, структура и свойства полимеров. (Лекция 1)
Основные понятия, классификация, структура и свойства полимеров. (Лекция 1) Мыло ручной работы Подготовила ученицы 11 класса Хахалева Юлия
Мыло ручной работы Подготовила ученицы 11 класса Хахалева Юлия  Урок в 8 классе
Урок в 8 классе Белки. Свойства белков. (Тема 2)
Белки. Свойства белков. (Тема 2) Металлы в живой приподе
Металлы в живой приподе Основы электрохимии
Основы электрохимии Разработка реактора для отопления домов путем извлечения водорода из воды
Разработка реактора для отопления домов путем извлечения водорода из воды Химия нефти и газа
Химия нефти и газа Основные характеристики клеев
Основные характеристики клеев Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Профилактика интоксикаций медьсодержащими веществами
Профилактика интоксикаций медьсодержащими веществами Процесс электролиза
Процесс электролиза Гетероциклічні ароматичні сполуки
Гетероциклічні ароматичні сполуки Коррозия металлов
Коррозия металлов Кислоты. Классификация. Способы получения
Кислоты. Классификация. Способы получения Симметрия кристаллических решеток
Симметрия кристаллических решеток Липиды омыляемые и неомыляемые
Липиды омыляемые и неомыляемые Химия функциональных материалов. Адсорбционные материалы. Цеолиты
Химия функциональных материалов. Адсорбционные материалы. Цеолиты Классификация методов аналитической химии
Классификация методов аналитической химии Амфотерность. Амфотерные соединения
Амфотерность. Амфотерные соединения