Содержание
- 2. Коррозия - это самопроизвольный процесс разрушения металлов и сплавов в результате окислительно-восстановитель-ного (химического, электрохимического и биологического)
- 3. Коррозия протекает с уменьшением энергии Гиббса: Меn+ + nе- → Мео (ΔG > O) металлургия Мео
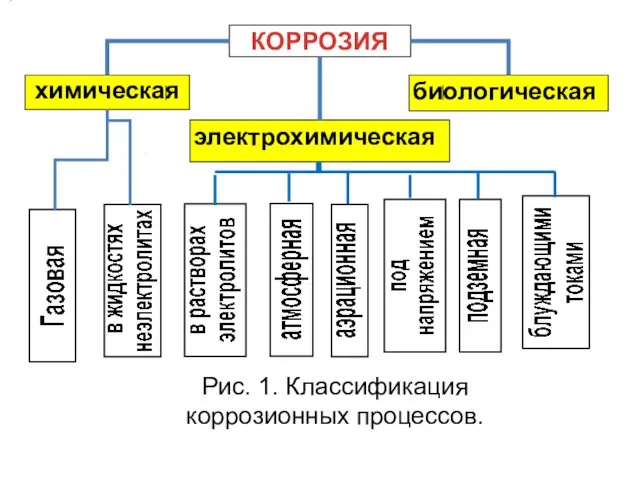
- 4. КОРРОЗИЯ химическая электрохимическая биологическая Рис. 1. Классификация коррозионных процессов.
- 5. - зона коррозии - кристаллиты 1- равномерная 2 - селективная 3 - точечная (питинг) 5-межкристаллитная 6-транскристаллитная
- 7. ХИМИЧЕСКАЯ КОРРОЗИЯ Химическая коррозия - это самопроизвольное разрушение металлов под действием окислителей-неэлектролитов, обычно газов и органических
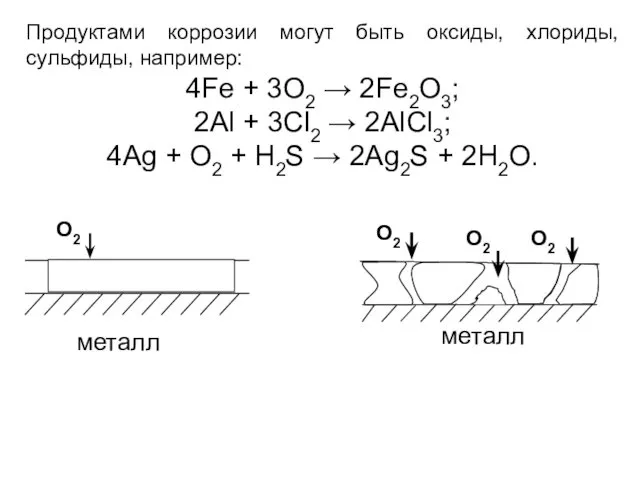
- 8. Продуктами коррозии могут быть оксиды, хлориды, сульфиды, например: 4Fe + 3O2 → 2Fe2O3; 2Al + 3Cl2
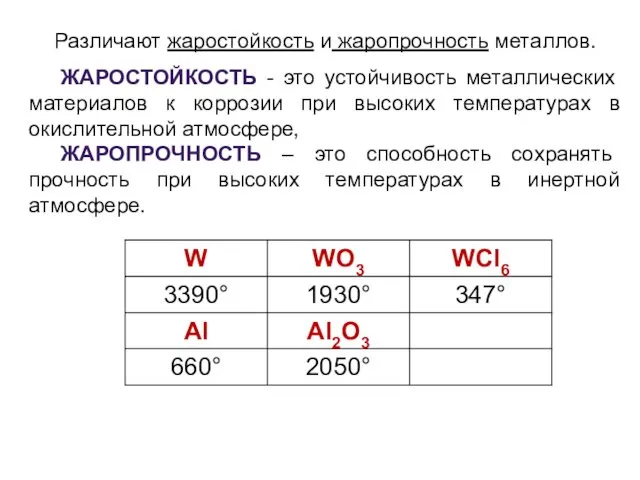
- 9. Различают жаростойкость и жаропрочность металлов. ЖАРОСТОЙКОСТЬ - это устойчивость металлических материалов к коррозии при высоких температурах
- 10. КОРРОЗИЯ В ЖИДКОСТЯХ - НЕЭЛЕКТРОЛИТАХ. К неэлектролитам (непроводящим электрический ток) относятся жидкости органического происхождения - спирт,
- 11. ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ Эл.хим.коррозия возникает при соприкосновении металла с электропроводящей средой (водой, водными растворами солей, кислот, щелочей;
- 12. В общем случае причиной образования короткозамкнутых микрогальванических элементов может служить не только наличие примесей в металле,
- 13. На аноде происходит окисление и растворение металла по схеме: (−)А: Me0 – nе- → Me n+
- 14. ВОДОРОДНАЯ ДЕПОЛЯРИЗАЦИЯ сопровождается восстановлением на катодных участках водорода. в кислой среде: (+)К: 2Н+ + 2е- =
- 15. при водородной деполяризации электрохимической коррозии могут подвергаться металлы с электродным потенциалом более отрицательным, чем у водородного
- 16. МЕХАНИЗМЫ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ При электрохимической коррозии металлов выделяют четыре механизма, вызывающих образование и работу короткозамкнутых микрогальванических
- 17. К[Cu]: 2Н+ + 2e- → Н2 А: Fe0- 2e-→Fe2+ 4Fe(OH)2 + 2H2O + O2 → 4Fe(OH)3
- 18. 2. КОНТАКТ С ПРОДУКТОМ КОРРОЗИИ. Fe(OH)2 Раствор Анод (–) Fe Катод (+) -e¯ Fe(OH)2 H2↑ А:
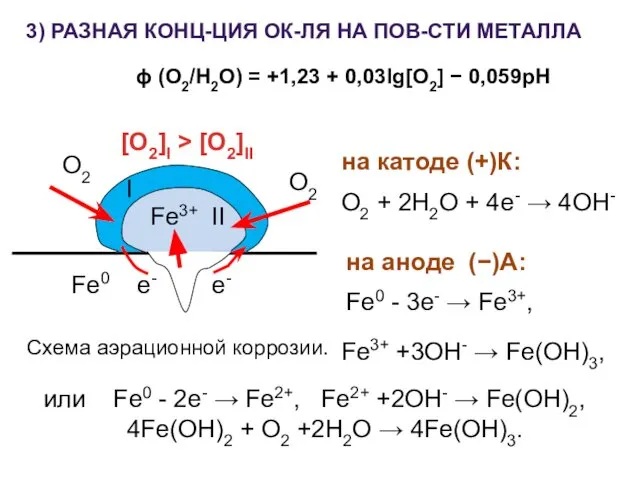
- 19. или Fe0 - 2e- → Fe2+, Fe2+ +2OH- → Fe(OH)2, 4Fe(OH)2 + O2 +2H2O → 4Fe(OH)3.
- 20. 4. КОРРОЗИЯ ПОД МЕХ. НАПРЯЖЕНИЕМ. Статические напряжения могут понижать термодинамическую устойчивость металла, разрушать защитные пленки. При
- 21. растяжение сжатие 4. Коррозия под механ. напряжением ножевая или транскристаллитная коррозия φсжат > φрастяж на аноде
- 22. ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ легирование металлов защитные покрытия электрохимичес-кая защита обработка коррозионной среды металлические неметалли-ческие химические
- 23. Катодное покрытие - это покрытие более активного металла менее активным. Пример: железо, покрытое оловом (луженое железо).
- 24. Анодное покрытие - это покрытие менее активного металла более активным, например, железо - цинком (оцинкованное железо)
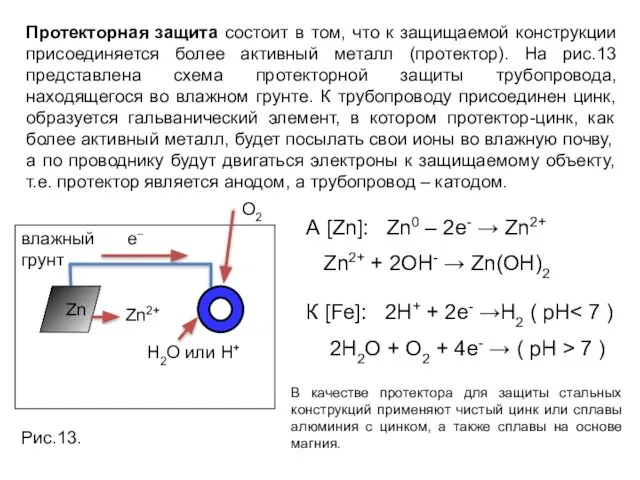
- 25. Протекторная защита состоит в том, что к защищаемой конструкции присоединяется более активный металл (протектор). На рис.13
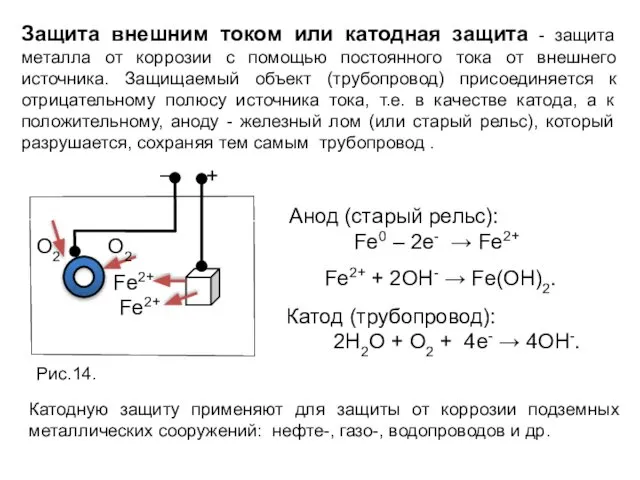
- 26. Защита внешним током или катодная защита - защита металла от коррозии с помощью постоянного тока от
- 27. КЛАССИФИКАЦИЯ КОРРОЗИОННЫХ ПРОЦЕССОВ Коррозионные процессы чрезвычайно многообразны и их классификация проводится по разным признакам. По механизму
- 30. Скачать презентацию












![К[Cu]: 2Н+ + 2e- → Н2 А: Fe0- 2e-→Fe2+ 4Fe(OH)2 +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/471258/slide-16.jpg)








 Акриловые волокна
Акриловые волокна Химические реакции
Химические реакции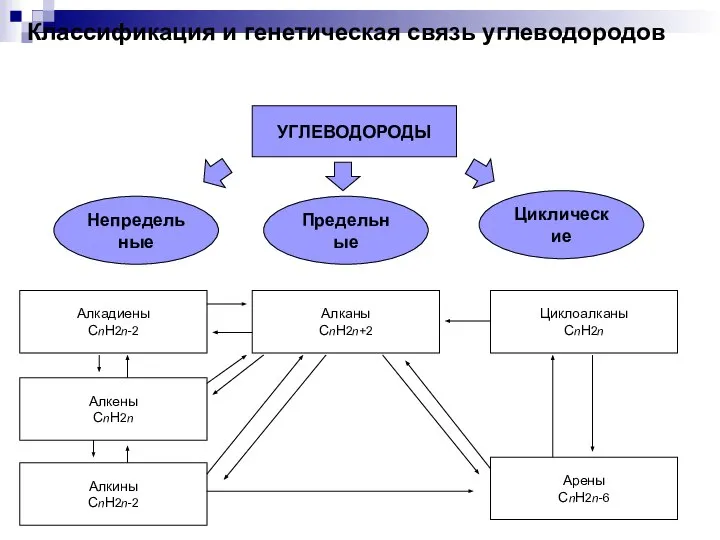 Классификация и генетическая связь углеводородов
Классификация и генетическая связь углеводородов Дипломная работа. Тема: Получение гальванических покрытий на основе цинка
Дипломная работа. Тема: Получение гальванических покрытий на основе цинка ПРИРОДНЫЕ И ПОПУТНЫЕ ГАЗЫ.
ПРИРОДНЫЕ И ПОПУТНЫЕ ГАЗЫ. Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О
Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О Получение полимеров из низкомолекулярных соединений
Получение полимеров из низкомолекулярных соединений Карбон Характеристика елемента та утворених ним сполук, кругообіг елемента в природі
Карбон Характеристика елемента та утворених ним сполук, кругообіг елемента в природі  Химические формулы. Классы неорганических веществ. Урок №1
Химические формулы. Классы неорганических веществ. Урок №1 Геохимия урана и тория в карбонатитовом процессе
Геохимия урана и тория в карбонатитовом процессе Горение и медленное окисление. Тепловой эффект химической реакции
Горение и медленное окисление. Тепловой эффект химической реакции Галогены. Межгалогенные соединения
Галогены. Межгалогенные соединения Способы переработки нефти
Способы переработки нефти Свойство воды, устранение жесткости воды и очистка воды
Свойство воды, устранение жесткости воды и очистка воды 1. Взаємодія неметалів з металами: 1. Взаємодія неметалів з металами: а) Сu0 + Cl20 = Сu+2 Cl2-1 – купрум (ІІ) хлорид Сu0 – 2e-→ Сu+2 2 Cl20 + 2(1e-) → Cl2−1 2 б) Fe0 + Cl20 = Fe+3 Cl3-1 – ферум
1. Взаємодія неметалів з металами: 1. Взаємодія неметалів з металами: а) Сu0 + Cl20 = Сu+2 Cl2-1 – купрум (ІІ) хлорид Сu0 – 2e-→ Сu+2 2 Cl20 + 2(1e-) → Cl2−1 2 б) Fe0 + Cl20 = Fe+3 Cl3-1 – ферум Изучение геохимических свойств редкоземельных элементов
Изучение геохимических свойств редкоземельных элементов Physics and chemistry of surface phenomena
Physics and chemistry of surface phenomena Классы неорганических веществ. Оксиды. Кислоты
Классы неорганических веществ. Оксиды. Кислоты Строение атома
Строение атома Значение органической химии в жизни людей
Значение органической химии в жизни людей Химическая посуда
Химическая посуда Технология коллоидов и наносистем. Лекция 4. Физико-химические основы нуклеации и технологии формирования новой фазы
Технология коллоидов и наносистем. Лекция 4. Физико-химические основы нуклеации и технологии формирования новой фазы Химический эквивалент. Значение растворов в жизнедеятельности организмов. Способы выражения состава растворов
Химический эквивалент. Значение растворов в жизнедеятельности организмов. Способы выражения состава растворов Буферные системы
Буферные системы Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Водород- зеленое топливо
Водород- зеленое топливо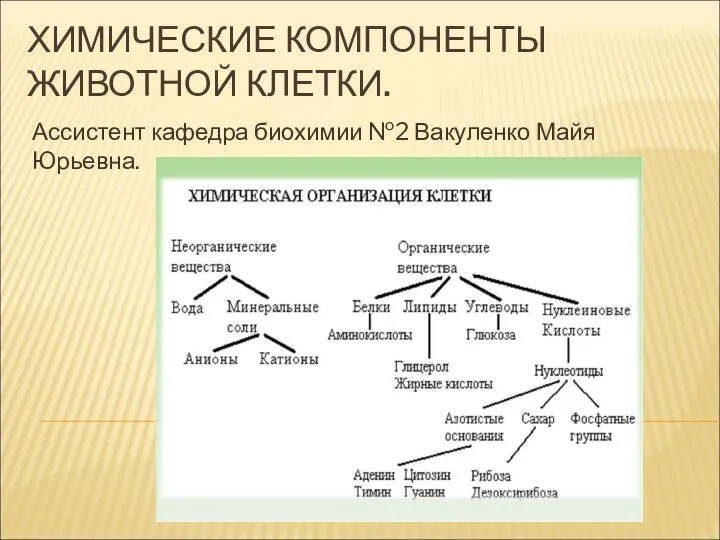 Химические компоненты животной клетки
Химические компоненты животной клетки