Содержание
- 2. Почему? минимуму энергии системы соответствует максимум устойчивости и, наоборот, минимуму устойчивости отвечает максимум энергии» Атом 1
- 3. Химическая связь… ХИМИЧЕСКАЯ СВЯЗЬ это взаимодействие атомов, обусловленное перекрыванием их электронных облаков и сопровождающееся уменьшением полной
- 4. Химическая связь Ядерно-электронные взаимодействия способствуют образованию химической связи Межэлектронные взаимодействия а) притяжение электронов с антипараллельными спинами
- 5. Химическая связь r0 – расстояние между атомами в молекуле E0 – энергия связи В 1927 году
- 6. Химическая связь Длина связи (r) – межъядерное расстояние взаимодействующих атомов Зависит от размеров электронных оболочек и
- 7. ИОННАЯ СВЯЗЬ КОВАЛЕНТНАЯ СВЯЗЬ МЕТАЛЛИЧЕСКАЯ СВЯЗЬ ПОЛЯРНАЯ СВЯЗЬ ДЕЛОКАЛИЗОВАННАЯ СВЯЗЬ Межмолекулярные связи отличаются значительно меньшей прочностью
- 8. Теории химической связи Метод валентных связей (ВС) Метод молекулярных орбиталей (ММО) Представления о многоцентровых делокализованных связях
- 9. Метод валентных связей Химическая связь между атомами образуется в результате обобществления валентных электронов, т.е. образования общих
- 10. Метод валентных связей Ковалентность элемента или его спинвалентность определяется числом неспаренных валентных электронов в основном и
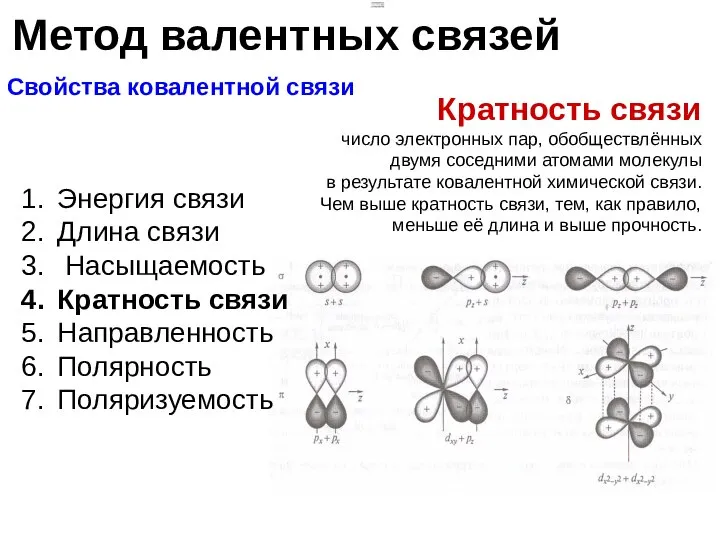
- 11. Метод валентных связей Свойства ковалентной связи Энергия связи Длина связи Насыщаемость Кратность связи Направленность Полярность Поляризуемость
- 12. Метод валентных связей Свойства ковалентной связи Энергия связи Длина связи Насыщаемость Кратность связи Направленность Полярность Поляризуемость
- 13. Метод валентных связей Свойства ковалентной связи Энергия связи Длина связи Кратность связи Насыщаемость Направленность Полярность Поляризуемость
- 14. Свойства ковалентной связи Направленность
- 15. Энергия связи Длина связи Кратность связи Насыщаемость Направленность Полярность Поляризуемость Полярность определяется степенью перекрывания орбиталей Свойства
- 16. Полярность Свойства ковалентной связи Степень ионности связи + - H Cl Смещение электронной плотности к более
- 17. Полярность Свойства ковалентной связи Дипольный момент связи (μ) l – длина связи q – эффективный заряд
- 18. Поляризуемость или динамическая поляризация Свойства ковалентной связи – это способность электронной оболочки атома или молекулы деформироваться
- 19. Метод молекулярных орбиталей ОСНОВНЫЕ ПОЛОЖЕНИЯ При образовании молекулы по ММО изменяют своё состояние не только валентные
- 20. Метод молекулярных орбиталей ОСНОВНЫЕ ПОЛОЖЕНИЯ Для получения МО используют метод линейной комбинации атомных орбиталей МЛКАО. Из
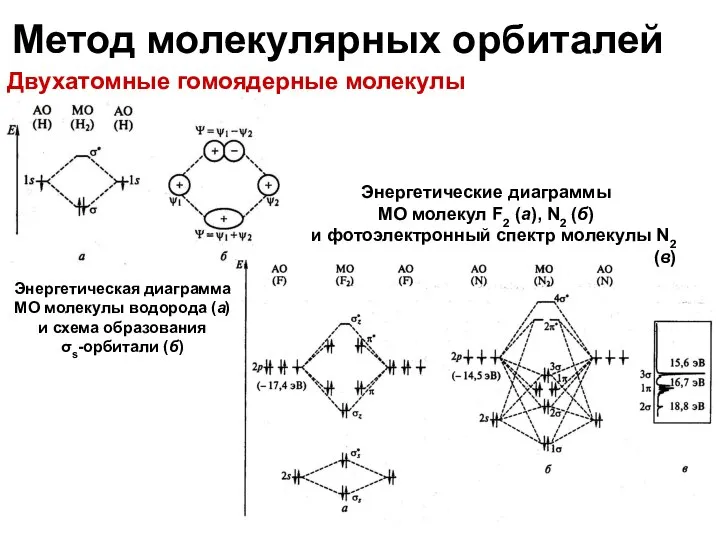
- 21. Метод молекулярных орбиталей Двухатомные гомоядерные молекулы Энергетические диаграммы МО молекул F2 (а), N2 (б) и фотоэлектронный
- 22. Метод молекулярных орбиталей Гетероядерные двухатомные молекулы Энергетические диаграммы МО молекул HF (а), LiH (б)
- 23. Метод молекулярных орбиталей Какую информацию можно извлечь из энергетических диаграмм МО? Прочность молекул – определяется выигрышем
- 24. Теории химической связи
- 25. Теории химической связи достоинства: Метод Валентных связей не рассматривает вклад неспаренных электронов в образование связи (природу
- 26. Теории химической связи достоинства: Метод Молекулярных орбиталей общий подход при описании всех химических соединений недостатки: не
- 27. Ионная связь При взаимодействии наиболее электроотрицательных атомов с наиболее электроположительными образуется связь с большой степенью полярности
- 28. Ионная связь Пространственное расположение ионов Координационное число (число ближайших соседей) – определяется относительными размерами аниона и
- 29. Ионная связь Электронная структура Схема энергетической диаграммы МО молекулы NaCl (а), энергетических зон (б) и рентгеноэлектронного
- 30. Металлическая связь Металлической обычно называют связь между атомами металлов в твердом состоянии Схема энергетических зон (а)
- 31. Комплексные соединения химические вещества, в состав которых входят комплексные частицы Комплексная частица — сложная химическая частица,
- 32. Комплексные соединения Дентатность лиганда определяется числом координационных мест, занимаемых лигандом в координационной сфере комплексообразователя Координационный полиэдр
- 33. Комплексные соединения По заряду комплекса 1) Катионные комплексы образованы в результате координации вокруг положительного иона нейтральных
- 34. Комплексные соединения По числу мест, занимаемых лигандами в координационной сфере 1) Монодентатные лиганды. Такие лиганды бывают
- 35. Комплексные соединения По природе лиганда 1) Аммиакаты — комплексы, в которых лигандами служат молекулы аммиака, например:
- 36. Кристаллическое строение Кристаллические решётки веществ – это упорядоченное расположение частиц (атомов, молекул, ионов) в строго определённых
- 37. Типы кристаллических решеток Тип химической связи Атомная Молекулярная Ионная Металлическая Свойства кристаллов определяются особенностями строящих кристаллическую
- 38. Кристаллическое строение Типы (сингонии) кристаллических решеток кубическая a=b=c, α=β=γ=90° тетрагональная a=b ≠c, α=β=γ=90° гексагональная a=b ≠c,
- 39. Кристаллическое строение Типы элементарных ячеек кристаллических решеток металлов и схемы упаковки в них атомов гранецентрированная кубическая
- 40. Реальные кристаллы дефекты кристаллической решетки или дефектное строение кристалла условия минералоообразования (Т, Р, геометрия полостей, в
- 41. Реальные кристаллы Ориентировка кристаллических решеток
- 42. Дефекты строения ТОЧЕЧНЫЕ ДЕФЕКТЫ К точечным дефектам относятся: а) свободные места в узлах кристаллической решетки —
- 43. Дефекты строения ЛИНЕЙНЫЕ ДЕФЕКТЫ Линейные дефекты характеризуются малыми размерами в двух измерениях, но имеют значительную протяженность
- 45. Скачать презентацию








































 Презентация по Химии "Разнообразие веществ" - скачать смотреть
Презентация по Химии "Разнообразие веществ" - скачать смотреть  Нафта та продукти нафтопереробки
Нафта та продукти нафтопереробки  Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури
Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури Алканы «Гексан»
Алканы «Гексан» ИЗ ОПЫТА ИСПОЛЬЗОВАНИЯ ИНТЕРАКТИВНОЙ ДОСКИ НА УРОКАХ ХИМИИ.
ИЗ ОПЫТА ИСПОЛЬЗОВАНИЯ ИНТЕРАКТИВНОЙ ДОСКИ НА УРОКАХ ХИМИИ. Применение наноматериалов
Применение наноматериалов Структура кристаллических полимеров
Структура кристаллических полимеров Решение 33 задания
Решение 33 задания Корреляция структуры ксенобиотика и его токсичности. Топологические индексы
Корреляция структуры ксенобиотика и его токсичности. Топологические индексы Предельные углеводороды
Предельные углеводороды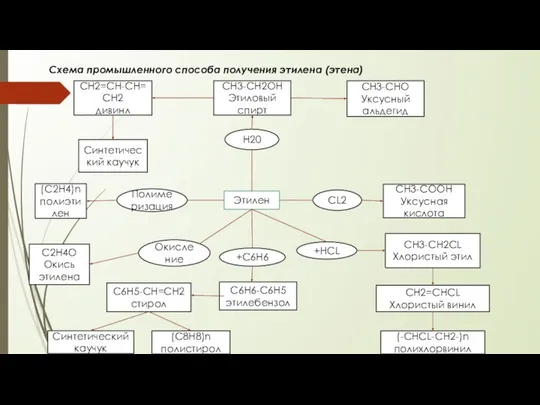 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена) Алюминий и его соединения
Алюминий и его соединения Химические знаки
Химические знаки Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Застосуваня електролізу
Застосуваня електролізу Пластмассы в автомобилестроении
Пластмассы в автомобилестроении Презентация по Химии "КОРРОЗИЯ МЕТАЛЛОВ" - скачать смотреть бесплатно
Презентация по Химии "КОРРОЗИЯ МЕТАЛЛОВ" - скачать смотреть бесплатно Соли. Классификация солей. Способы получения. Физические и химические свойства
Соли. Классификация солей. Способы получения. Физические и химические свойства Презентация по Химии "ПЛАСТМАССА" - скачать смотреть
Презентация по Химии "ПЛАСТМАССА" - скачать смотреть  Химия. D-элементтер
Химия. D-элементтер Гетероциклические соединения
Гетероциклические соединения Презентация по Химии "Знаки химических элементов" - скачать смотреть
Презентация по Химии "Знаки химических элементов" - скачать смотреть  Необычные минералы
Необычные минералы Алюміній: будова атома, поширення в природі. Фізичні і хімічні властивості алюмінію. Застосування алюмінію Підготував
Алюміній: будова атома, поширення в природі. Фізичні і хімічні властивості алюмінію. Застосування алюмінію Підготував  Технология адсорбционной осушки газа
Технология адсорбционной осушки газа Химия и современный быт человека
Химия и современный быт человека Фуллерены Квазикристаллы Использование кристаллов
Фуллерены Квазикристаллы Использование кристаллов Ток в жидкостях. Закон электролиза. Гальваностегия. Гальванопластика
Ток в жидкостях. Закон электролиза. Гальваностегия. Гальванопластика