Содержание
- 2. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
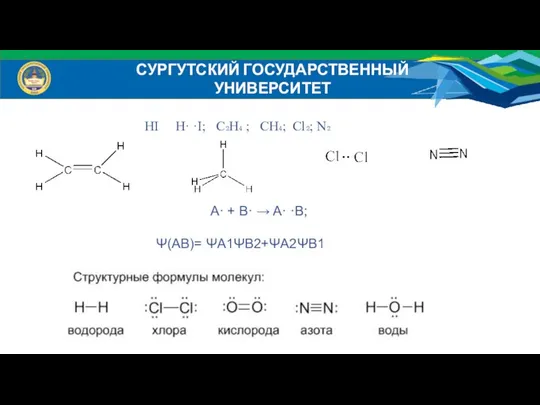
- 3. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ HI H· ·I; C₂H₄ ; CH₄; Cl₂; N₂ А· + В· → А·
- 4. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Термин «химическое строение» введено А.М. Бутлеровым в 1861 году. Также он заложил основы
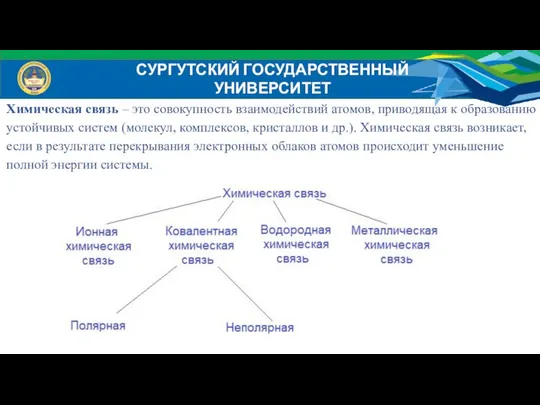
- 5. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Химическая связь – это совокупность взаимодействий атомов, приводящая к образованию устойчивых систем (молекул,
- 6. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Ионная химическая связь – это связь, образовавшаяся за счет электростатического притяжения катионов (положительно
- 7. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Физические свойства веществ с ионной кристаллической решеткой: тугоплавкие; Нелетучие; Твердые, но хрупкие; Многие
- 8. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Ковалентная связь - это связь между атомами, возникающая за счет образования общих электронных
- 9. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 10. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Число общих электронных пар равно числу связей между двумя атомами, или кратности связи.
- 11. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Параметры ковалентной связи: 1. Направленность – это такое размещение электронной плотности между атомами,
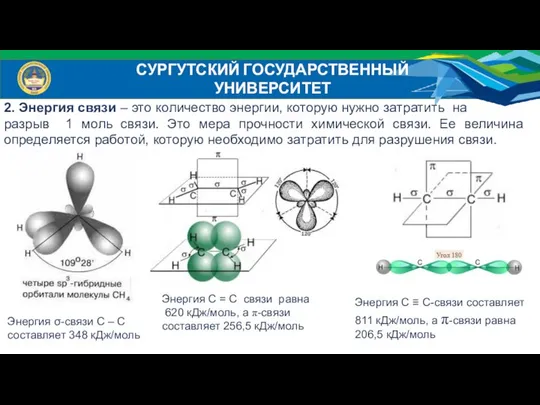
- 12. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ 2. Энергия связи – это количество энергии, которую нужно затратить на разрыв 1
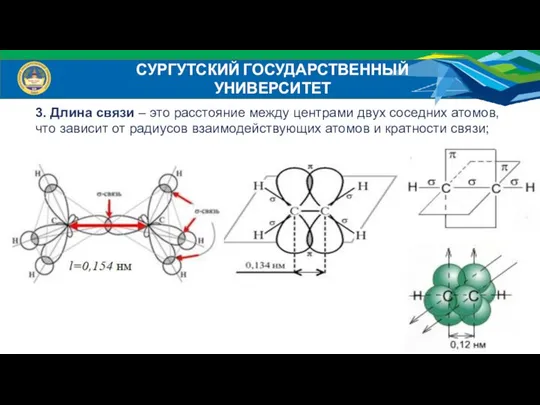
- 13. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ 3. Длина связи – это расстояние между центрами двух соседних атомов, что зависит
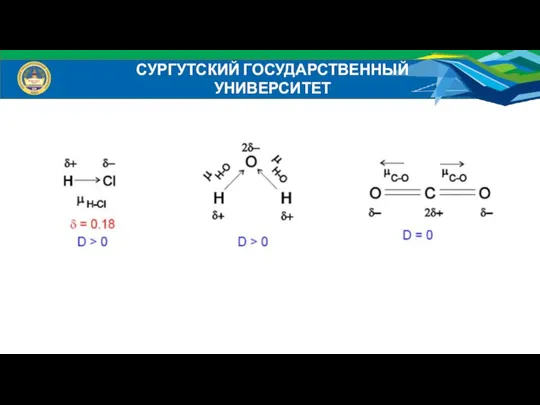
- 14. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ 4. Полярность связи – неравномерное распределение электронной плотности между атомами в молекуле. Когда
- 15. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 16. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Вещества с ковалентной связью при обычных условиях бывают: 1. Газами; 2. Жидкостями; 3.
- 17. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ При кристаллизации веществ с ковалентной связью, образуются вещества с атомной кристаллической решеткой, в
- 18. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Молекулярную кристаллическую решётку имеют также вещества с ковалентными полярными связями: вода — лёд,
- 19. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Металлическая связь В узлах кристаллической решетки находятся катионы металла, а в межузлиях электронный
- 20. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Водородная химическая связь – это электростатическое притяжение между сильно электроотрицательными атомами (F, O,
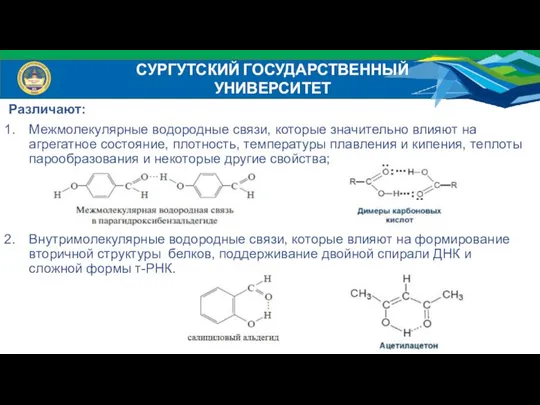
- 21. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Различают: Межмолекулярные водородные связи, которые значительно влияют на агрегатное состояние, плотность, температуры плавления
- 22. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Резких границ между разными видами химических связей нет, все типы химической связи имеют
- 23. Метод валентных связей (МВС) или теория локализованных электронных пар Преимущества принципа локализованных связей: Наглядность; Предсказывает валентные
- 24. Основные положения теории гибридизации: 1. Введение гибридных орбиталей служит для описания направленных локализованных связей. Гибридные орбитали
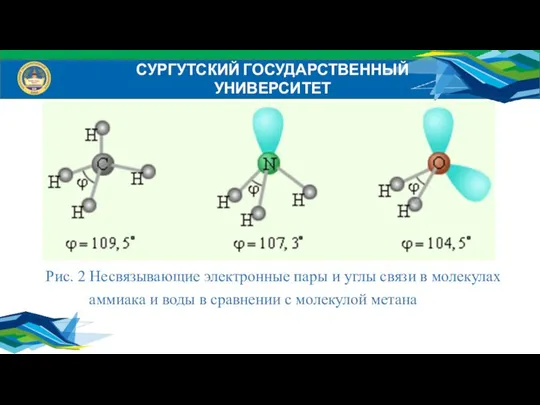
- 25. Рис. 2 Несвязывающие электронные пары и углы связи в молекулах аммиака и воды в сравнении с
- 26. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 27. Распределение электронов в пространстве описывается вероятностью нахождения электрона в определенном месте атомного пространства: Вероятность заполнения связующих
- 28. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Метод молекулярных орбиталей как линейная комбинация атомных орбиталей
- 29. Основные положения МО ЛКАО Молекулярные орбитали (МО) образуются при перекрывании атомных орбиталей (АО); Число МО равно
- 30. 5. Заполнение молекулярных орбиталей осуществляется парой электронов в соответствии с принципом наименьшей энергии, принципом Паули и
- 31. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Например: определить существование молекул и частиц и порядок связи в терминах теории молекулярных
- 32. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Например: определить существование молекул и частиц и порядок связи в терминах теории молекулярных
- 33. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 34. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
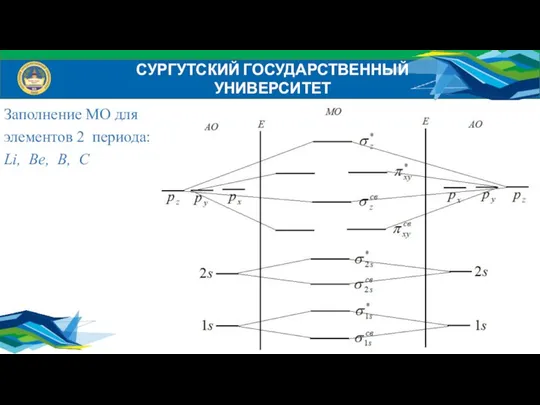
- 35. Заполнение МО для элементов 2 периода: Li, Be, B, C СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
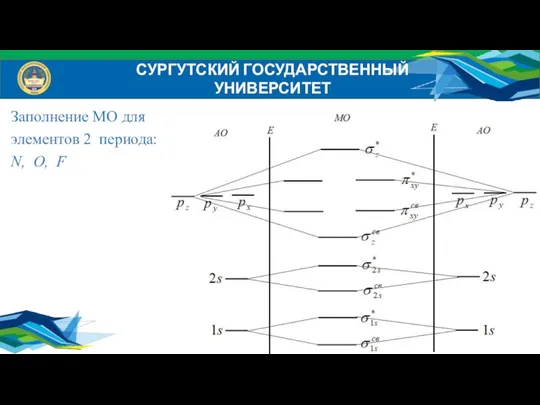
- 36. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Заполнение МО для элементов 2 периода: N, O, F
- 37. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
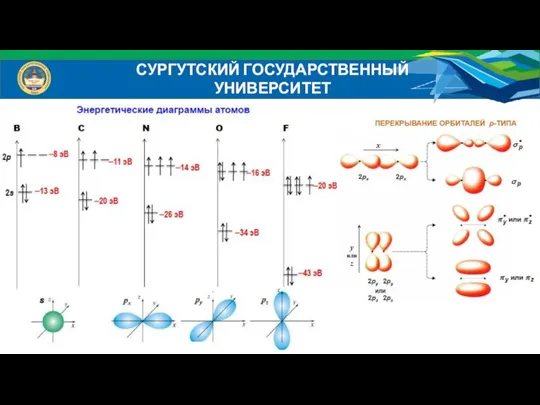
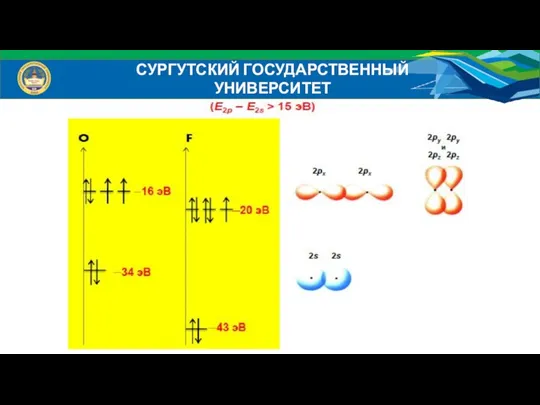
- 38. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Энергетические диаграммы атомов:
- 39. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ Энергетические диаграммы МО гетероядерных молекул Исходные АО дают разный вклад в энергию связующих
- 40. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 41. СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 42. Спасибо за внимание! Вопросы? СУРГУТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
- 44. Скачать презентацию






























 Тайна воды которую мы пьём
Тайна воды которую мы пьём Вещества. Классификация веществ
Вещества. Классификация веществ Ионное уравнения
Ионное уравнения Морские льды. Их классификация и закономерности движения
Морские льды. Их классификация и закономерности движения Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости Білки
Білки 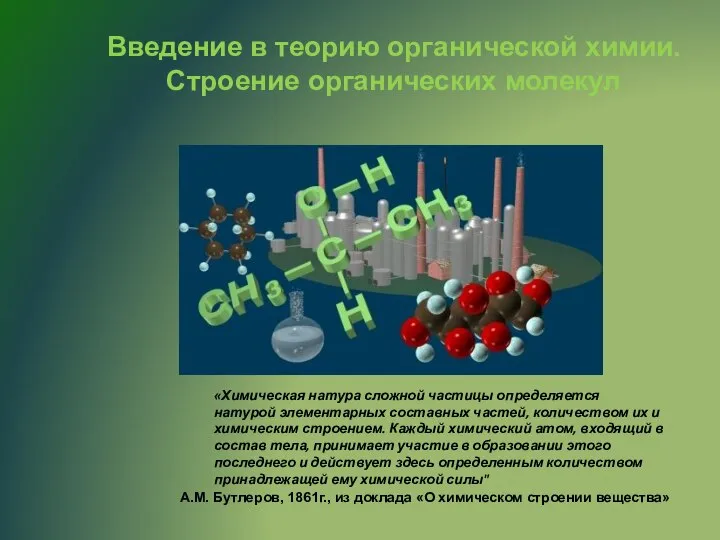 Строение органических молекул. (Лекция 2)
Строение органических молекул. (Лекция 2) Перманганатометрия. Окислительно-восстановительное титрование. (Лекция 8)
Перманганатометрия. Окислительно-восстановительное титрование. (Лекция 8) Номенклатура органических соединений. Структурные формулы соединений. Алканы. (Лабораторная работа 2)
Номенклатура органических соединений. Структурные формулы соединений. Алканы. (Лабораторная работа 2) Электрохимическая коррозии. Катодные процессы электрохимической коррозии
Электрохимическая коррозии. Катодные процессы электрохимической коррозии Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат
Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат Минералы горных пород
Минералы горных пород Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Предельные одноосновные карбоновые кислоты. Сложные эфиры
Предельные одноосновные карбоновые кислоты. Сложные эфиры Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Морфология палочковидных и извитых бактерий. Краски используемые в микробиологии. Приготовление бакпрепаратов. Методы окраски
Морфология палочковидных и извитых бактерий. Краски используемые в микробиологии. Приготовление бакпрепаратов. Методы окраски Полимеры, пластмассы и волокна
Полимеры, пластмассы и волокна Химические реакции
Химические реакции Сульфат меди
Сульфат меди Галлий - металл, который плавится в руке
Галлий - металл, который плавится в руке Качественный анализ молока
Качественный анализ молока Carbohydrate metabolism
Carbohydrate metabolism Мәктәптә-химия атналыгы
Мәктәптә-химия атналыгы Аминокислоты
Аминокислоты Физико-химические свойства крахмала
Физико-химические свойства крахмала Неорганические вещества в структуре питания
Неорганические вещества в структуре питания Благородные металлы
Благородные металлы Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод
Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод