Содержание
- 2. 1.Cm – элементінің атауы 2. S элементінің атауы 3.С элементінің атауы 4.Құрамында металл атомдарымен байланысқан бір
- 5. Күкірт және оның қосылыстары
- 6. І.Ой қозғау (нені білеміз?) Миға шабуыл
- 7. 1.Ерте заманнан бастап, үйді аластауға, түрлі жараларды емдеуге қолданылатын элемент?
- 8. КҮКІРТ
- 9. 2.Сутек пен күкірт әрекеттесе ме? Қандай зат түзіледі?
- 10. Әрекеттеседі, улы газ күкіртті сутек түзіледі
- 11. 3. Күкірттің неше аллотропиялық түр өзгерістері бар?
- 12. ҮШ
- 13. 4. Күкірттің валенттілігі нешеге тең?
- 14. II , IV, VI
- 15. 5. Күкірт қандай тотығу дәрежелерін көрсетеді.
- 16. -2 , +4, +6
- 17. 6. Күкірт қай топта орналасқан?
- 18. VI A - топта
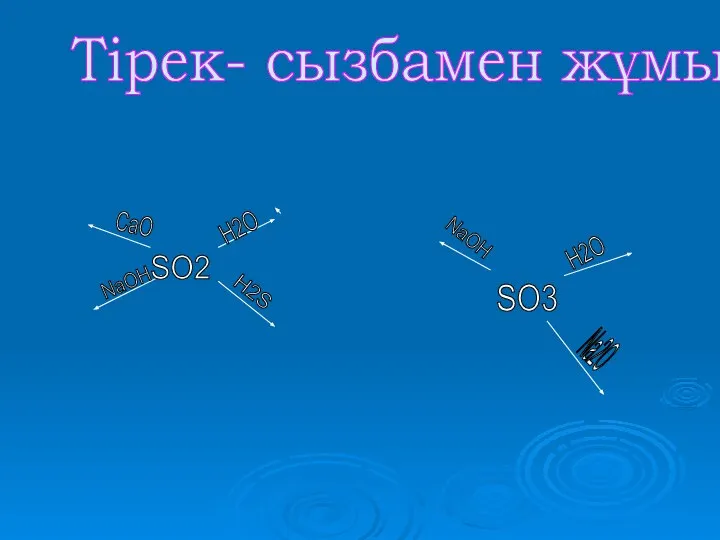
- 19. Тірек- сызбамен жұмыс SO2 H2O H2S NaOH CaO SO3 H2O NaOH Na2O
- 20. ІІ.Қызығуды ояту
- 21. 1.Айналуды жүзеге асыр: S SO2 H2SO3 Na2SO3 SO2
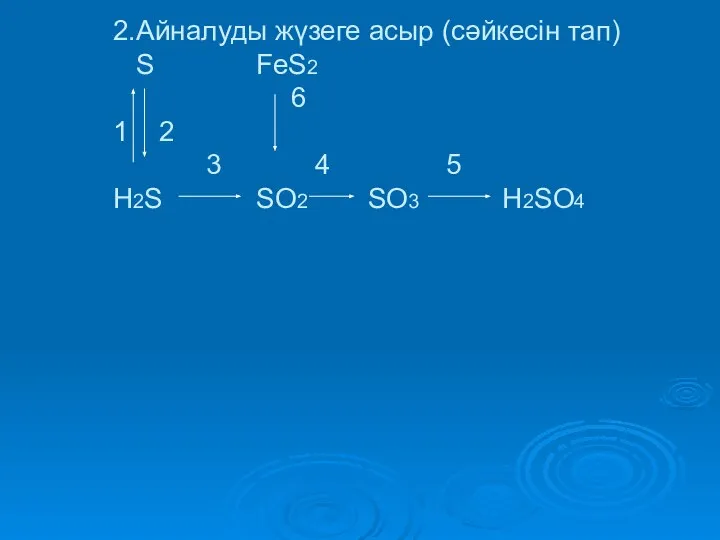
- 22. 2.Айналуды жүзеге асыр (сәйкесін тап) S FeS2 6 1 2 3 4 5 H2S SO2 SO3
- 23. а) H2S S + H2 ә) FeS + 2HCl = FeCl2 + H2S б) S +
- 24. Жауабы:1. а) 2. в) 3. ғ) 4. г) 5. д) 6. ж)
- 25. Кім математик?
- 26. Массасы 20 г Na2SO4 барий хлоридімен әрекеттескенде қанша грамм барий сульфаты тұнбаға түседі?
- 27. Жауабы: m(BaSO4) = 32,8 г
- 28. ІІI.Ой қорыту
- 29. Кестені толтыр 1.Күкіртті қышқыл 7.Май тәрізді сұйықтық 2.Күкірт қышқылы 8.Орта тұздары сульфитер 3.Орташа күші бар 9.Орта
- 31. Венн диаграммасы
- 32. SO2 SO3
- 33. Бейне сұрақ
- 34. ТЕСТ ОРЫНДАУ
- 35. 1.Күкірттің химиялық таңбасы: а) Р, в) Ғ, с) S. 2. Электрондық формуласы: а)2е,8е,3е, в)2е,8е,6е, с)2е,8е,7е. 3
- 36. Жауаптары: 1с 2в 3в 4с 5а 6в 7а 8в 9а 10в
- 37. ІV.Ой дамыту (Шығармашылық жұмыс)
- 38. Күкірт - дәру әрі дерт SO2
- 39. Ғасыр келісімі қалай жасалды? Алматыда 1993 жылы 16 сәуірде ҚР президенті Н. Ә. Назарбаев пен «Шеврон»
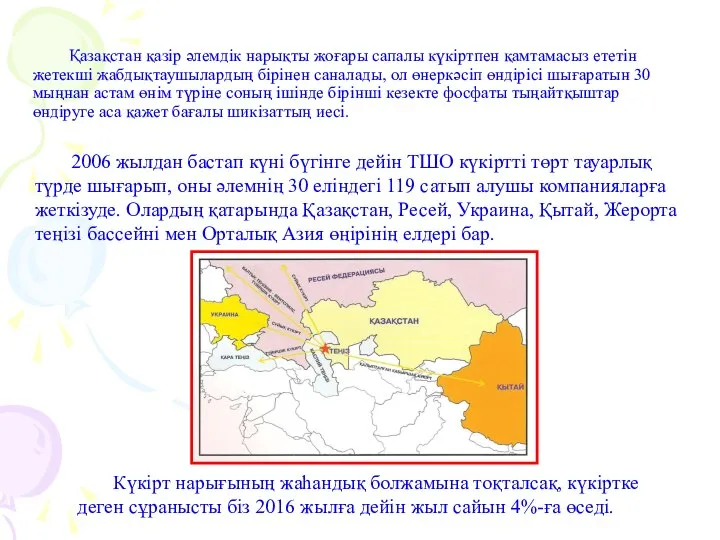
- 40. Қазақстан қазір әлемдік нарықты жоғары сапалы күкіртпен қамтамасыз ететін жетекші жабдықтаушылардың бірінен саналады, ол өнеркәсіп өндірісі
- 41. Түйіршіктелінген күкірт тиеуге, тасымалдауға және тұтынушының пайдалануына тиімді Қабыршақ күкіртті өндіру Сұйық күкіртті темір жол цистерналарына
- 42. Күкірт – дәру Аластау (салт,ырым). «Алас, алас, пәле-жаладан алас» (ел аузынан). Жас отау босағасын, бесікті, жаңа
- 43. Күкірт – дәру
- 44. Күкірттің табиғаттағы биологиялық ролі Күкірт маңызды биогендік элемент болғандықтан, барлық тірі ағзаларда үнемі болады. Өсімдіктер құрамындағы
- 45. Күкірт – дерт SO2 SO2 SO2 SO2 SO2 SO2 SO2 SO2
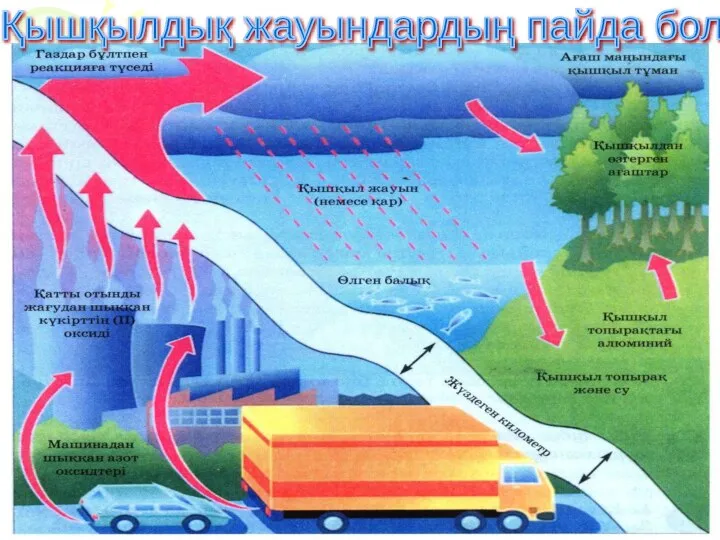
- 46. Қышқылдық жауындардың пайда болуы
- 47. Қорытынды
- 48. V.Үйге тапсырма: 1. Мына қосылыстардағы күкірттің тотығу дәрежесін анықта: K2S H2SO4 SO4 Li2S SO3 2. Мына
- 49. Назарларыңызға рахмет
- 53. Скачать презентацию










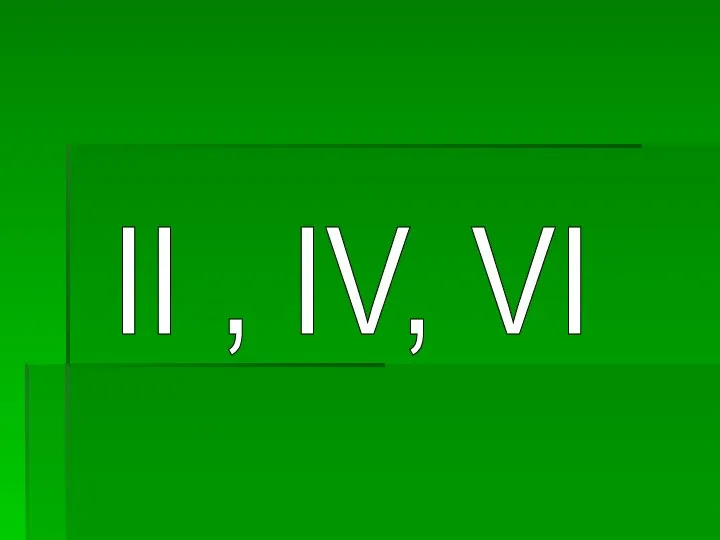

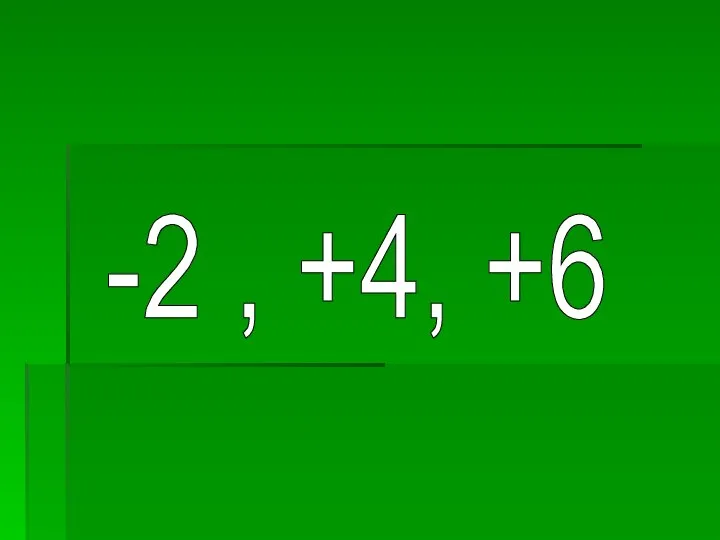































 Кислоты. Номенклатура кислот
Кислоты. Номенклатура кислот Применение этанола
Применение этанола Пластмассы или пластики
Пластмассы или пластики Химия и биохимия игристых вин
Химия и биохимия игристых вин Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер
Күрделі липидтер.Сабынданбайтын липидтер (стериндер, стероидтар) және олардың биологиялық маңызы. Терпендер Поверхностные явления
Поверхностные явления Стекло. Виды стекол
Стекло. Виды стекол ХАРЧОВІ ДОБАВКИ ПІДГОТУВАЛА СОКОЛОВСЬКА АЛЬОНА УЧЕНИЦЯ 8А КЛАСУ КНЗ ХЕЛ
ХАРЧОВІ ДОБАВКИ ПІДГОТУВАЛА СОКОЛОВСЬКА АЛЬОНА УЧЕНИЦЯ 8А КЛАСУ КНЗ ХЕЛ  Генетическая связь классов соединений
Генетическая связь классов соединений Frunol delicia GmbH. Витаминизированные жидкие удобрения
Frunol delicia GmbH. Витаминизированные жидкие удобрения Ochistka_stochnykh_vod
Ochistka_stochnykh_vod Гидролиз солей
Гидролиз солей Мұнай тотықтырушы микроағзалардың өсу және дамуына күкірттің әсерін зерттеу
Мұнай тотықтырушы микроағзалардың өсу және дамуына күкірттің әсерін зерттеу Білки. Властивості та функції
Білки. Властивості та функції Физические методы анализа
Физические методы анализа Аморфные сплавы
Аморфные сплавы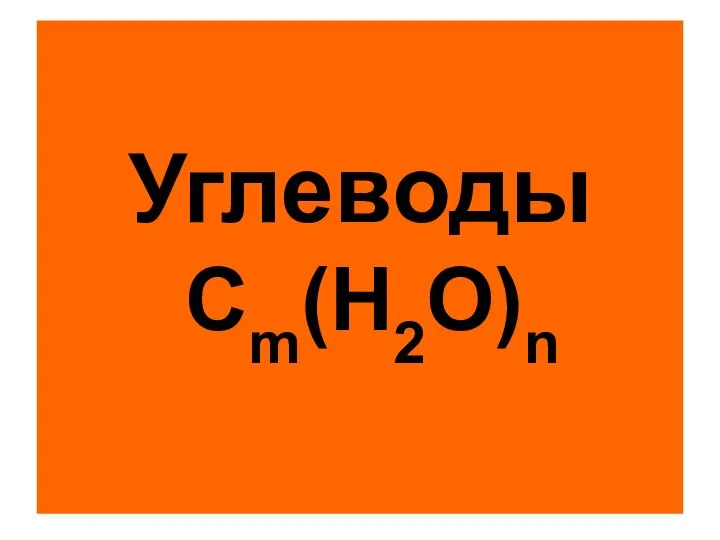 Углеводы Сm(Н2О)n
Углеводы Сm(Н2О)n  Мы́ло — жидкий или твёрдый продукт, содержащий поверхностноактивные вещества
Мы́ло — жидкий или твёрдый продукт, содержащий поверхностноактивные вещества Робота учня 11-В класу: Андрійка Андрія
Робота учня 11-В класу: Андрійка Андрія  Органическое часть почвы
Органическое часть почвы Теоретические основы химической технологии
Теоретические основы химической технологии Получение и установление состава кристаллогидрата фосфата цинка
Получение и установление состава кристаллогидрата фосфата цинка Метаболизм этанола
Метаболизм этанола Лекарственные вещества (определения и классификация)
Лекарственные вещества (определения и классификация) Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Фитотерапия в кардиологии
Фитотерапия в кардиологии Синтетикалық полимерлер (пластиктер)
Синтетикалық полимерлер (пластиктер) Общая характеристика металлов IА группы ПСХЭ Д.И. Менделеева
Общая характеристика металлов IА группы ПСХЭ Д.И. Менделеева