Содержание
- 3. Лекция 1. Химическая термодинамика. Основные понятия.
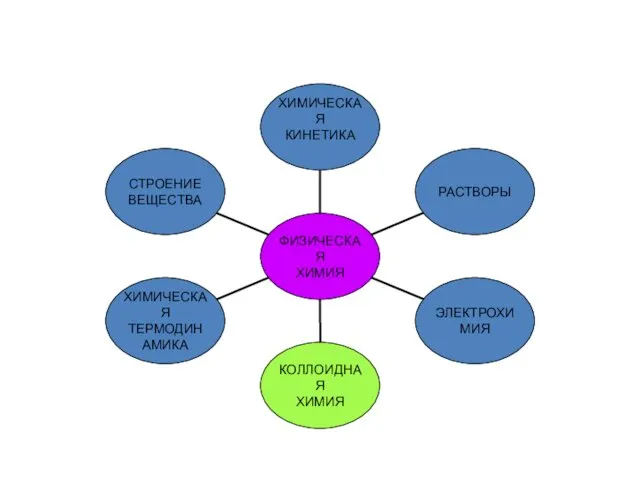
- 4. Химическая термодинамика – раздел физической химии, изучающий превращение энергии в химических процессах и энергетические характеристики различных
- 5. Обратимый процесс – система бесконечно медленно (на практике исп. конечное время) переходит из одного состояния равновесия
- 6. Работа и Теплота – единственно возможные неравноценные формы передачи энергии, зависящие от способа перехода системы из
- 7. Первое начало термодинамики (Ю. Майер (1842г.); Дж. Джоуль (1843г.)) В замкнутой системе сумма всех видов энергии
- 8. Процессы при постоянном объеме: Тогда - тепловая энергия процесса при постоянном объеме (в данном случае является
- 9. Эндотермический процесс – идет с поглощением тепловой энергии системой: Экзотермический процесс – идет с выделением тепловой
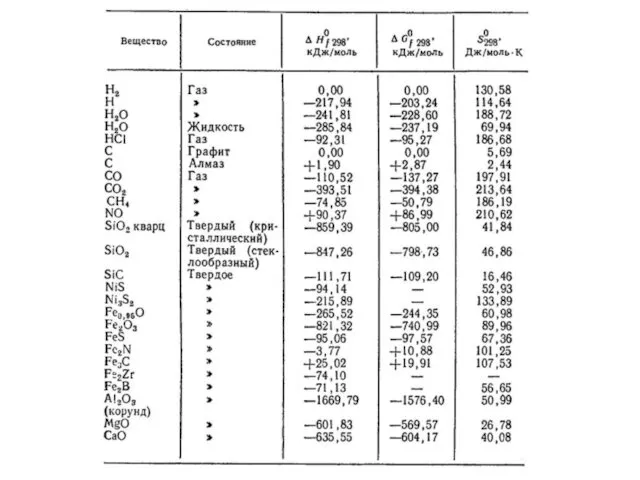
- 10. Стандартные энтальпии образования некоторых веществ
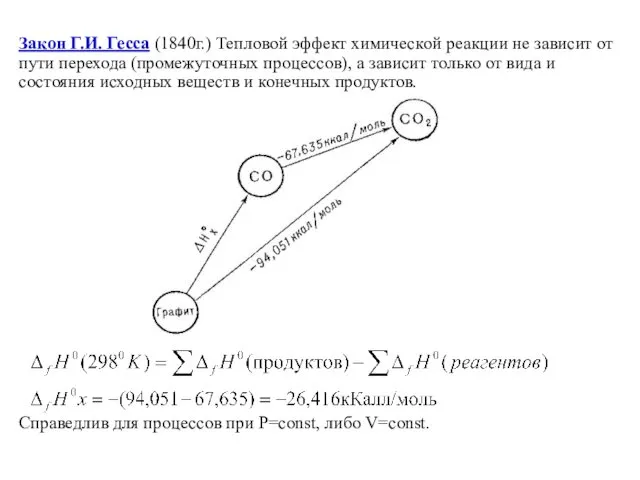
- 11. Закон Г.И. Гесса (1840г.) Тепловой эффект химической реакции не зависит от пути перехода (промежуточных процессов), а
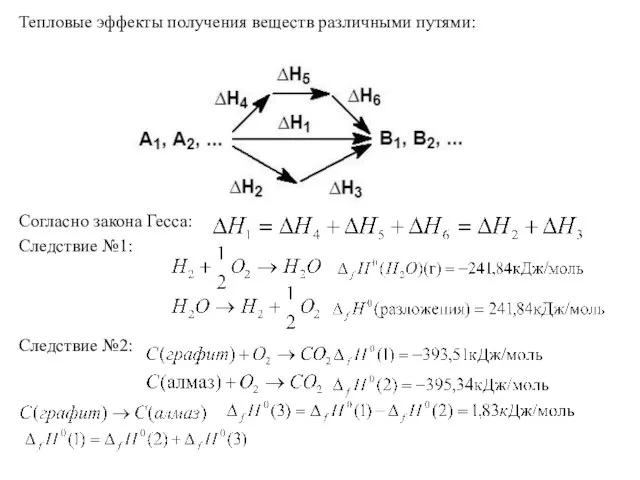
- 12. Тепловые эффекты получения веществ различными путями: Согласно закона Гесса: Следствие №1: Следствие №2:
- 13. Следствие №3:
- 14. Второе начало термодинамики Первое начало термодинамики не характеризует направленность и самопроизвольность процессов. Однако процессы могут быть
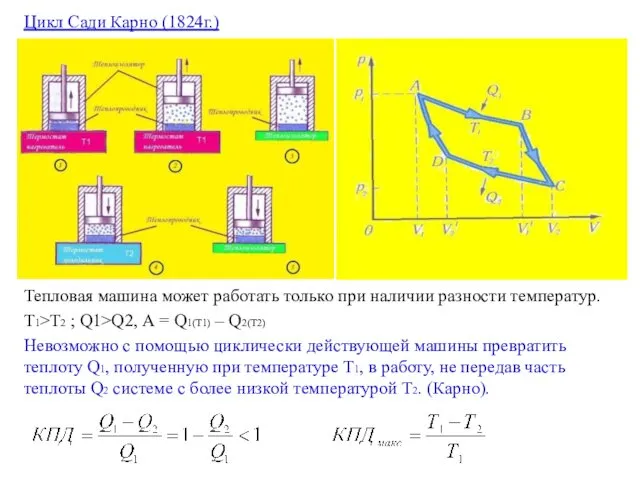
- 15. Цикл Сади Карно (1824г.) Тепловая машина может работать только при наличии разности температур. Т1>T2 ; Q1>Q2,
- 16. Ни одно устройство не может извлечь работу из системы, которая находится на одном энергетическом уровне. Теплота
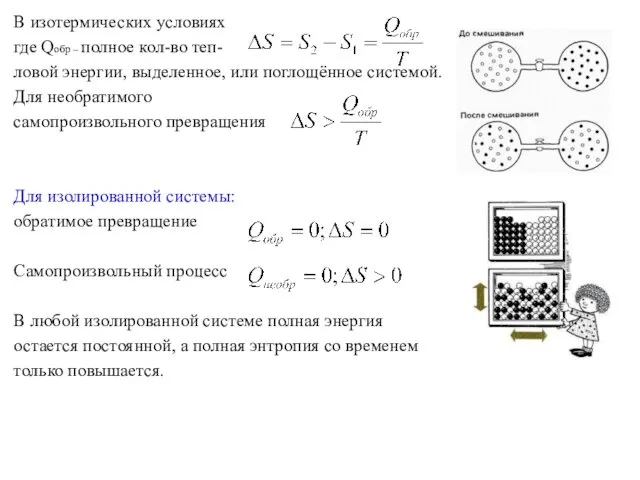
- 17. В изотермических условиях где Qобр – полное кол-во теп- ловой энергии, выделенное, или поглощённое системой. Для
- 18. Статистическая интерпретация энтропии. Шарики в коробке – макросостояние. Черные к черным, белые к белым (вариант упаковки
- 19. Третье начало позволяет определить абсолютную энтропию SТ [Дж/(моль*К)] всех чистых веществ при любой температуре.
- 20. Свободная энергия (рассматривается закрытая система при T=const.) Обратимый процесс Необратимый процесс Если P = const., то:
- 21. Обратимый процесс (равновесный) Необратимый процесс Если T = const. и V = const.: F (изохорно-изотермический потенциал,
- 22. Примеры реакций 1. 2. 3. 4.
- 23. Свободная энергия образования соединения - равна изменению свободной энергии, сопровождающему реакцию образования 1 моль сложного соединения
- 26. Скачать презентацию








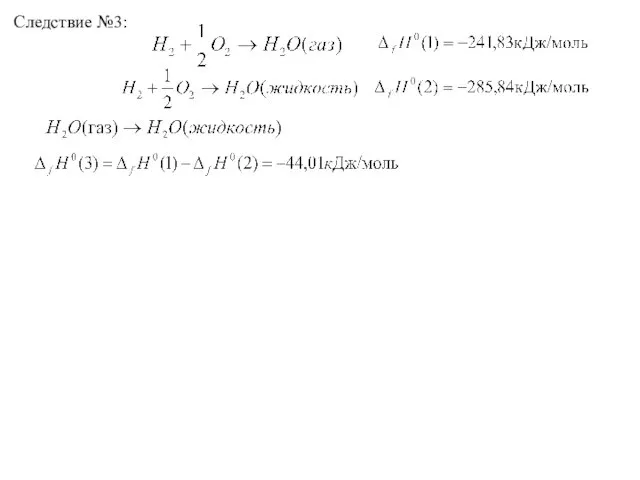



![Третье начало позволяет определить абсолютную энтропию SТ [Дж/(моль*К)] всех чистых веществ при любой температуре.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/474793/slide-18.jpg)




 Презентация по Химии "История развития химии" - скачать смотреть
Презентация по Химии "История развития химии" - скачать смотреть  Строение атома Подготовка к ЕГЭ
Строение атома Подготовка к ЕГЭ Производство каустической соды Дисциплина: Технология химических производств
Производство каустической соды Дисциплина: Технология химических производств Негосударственное образовательное учреждение частная школа «Радуга» Исследование чипсов Выполнил Ученик 10класса Борзов Ден
Негосударственное образовательное учреждение частная школа «Радуга» Исследование чипсов Выполнил Ученик 10класса Борзов Ден Химический элемент цинк
Химический элемент цинк Кислородсодержащие органические соединения. Предельные одноатомные спирты
Кислородсодержащие органические соединения. Предельные одноатомные спирты Энергетика химических процессов
Энергетика химических процессов Обмен аминокислот и белков
Обмен аминокислот и белков Разработка и добыча нефти и газа. (Тема 1.5)
Разработка и добыча нефти и газа. (Тема 1.5) Презентация по Химии "Химия. Классификация химических реакций" - скачать смотреть бесплатно
Презентация по Химии "Химия. Классификация химических реакций" - скачать смотреть бесплатно Спирты. Классификация, номенклатура, изомерия. Спирты в природе
Спирты. Классификация, номенклатура, изомерия. Спирты в природе Хлороводород и соляная кислота. Свойства и применение. Подготовила: Ученица 8 класса МБОУ СОШ с.Фащёвка Столяренко Дарья
Хлороводород и соляная кислота. Свойства и применение. Подготовила: Ученица 8 класса МБОУ СОШ с.Фащёвка Столяренко Дарья  Химические свойства легкоплавких металлов
Химические свойства легкоплавких металлов Презентация по Химии "Классификация химических реакций" - скачать смотреть
Презентация по Химии "Классификация химических реакций" - скачать смотреть  Кислород, его получение и физ свойства
Кислород, его получение и физ свойства Экзогенная серия. Группа выветривания
Экзогенная серия. Группа выветривания Цинк (Zn). Свойства
Цинк (Zn). Свойства Теория растворов. Растворы электролитов
Теория растворов. Растворы электролитов Подготовка к ЕГЭ
Подготовка к ЕГЭ Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Закономерности протекания химических процессов. Основы химической термодинамики. (Лекция 2)
Закономерности протекания химических процессов. Основы химической термодинамики. (Лекция 2) Строение атома азота
Строение атома азота Применение неорганических соединений в пищевой промышленности
Применение неорганических соединений в пищевой промышленности Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение
Группа веществ, требующих особых методов изолирования. Характеристика соединений. Токсикологическое значение Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ
Общие вопросы аналитической химии. Химические методы обнаружения неорганических веществ Презентация по Химии "Чугуны. Классификация" - скачать смотреть
Презентация по Химии "Чугуны. Классификация" - скачать смотреть  Метаморфогенные месторождения
Метаморфогенные месторождения Оксиды. Физические свойства
Оксиды. Физические свойства