Содержание
- 2. Взаимодействие с газами Взаимодействие с водой Взаимодействие с технологическими средами ЛИТИЙ НАТРИЙ, КАЛИЙ, Na-K, ЦЕЗИЙ СВИНЕЦ,
- 3. ХИМИЧЕСКИЕ СВОЙСТВА ЛИТИЯ
- 4. ВЗАИМОДЕЙСТВИЕ ЛИТИЯ С КИСЛОРОДОМ, АЗОТОМ, УГЛЕРОДОМ, ВОДОЙ И ВОДЯНЫМ ПАРОМ
- 5. Свойства лития Литий взаимодействует с атмосферными газами. Это процесс зависит состава газовой среды, влажности, температуры, наличия
- 6. Взаимодействие лития с O2, N2, CO2 идет с выделением избыточного тепла по следующим реакциям (при 500oC):
- 7. При нормальных условиях литий медленно взаимодействует с воздухом. Конечным продуктом взаимодействия является Li2CO3∙OH. Взаимодействие твердого лития
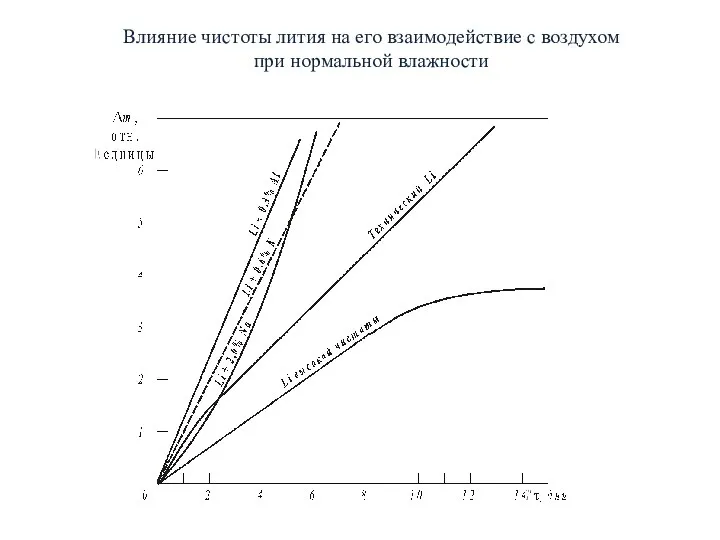
- 8. Влияние чистоты лития на его взаимодействие с воздухом при нормальной влажности
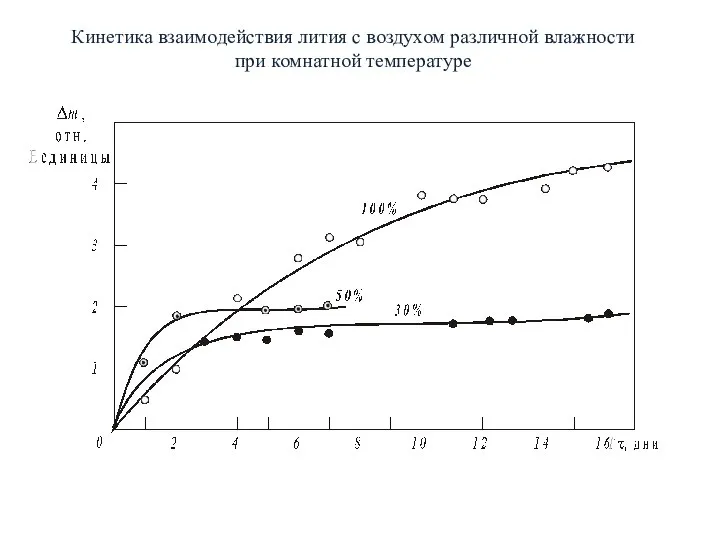
- 9. Кинетика взаимодействия лития с воздухом различной влажности при комнатной температуре
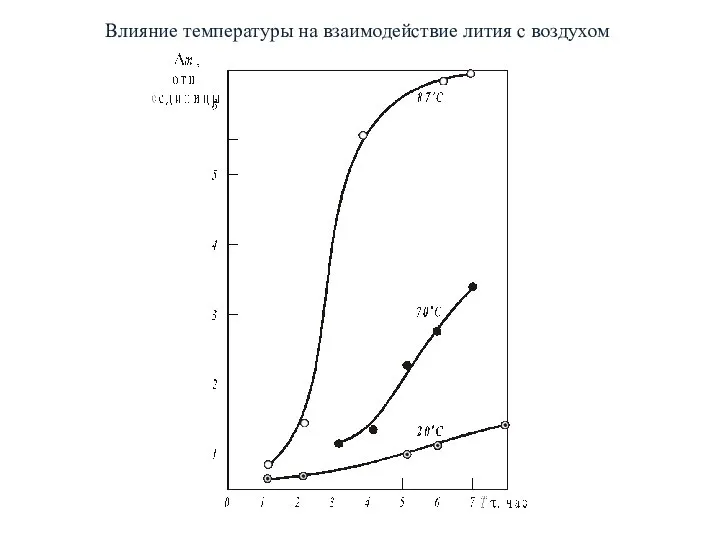
- 10. Влияние температуры на взаимодействие лития с воздухом
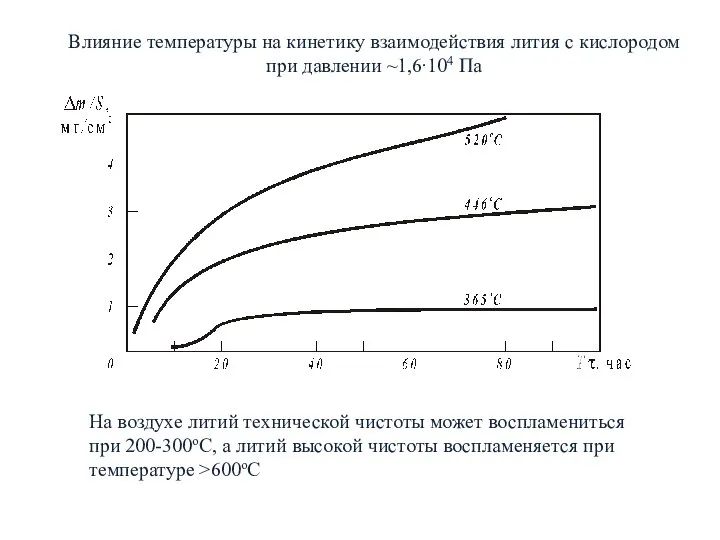
- 11. Влияние температуры на кинетику взаимодействия лития с кислородом при давлении ~1,6∙104 Па На воздухе литий технической
- 12. Влияние температуры на взаимодействие лития с азотом при давлении ~1,4∙104 Па При температурах >450оС литий воспламеняется
- 13. При взаимодействии открытой поверхности жидкого металла с воздухом при нормальной влажности происходит его горение, температура которого
- 14. Li марки ЛЭ-1 (>99,5% Li; основные примеси: Na, Ca, O, N ...) Время экспозици на воздухе
- 15. 10 с после раз-реза 45 с 1 час 3 часа 17 дней 8 дней 3 дня
- 16. Конденсат Li на фольге из нержавеющей стали Чистота Li >99.99% обеспечивалась низкой температурой испарения - ~600oC)
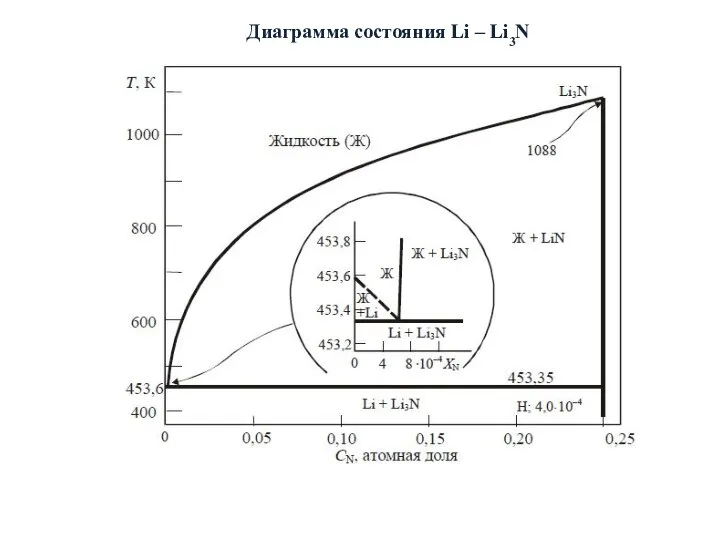
- 17. Диаграмма состояния Li – Li3N
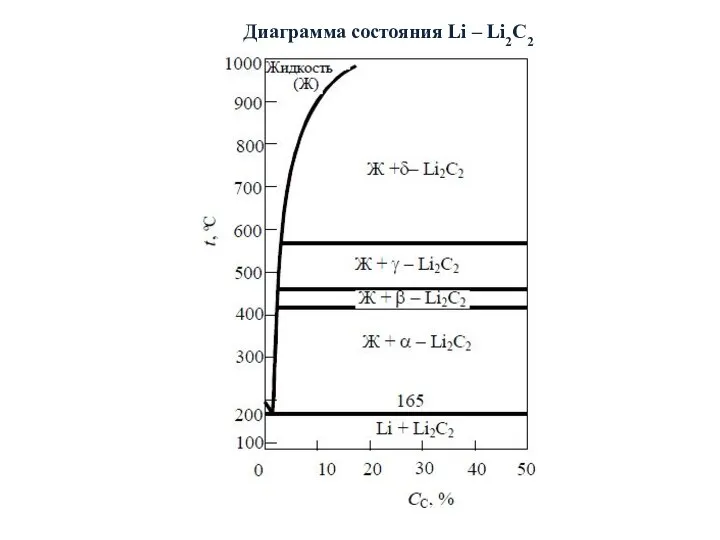
- 18. Диаграмма состояния Li – Li2C2
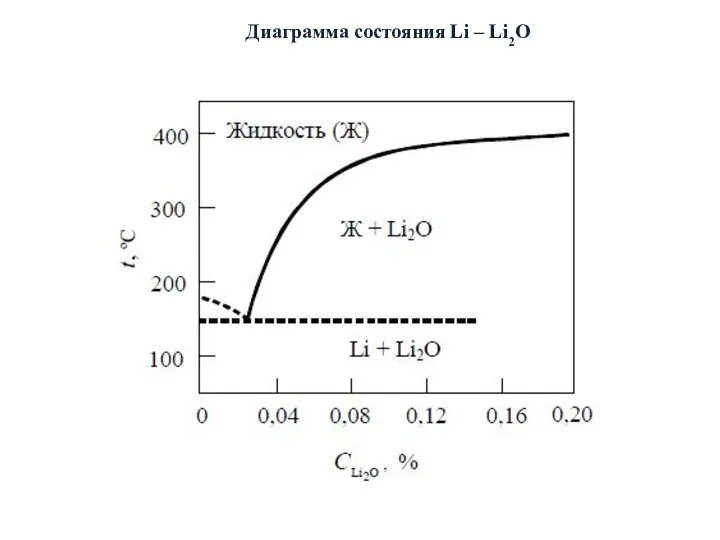
- 19. Диаграмма состояния Li – Li2O
- 20. Диаграмма состояния Li – LiH (DH)
- 21. Зависимость растворимости неметаллических примесей, в литии и других жидких металлах в практически интересующем интервале температур описывается
- 22. Растворимость кислорода, азота, углерода и водорода в литии
- 23. Растворимость неметаллов в литии при различных температурах, %
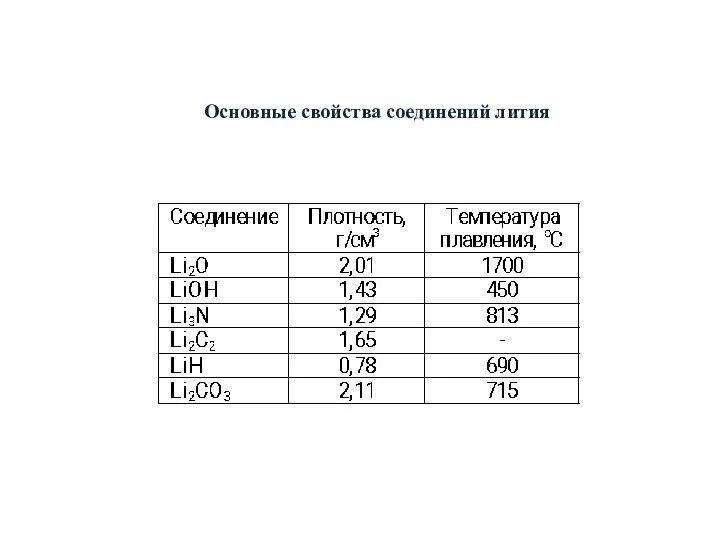
- 24. Основные свойства соединений лития
- 25. ХИМИЧЕСКИЕ СВОЙСТВА НАТРИЯ, КАЛИЯ, ЦЕЗИЯ
- 26. Свойства натрия При непосредственном взаимодействии натрия с кислородом в зависимости от условий образуется оксид Na2O или
- 27. Взаимодействие натрия с водой, спиртом Реагируя с водой Na образует гидрооксид NaOH и H2; реакция может
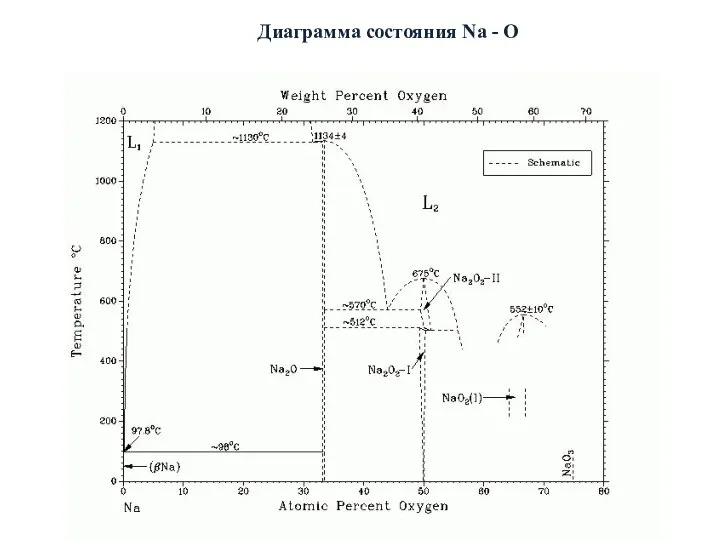
- 28. Диаграмма состояния Na - O
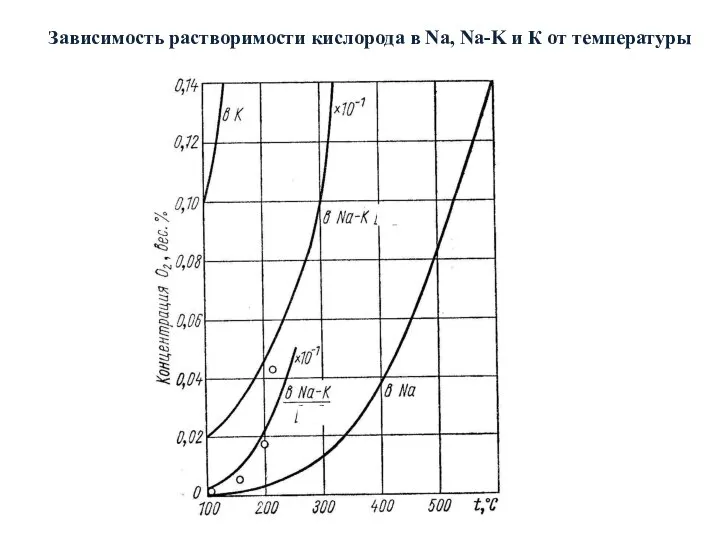
- 29. Зависимость растворимости кислорода в Na, Na-K и К от температуры
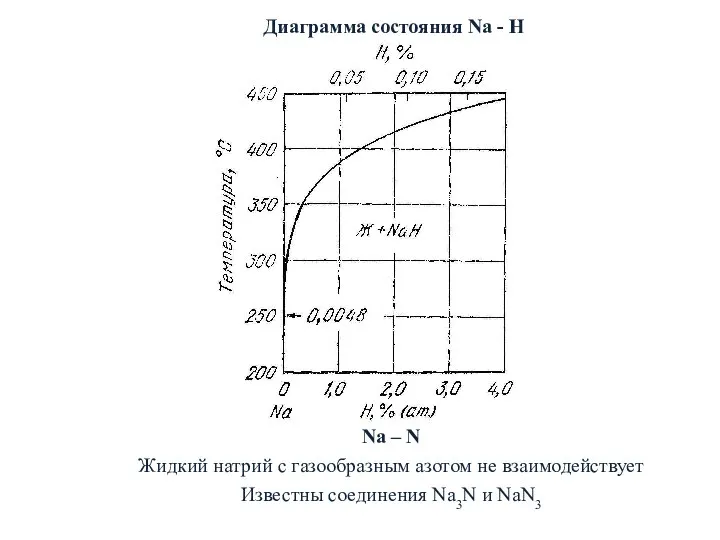
- 30. Диаграмма состояния Na - H Na – N Жидкий натрий с газообразным азотом не взаимодействует Известны
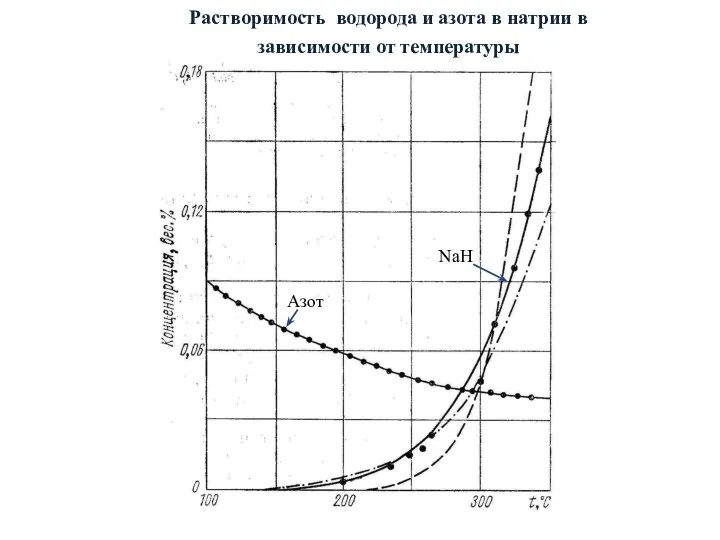
- 31. Растворимость водорода и азота в натрии в зависимости от температуры Азот NaH
- 32. Свойства калия Валентный электрон атома калия более удален от его ядра, чем валентные электроны лития и
- 33. Свойства цезия Цезий обладает очень высокой реакционной способностью. На воздухе мгновенно воспламеняется с образованием пероксида Cs2O2
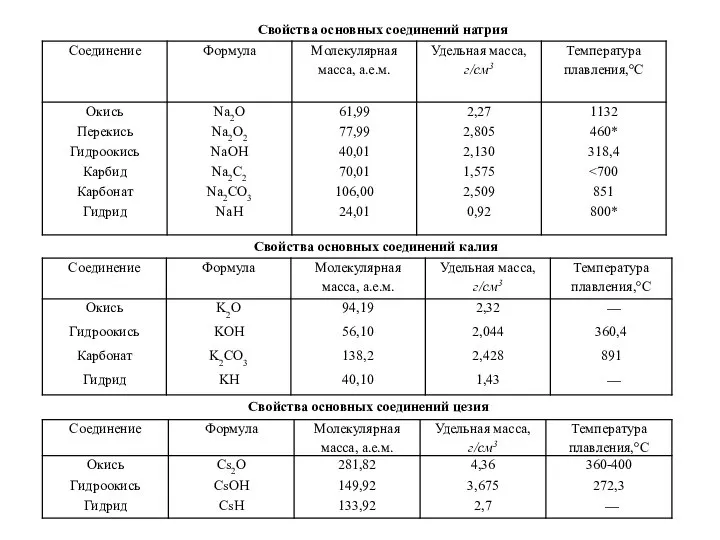
- 34. Свойства основных соединений натрия Свойства основных соединений калия Свойства основных соединений цезия
- 35. ХИМИЧЕСКИЕ СВОЙСТВА СВИНЦА и Li17Pb83
- 36. Свинец сравнительно мало активен химически. С кислородом свинец образует оксиды Рb2О, РbО, РbО2, Рb3О4 и Рb2О3.
- 37. Свинец хорошо растворим в разбавленной азотной кислоте, а в серной и соляных кислотах растворяется лишь при
- 38. В свинце неметаллические примеси растворяются по сравнению с литием незначительно. Растворимость кислорода в свинце, весьма низка
- 39. Теплота, выделяющаяся при взаимодействии лития и Li17Pb83 с водой и воздухом при 527 °С
- 40. Растворимость водорода в металлах Основной закон, связывающий концентрацию С двухатомного диссоциирующего при растворении в металле газа
- 41. ХИМИЧЕСКИЕ СВОЙСВА ГАЛЛИЯ
- 42. Химические свойства галлия близки к свойствам алюминия. Оксидная плёнка Ga2O3 (Тпл= 1795°C), образующаяся на поверхности металла
- 43. Галлий реагирует с галогенами: реакция с хлором и бромом идёт при комнатной температуре, с фтором —
- 44. ВЗАИМОДЕЙСТВИЕ ЖИДКИХ МЕТАЛЛОВ С ТЕХНОЛОГИЧЕСКИМИ СРЕДАМИ
- 45. ЛИТИЙ Литий активно взаимодействует с разбавленными неорганическими кислотами (HNO3, H2SO4, HF, HCl) С концентрированными HNO3, HCl
- 46. НАТРИЙ, КАЛИЙ, Na-K С разбавленными растворами неорганических кислот Na, K реагируют со взрывом. С органическими кислотами
- 48. Скачать презентацию
































 Применение алкинов
Применение алкинов Кристаллография. Кристаллическое состояние
Кристаллография. Кристаллическое состояние Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Основные классы неорганических веществ
Основные классы неорганических веществ Кислоты
Кислоты Inert metals
Inert metals Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены
Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены Химия переходных элементов. Триада железа и металлы платиновой группы
Химия переходных элементов. Триада железа и металлы платиновой группы Пищевые кислоты Выполнил: Черепнин Евгений Группа: ТХ-921
Пищевые кислоты Выполнил: Черепнин Евгений Группа: ТХ-921  Последствия применения удобрений в сельском хозяйстве
Последствия применения удобрений в сельском хозяйстве Задача №7. По щам! Команда Карбораны
Задача №7. По щам! Команда Карбораны Азот
Азот V и III группы периодической системы элементов Д.И. Менделеева
V и III группы периодической системы элементов Д.И. Менделеева Установка гидрокрекинга в составе завода глубокой переработки нефти ООО Кинеф
Установка гидрокрекинга в составе завода глубокой переработки нефти ООО Кинеф Фосфор
Фосфор Спиртовое, масляное и кисломолочное брожение
Спиртовое, масляное и кисломолочное брожение Сера
Сера Химические свойства металлов Урок химии в 11 классе
Химические свойства металлов Урок химии в 11 классе Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Гидролиз солей
Гидролиз солей Роль взаимодействия серотонин- и дофаминергической систем в иммуномодуляции
Роль взаимодействия серотонин- и дофаминергической систем в иммуномодуляции Кислоты и их свойства
Кислоты и их свойства Минералогическая шкала твёрдости Мооса
Минералогическая шкала твёрдости Мооса Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП
Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП ГИА. Вопрос А2. ПЗ и ПСХЭ
ГИА. Вопрос А2. ПЗ и ПСХЭ Строение атома и атомного ядра
Строение атома и атомного ядра Строение атома. Периодическая таблица Менделеева. Химическая связь
Строение атома. Периодическая таблица Менделеева. Химическая связь Презентация по Химии "Органические вещества. Нуклеиновые кислоты" - скачать смотреть
Презентация по Химии "Органические вещества. Нуклеиновые кислоты" - скачать смотреть