Содержание
- 2. Горение сурьмы в атмосфере хлора. 2Sb + 3Cl2 = 2SbCl3 2Sb + 5Cl2 = 2SbCl5
- 3. Горение натрия 2Na + O2 = Na2O2
- 5. Выберите реакцию горения алюминия. 2Al + 3Cl2 = 2AlCl3 4Al + 3O2 = 2Al2O3 4Li +O2
- 6. Где применяют или применяли реакции горения Al и Mg ?
- 7. Реакция взаимодействия кальция с водой. 2Na + 2H2O = 2NaOH + H2↑
- 8. Условия взаимодействия металлов с растворами кислот и солей. Металл должен находиться в ряду напряжения левее водорода;
- 10. Скачать презентацию







 Хімія в побуті
Хімія в побуті Металлы
Металлы Развитие учебной мотивации на уроках химии через систему урочной и внеурочной деятельности
Развитие учебной мотивации на уроках химии через систему урочной и внеурочной деятельности Кислоты и соли. (8 класс)
Кислоты и соли. (8 класс) Вермикулит. Технические характеристики
Вермикулит. Технические характеристики Минералы и Близнецы
Минералы и Близнецы Биологическое окисление
Биологическое окисление Общая характеристика ферментов как биологических катализаторов
Общая характеристика ферментов как биологических катализаторов Оксиды ангидриды
Оксиды ангидриды Презентация по Химии "ПЛАСТМАССА" - скачать смотреть
Презентация по Химии "ПЛАСТМАССА" - скачать смотреть  Презентация по Химии "Презентація на тему: Природний газ" - скачать смотреть бесплатно
Презентация по Химии "Презентація на тему: Природний газ" - скачать смотреть бесплатно Выращивание кристаллов Выполнил: ученик 8 класса А Алексеев Ден
Выращивание кристаллов Выполнил: ученик 8 класса А Алексеев Ден Хлор. Способы получения хлора
Хлор. Способы получения хлора Положение тугоплавких металлов в Периодической системе элементов
Положение тугоплавких металлов в Периодической системе элементов Фильтрационные свойства.Решение уравнений Стокса для несжимаемой жидкости
Фильтрационные свойства.Решение уравнений Стокса для несжимаемой жидкости Дисперсные системы
Дисперсные системы Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток
Кристалічні ґратки. Залежність фізичних властивостей речовини від типів кристалічних ґраток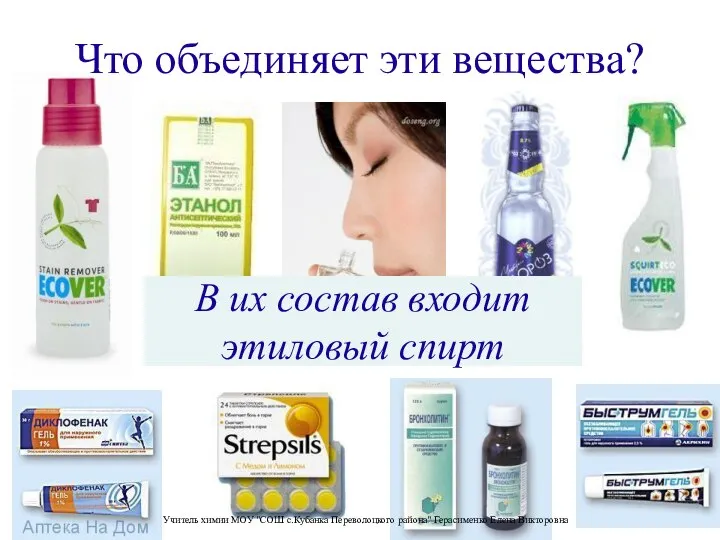 Что объединяет эти вещества?
Что объединяет эти вещества?  Щелочноземельные металлы
Щелочноземельные металлы Теория растворов. Растворы электролитов
Теория растворов. Растворы электролитов Металлы 4 группы А подгруппы
Металлы 4 группы А подгруппы Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение МОУ средняя общеобразовательная школа с. Минаевки Асиновского района Томской области урок подготовила : учитель 1 категории Суц
МОУ средняя общеобразовательная школа с. Минаевки Асиновского района Томской области урок подготовила : учитель 1 категории Суц Нефть: состав, свойства, месторождения, применение
Нефть: состав, свойства, месторождения, применение Технология вакуумной перегонки мазута
Технология вакуумной перегонки мазута Метаболизм липидов. Метаболизм глицерофосфолипидов и холестерола. (Лекция 3)
Метаболизм липидов. Метаболизм глицерофосфолипидов и холестерола. (Лекция 3) Органічні сполуки. Вплив на організм людини Учениця 11-Б класу Колчаг Юлія
Органічні сполуки. Вплив на організм людини Учениця 11-Б класу Колчаг Юлія