Содержание
- 2. Химиялық формула –заттың құрамын химиялық элемент таңбалары және индекстері көмегімен шартты түрде бейнелеу. Индекс - затттың
- 4. Зат массасының сақталу заңы - реакцияға қатысқан заттардың массасы реакция нәтижесінде түзілген заттардың массасына тең болады.
- 5. Химиялық теңдеудің сол жағына әрекеттесуші заттардың формуласын, ал оң жағына жаңадан түзілген заттардың формуласын жазады. Әрекеттесуші
- 6. Зат массасының сақталу заңының ашылуы 1789г. Роберт Бойль 1673г. 1756г. М. В. Ломоносов Антуан Лавуазье
- 8. Теңдеу бойынша қандай мәліметтер алуға болады Сапалық және сандық кұрамы туралы мәлімет (қандай заттар және қаншасы
- 9. Коэффициенттер қою ережелері: 1. Коэффициенттерді орналастырып қою үшін құрамы жағынан ең күрделі қосылыстардаң бастау қажет және
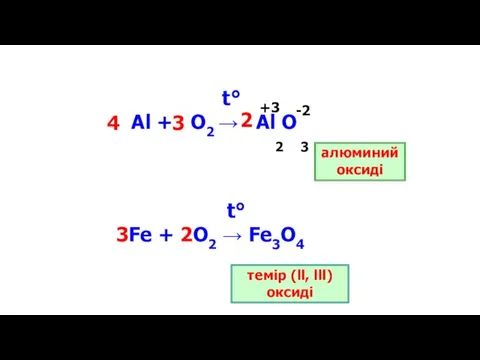
- 10. t° Al + O2 → Al O t° 3Fe + 2O2 → Fe3O4 +3 -2 2
- 11. t° S + O2 → SO t° Р + О2 → Р О t° С +
- 12. Химиялық реакция теңдеуін құрастыру Үш кезеңді қамтиды: Бастапқыда реакцияға қатысқан(сол жақ) және реакция нәтижесінде түзген өнімнің
- 13. Химиялық теңдеулер бойынша есептеулер (алгаритмі) Химиялық теңдеулер бойынша есептеулер (стехиометриялық есептеулер) зат массасының сақталу заңына негізделген.
- 14. Химиялық реакциялар Қайтымсыз Қайтымды Нәтижесінде бастапқы заттар (реагенттер) толығымен реакция өнімдеріне айналатын химиялық реакция Бір мезгілде
- 15. Қайтымсыз реакциялар жану Кейбір қосылыстардың ыдырауы 1. Тұнбаның түсуі 2. Газ бөліну 3. Өте аз диссоцияланатын
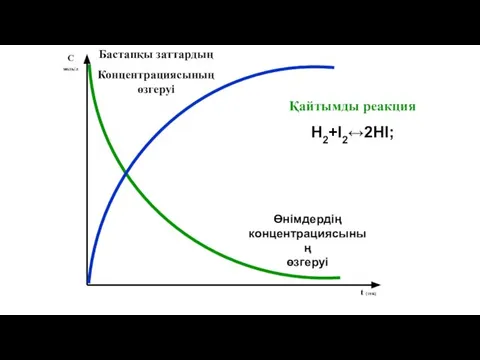
- 16. С моль/л t (сек) Қайтымды реакция H2+І2↔2HІ; Бастапқы заттардың Концентрациясының өзгеруі Өнімдердің концентрациясының өзгеруі
- 17. Тура реакция Кері реакция Теңдеудің сол жағы Теңдеудің оң жағы
- 18. Қайтымсыз реакциялар АgNO3 + NaCl → AgCl↓+NaNO3 2LiOH + H2SO4 → Li2SO4+2H2O K2CO3 + 2HCl →
- 19. Қайтымды реакциялар N2 + 3H2 ↔ 2NH3 N2 + O2 ↔ 2NO FeCl3 + 3KCNS ↔
- 20. N2 + 3H2 ↔ 2NH3 СО + 2Н2 ↔ СН3ОН Al2O3 + 6HCl = 2AlCl3 +
- 22. Кез-келген қайтымды реакция реакция үшін бастапқы сәтте әрекеттесуші массалар заңына сәйкес тура реакцияның жылдамдығы нөлге тең.
- 23. Химиялық тепе-теңдік Тура және кері реакциялардың жылдамдықтары тең болғандағы жүйенің күйін химиялық тепе-теңдік деп атайды.
- 24. Ле -Шателье принципі химиялық тепе –теңдікте тұрған жүйе күйіне сыртқы факторлардың біреуімен( қысым, температура , концентрация
- 25. Химиялық тепе-теңдіктің ығысуына әсер етуші факторлар
- 29. Тура және кері реакцияның жылдамдық қатынастарының қатынасы да тұрақты болады және оны осы реакцияның тепе-теңдік константасы
- 30. N2 + 3H2 ↔ 2NH3 Химиялық кинетиканың заңы бойынша тура және кері реакциялардың жылдамдықтарын былай жазуға
- 31. Егер Кр ˃ 1, онда Vтура ˃Vкері , егер Кр ˂1 , онда Vтура ˂ Vкері
- 32. Есеп 1. Белгілі бір температурада тепе-теңдік концентрациясы жүйеде 2CO (г) + O2 (г) 2CO2(г)былай өзгерді: [CO]
- 33. . 2CO(г) + O2(г) 2CO(г).
- 34. Зат мөлшері – физикалық шама Зат мөлшері сол заттың құрылымдық бөлшектерінің санымен анықталады, яғни атом, молекула
- 35. Моль дегеніміз не? Моль – берілген заттың құрылымдық бөлшектері 12г көміртегіндегі атом санына сәйкес келетін зат
- 36. Заттың керекті мөлшерін қалай өлшеп алуға болады? Зат мөлшерін моль арқылы өрнектеген сияқты молярлық масса зат
- 37. Молярлы масса заттың салыстырмалы молекулық массасының шамасына тең Молярлы масса – бұл физикалық шама 1моль заттың
- 38. Авагадро саны Зат мөлшері мен бөлшек (атом, молекула т.б) сандары арасында байланыс, ѵ = N /
- 39. Зат мөлшері ұғымын қолданып есептер шығару Зат мөлшері
- 40. Бер: m(CO2) = 88 г Табу керек: n(CO2) - ? Шешуі: M(CO2) = 44 г/моль Жауабы:
- 41. Бер: n(N2) = 10 моль Табу керек: m (N2) - ? Шешуі: M (N2)= 28 г/моль
- 42. Бер: m (S) = 6,2 г Табу керек: n (S) - ? Шешуі: M(S) = 32
- 43. Газдың молярлық көлемі: Газдың мольдік көлемі – берілген газ көлемінің оның химиялық зат мөлшеріне қатынасына тең
- 44. Авогадро заңының салдары: Әртүрлі газдардың бірдей молекулалар саны бірдей қысымда және температурада бірдей көлемді алады. Қалыпты
- 48. Скачать презентацию











































 Титан. Физические свойства титана
Титан. Физические свойства титана Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі Энергетические эффекты реакций
Энергетические эффекты реакций Синтетичні речовини у сільському господарстві, медицині та промисловості Презентація на тему:
Синтетичні речовини у сільському господарстві, медицині та промисловості Презентація на тему:  Биохимия и молекулярная биология. Биосинтез мембранных липидов. Лекция 9
Биохимия и молекулярная биология. Биосинтез мембранных липидов. Лекция 9 Карбонильные соединения (оксосоединения)
Карбонильные соединения (оксосоединения) Углеводы
Углеводы Катализ.Лекция
Катализ.Лекция Тыңайтқыштар
Тыңайтқыштар Урок химии на тему: «Типы химических реакций»
Урок химии на тему: «Типы химических реакций» История мыловарения. Моющее действие мыла
История мыловарения. Моющее действие мыла Презентация по Химии "Открытия и изобретения в химии" - скачать смотреть
Презентация по Химии "Открытия и изобретения в химии" - скачать смотреть  Презентация на тему: Химия и производство
Презентация на тему: Химия и производство Периодическая система химических элементов Д.И. Менделеева и строение атома
Периодическая система химических элементов Д.И. Менделеева и строение атома Щелочные металлы
Щелочные металлы Презентация по Химии "Аммиак" - скачать смотреть
Презентация по Химии "Аммиак" - скачать смотреть  Аналитический скрининг
Аналитический скрининг Дослідження на тему: Повітря Христинівщини За проектом “Екологічна ситуація у рідному місті”
Дослідження на тему: Повітря Христинівщини За проектом “Екологічна ситуація у рідному місті” Растворы
Растворы Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату Адсорбционные взаимодействия
Адсорбционные взаимодействия Презентация по Химии "ГАЛЕРЕЯ РУССКИХ ХИМИКОВ" - скачать смотреть бесплатно
Презентация по Химии "ГАЛЕРЕЯ РУССКИХ ХИМИКОВ" - скачать смотреть бесплатно Презентация по Химии "Знакомство с кислотами" - скачать смотреть
Презентация по Химии "Знакомство с кислотами" - скачать смотреть  Основания. Классификация оснований
Основания. Классификация оснований Бинарные соединения
Бинарные соединения  Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Александрит
Александрит Фенол. Получение и использование, физические и химические свойства. Биологическая роль
Фенол. Получение и использование, физические и химические свойства. Биологическая роль