Содержание
- 2. КІРІСПЕ:
- 3. Термодинамика - термодинамикалық тепе –теңдік күйдегі макроскопиялық жүйелердің жалпы қасиеттерін және бір күйден екінші бір күйге
- 4. Термодинамикалық жүйе – өзара әсерлесуші, әрі өзара ғана емес басқа денелермен де (сыртқы ортамен) әсерлесуші және
- 5. . Идеал газдың күйін сипаттайтын заңдар Бойль — Мариот заңы Гей-Люссак заңы Шарль заңы
- 6. Изотермиялық процесс Изопроцестердің ішінен бірінші болып осы изотермиялық процесс зерттелді. Ағылшын физигі Р. Бойль 1662 ж.
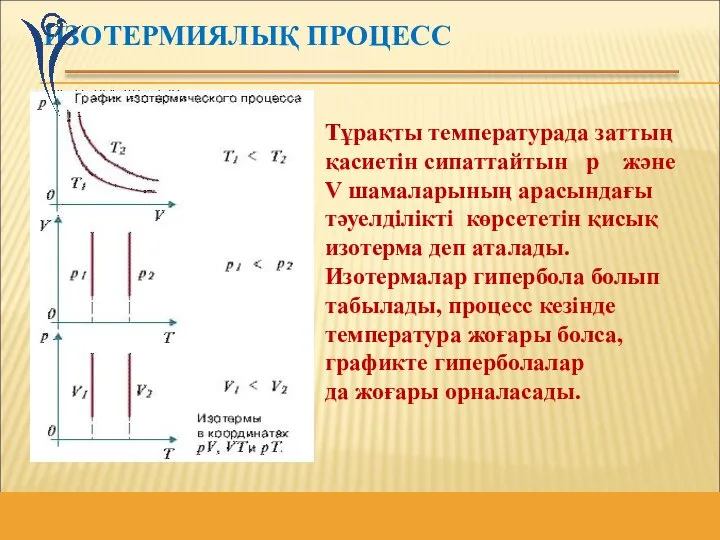
- 7. ИЗОТЕРМИЯЛЫҚ ПРОЦЕСС Тұрақты температурада заттың қасиетін сипаттайтын p және V шамаларының арасындағы тәуелділікті көрсететін қисық изотерма
- 8. Изохоралық процесс Бұл процесті француз физигі Ж.Шарль зерттеген. 1787 жылы ол тәжірибе жүзінде тұрақты көлемде берілген
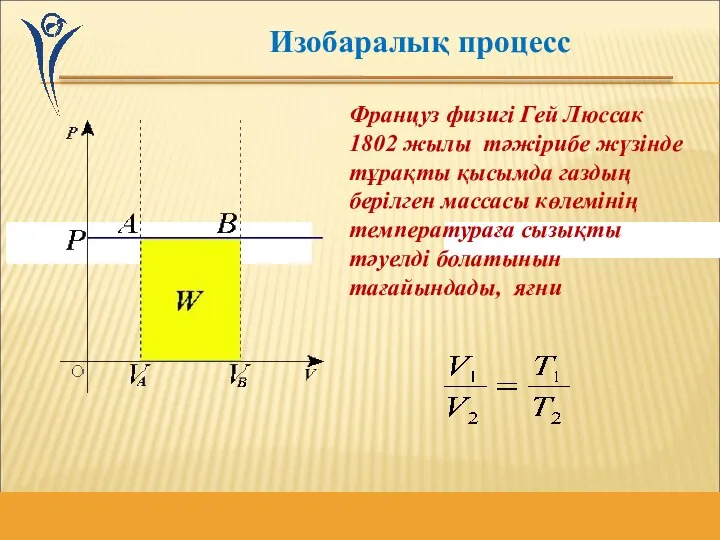
- 9. Француз физигі Гей Люссак 1802 жылы тәжірибе жүзінде тұрақты қысымда газдың берілген массасы көлемінің температураға сызықты
- 10. 1801 ж. Дальтон заңы газ қоспасының қысымын және жеке компоненттердің жалпы қысымға беретін нақты «үлесін» анықтады.
- 11. Парциал қысым деп газ қоспасының әрбір газы осы көлемді жалғыз өзі алатын кездегі қысымды атайды. Дальтон
- 12. Газ қоспасында әрбір газдың парциал қысымы берілген қоспа құрамындағы молекула санына пропорционал болады. Осыған байланысты газ
- 13. Газ тәрізді заттар қатынасында жүретін Қайтымды реакцияларда концентрация мен қысым арасында байланыс болады. Газ қоспасының жалпы
- 14. Газ қоспалары мен парциал қысым Көптеген газ тәрізді заттар таза түрінде емес, қоспа түрінде болады. Мысалы,
- 15. Газ қоспалары мен парциал қысым Мысалы, ауадағы азот молекуласы белгілі бір қысымда – 78%, жалпы қысымда
- 17. Парижде медицинадан дәріс алып, сонан соң Клод Бертолленің Политехникалық мектебінің лабораториясында химик болып жұмыс атқарды. 1811
- 18. Негізгі ғылыми зерттеу жұмыстары: Жалпы химия және бейорганикалық химия саласына арналды. 1811 жылы жеңіл жарылғыш заттармен
- 19. Алексис Терез Пти Францияда Везуле қаласында туылды. 1809 жылы Парижде политехникалық мектепті бітіріп, 1810 ж Париж
- 20. Негізгі ғылыми зерттеу жұмыстары: П. Дюлонгпен біріге отыра бос денені суытқан уақыттағы өзгерістерді зерттеді, (1818) қыздырылған
- 21. Дюлонг- Пти ережесі Дюлонгтің ең басты ғылыми жетістігі 1819 жылы Пти екеуінің бірігіп анықтаған қатты дененің
- 22. БӨЛМЕ ТЕМПЕРАТУРАСЫНДА ҚАТТЫ ЗАТТАРДЫҢ МОЛЯРЛЫҚ ЖЫЛУ СЫЙЫМДЫЛЫҒЫ 3R ЖАҚЫН БОЛАДЫ. R— универсал газ тұрақтысы Қатты заттың
- 23. ҚАЛЫПТЫ ТЕМПЕРАТУРАДА КЕЙБІР ХИМИЯЛЫҚ ЭЛЕМЕНТТЕРДІҢ ЖЫЛУ СЫЙЫМДЫЛЫҒЫНЫҢ ЭКСПЕРИМЕНТАЛЬДІ МӘНДЕРІНІҢ КӨРСЕТКІШТЕРІ КЕСТЕДЕ КЕЛТІРІЛГЕН: Дюлонг- Пти ережесі
- 24. Қатты элементар бөлшектердің атомдық массасының туындысының меншікті жылу сыйымдылыққа қатынасы тұрақты өлшем болып табылады. Бұл заңдылық
- 25. П.Дюлонг және А.Пти (1819 ) ережесі бойынша элементтердің атомдық массаларын анықтау (молярлы массасын анықтау). Металдардың жылу
- 26. Көп заттардың меншікті жылу сыйымдылықтары тәжірибе жүзінде анықталады. Мұнан соң, сол заттың меншікті жылу сыйымдылығын 26,0
- 28. Еске түсіре кететін жай, жекеленген атом, молекулалармен өлшеулер жүргізу мүмкін болмағандықтан біз тәжірибе жүзінде ылғи макроскопиялық
- 30. Скачать презентацию

























 Гетерофункциональные соединения, участвующие в процессах жизнедеятельности
Гетерофункциональные соединения, участвующие в процессах жизнедеятельности Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов
Гормоны. Классификация гормонов. Общие свойства. Биохимия стероидных гормонов Изотопы Подготовила Кузнецова Даша
Изотопы Подготовила Кузнецова Даша  Презентация по Химии "Углеводы или сахариды" - скачать смотреть
Презентация по Химии "Углеводы или сахариды" - скачать смотреть  Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти
Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти Электрохимические методы в радиохимии
Электрохимические методы в радиохимии Адсорбция
Адсорбция Полимеры. Протезы трахеи
Полимеры. Протезы трахеи Явление изоморфизма в геохимии
Явление изоморфизма в геохимии Особенности строения атома углерода. Гибридизация
Особенности строения атома углерода. Гибридизация Правила ДСС
Правила ДСС Сера. Аллотропные модификации
Сера. Аллотропные модификации Эндогенная серия. Карбонатитовая группа
Эндогенная серия. Карбонатитовая группа Обмен нуклеопротеинов. (Лекция 17)
Обмен нуклеопротеинов. (Лекция 17) Научные фокусы. Лавовая лампа
Научные фокусы. Лавовая лампа Рідкі кристали та їх властивості Підготувала Кравченко Дарина
Рідкі кристали та їх властивості Підготувала Кравченко Дарина  Багатоядерні ароматичні сполуки
Багатоядерні ароматичні сполуки Химический элемент - америций
Химический элемент - америций Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау
Хинолин және хинуклидин, 4- жағдайда алмасқан хинолин туындыларының дәрілік заттарын талдау Периодическая система. Закономерности изменения свойств
Периодическая система. Закономерности изменения свойств Химические элементы. Викторина
Химические элементы. Викторина Алкены. Присоединение простых веществ
Алкены. Присоединение простых веществ Электромагнитное облучение. Радиоактивное загрязнение
Электромагнитное облучение. Радиоактивное загрязнение Кислородосодержащие органические соединения
Кислородосодержащие органические соединения Метаболизм аммиака. Катаболизм углеродного скелета аминокислот. (Лекция 3)
Метаболизм аммиака. Катаболизм углеродного скелета аминокислот. (Лекция 3) Тонколистовой металл и проволока
Тонколистовой металл и проволока Система микросомального окисления
Система микросомального окисления Жидкостная хроматография
Жидкостная хроматография