Слайд 5

Оформление расчетов в задачах
Расчет по закону эквивалентов при прямом титровании
При аргентометрическом
определении хлорид-ионов на титрование 20,00 мл раствора хлорида натрия затрачено 18,00 мл стандартизованного раствора нитрата серебра с молярной концентрацией 0,0459 моль/л. Рассчитайте молярную концентрацию, титр раствора хлорида натрия и массу хлорида натрия в растворе.
NaCl + AgNO3 = AgCl↓ + NaNO3
n(NaCl ) = n( AgNO3 )
C( NaCl ) ∙ V( NaCl ) = С(AgNO3) ·V(AgNO3)
C( NaCl ) = С(AgNO3) ·V(AgNO3 )/ V( NaCl )
C( NaCl ) = 0,0459 моль/л · 18,00 мл/ 20,00 мл = 0,0413 моль/л
Т (NaCl) = С( NaCl ) ∙ M( NaCl ) ∙10-3 = 0,0413 моль/л · 58,5 г/моль· 10-3 = 0,002416 г/мл
m(NaCl) = C(NaCl) ∙ M(NaCl) ∙ VК = 0,0413 моль/л ∙ 58,5 г/моль ∙ 0,02 л = 0,0483г









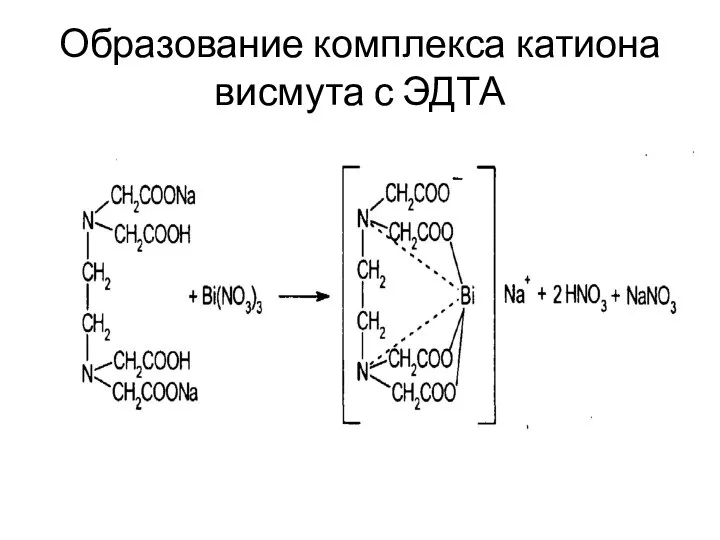
 Органические вещества. Предмет органической химии
Органические вещества. Предмет органической химии Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Кислородсодержащие. Углеводы. Подготовка к ЕГЭ
Кислородсодержащие. Углеводы. Подготовка к ЕГЭ Буферные растворы
Буферные растворы Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Консерванты для косметики и парфюмерных изделий
Консерванты для косметики и парфюмерных изделий Получение калийной селитры
Получение калийной селитры Кристаллическая структура
Кристаллическая структура Амиды кислот. Азо- и диазосоединения
Амиды кислот. Азо- и диазосоединения Сернистый ангидрид SO2. Диоксид серы
Сернистый ангидрид SO2. Диоксид серы ЙОД
ЙОД  Силикатная промышленность
Силикатная промышленность Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Презентация по Химии "Первичная переработка нефти" - скачать смотреть бесплатно
Презентация по Химии "Первичная переработка нефти" - скачать смотреть бесплатно Структура и физическое состояние полимеров
Структура и физическое состояние полимеров Фізичні та хімічні явища. (7 клас)
Фізичні та хімічні явища. (7 клас) Тема: Ионные уравнения реакции Вспомним реакцию нейтрализации.
Тема: Ионные уравнения реакции Вспомним реакцию нейтрализации.  Нина Кара 24 группа коррозия металлов
Нина Кара 24 группа коррозия металлов Алифатические углеводороды. Алканы, их свойства
Алифатические углеводороды. Алканы, их свойства Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4)
Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4) Выполнила студентка ХБ-4 Ширяева София
Выполнила студентка ХБ-4 Ширяева София Химические реакции. Скорость реакции
Химические реакции. Скорость реакции Механика полимеров
Механика полимеров Соли «Na2SO4»
Соли «Na2SO4» Приборы для измерения температуры
Приборы для измерения температуры Етилен і ацетилен – ненасичені вуглеводні
Етилен і ацетилен – ненасичені вуглеводні Химические реакции 11 кл Учитель химии МОУ СОШ с.Ильинское МО «Томаринский городской округ» Сахалинской области Чуб И.В.
Химические реакции 11 кл Учитель химии МОУ СОШ с.Ильинское МО «Томаринский городской округ» Сахалинской области Чуб И.В. Белки. Структуры белков
Белки. Структуры белков