Содержание
- 2. ИССЛЕДОВАНИЕ УРАВНЕНИЯ СЖИМАЕМОСТИ ПРИ ВЫСОКИХ ПЛОТНОСТЯХ ГАЗОВ НА ПРИМЕРЕ АРГОНА. Научный руководитель: Захарова Оксана Дмитриевна Июнь,
- 3. Содержание: Теоретические основы построения вириального уравнения состояния; Вывод модифицированных вириальных коэффициентов (МВК) в модели Апфельбаума-Воробьёва. Оценка
- 4. Вириальное уравнение состояния Уравнение Менделеева-Клапейрона: Одним из хорошо изученных УС является вириальное разложение, записанное в виде
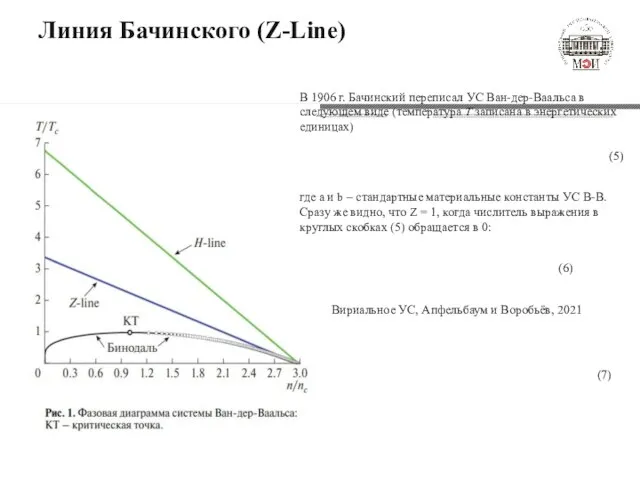
- 5. Линия Бачинского (Z-Line) В 1906 г. Бачинский переписал УС Ван-дер-Ваальса в следующем виде (температура Т записана
- 6. Линия Бачинского (Z-Line) Покажем, что для вириального ряда, контур Z=1 тоже может быть прямой линией, как
- 7. Вывод модифицированных вириальных коэффициентов (МВК) Рассмотрим Z-линию: Введем понятие эффективной температуры, которая используется для расчёта модифицированных
- 8. Вывод модифицированных вириальных коэффициентов (МВК) Аналогичным образом раскладываются в ряды все вириальные коэффициенты, и получившееся выражения
- 9. Анализ поведения модифицированных вириальных коэффициентов DS Воробьёв и Апфельбаум рассмотрели коэффициенты DS для системы частиц, взаимодействующих
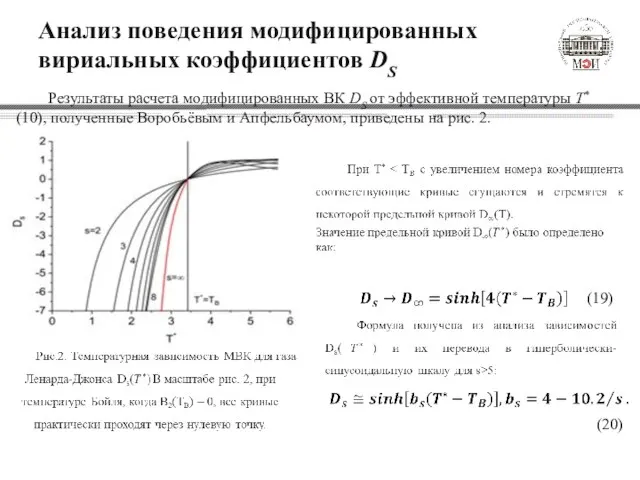
- 10. Анализ поведения модифицированных вириальных коэффициентов DS Результаты расчета модифицированных ВК DS от эффективной температуры T* (10),
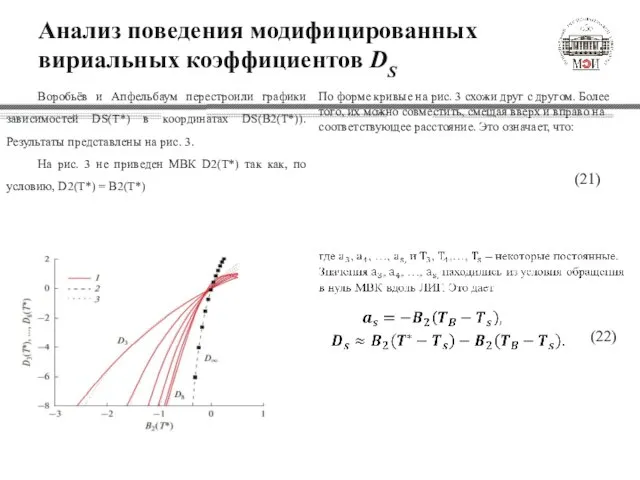
- 11. Анализ поведения модифицированных вириальных коэффициентов DS Воробьёв и Апфельбаум перестроили графики зависимостей DS(T*) в координатах DS(B2(T*)).
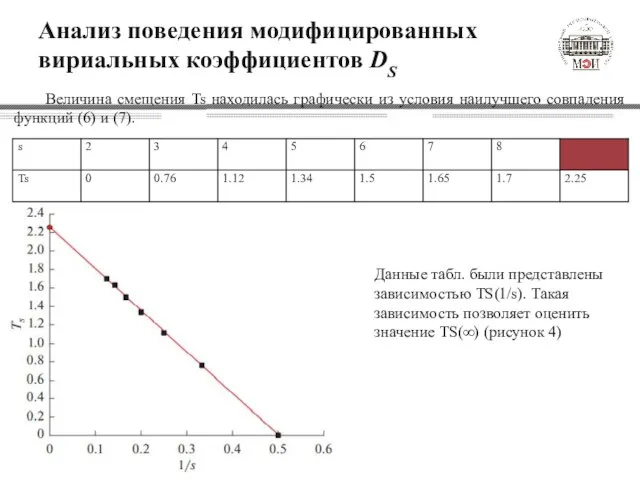
- 12. Анализ поведения модифицированных вириальных коэффициентов DS Величина смещения Ts находилась графически из условия наилучшего совпадения функций
- 13. Анализ поведения модифицированных вириальных коэффициентов DS Как видно из рис. 4, зависимость TS от s аппроксимируется
- 14. Малоконстантное модифицированное УС В итоге получено следующее УС: (26) (27) (28)
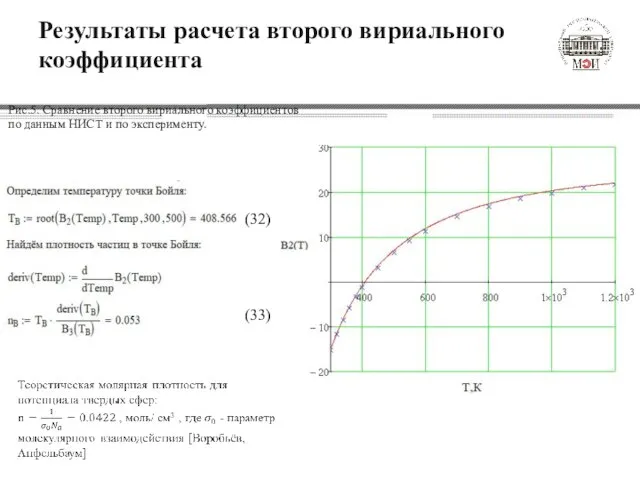
- 15. Результаты расчета второго вириального коэффициента Рис.5. Сравнение второго вириального коэффициентов по данным НИСТ и по эксперименту.
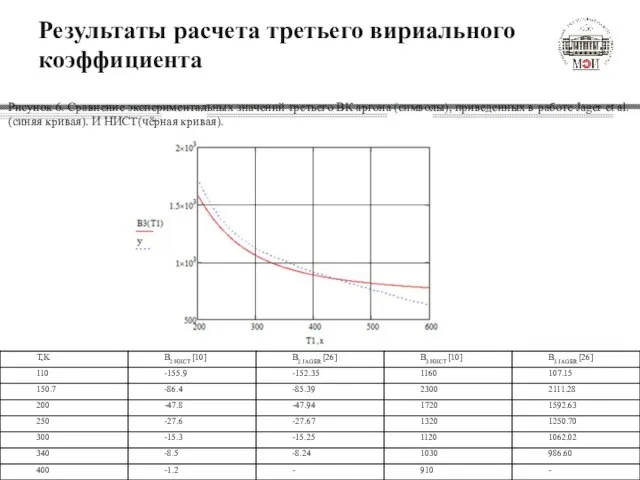
- 16. Результаты расчета третьего вириального коэффициента Рисунок 6. Сравнение экспериментальных значений третьего ВК аргона (символы), приведенных в
- 17. Уравнение Z-линий с модифиц. вириал. коэфф. (34) (35) (36) (37) (38) (39)
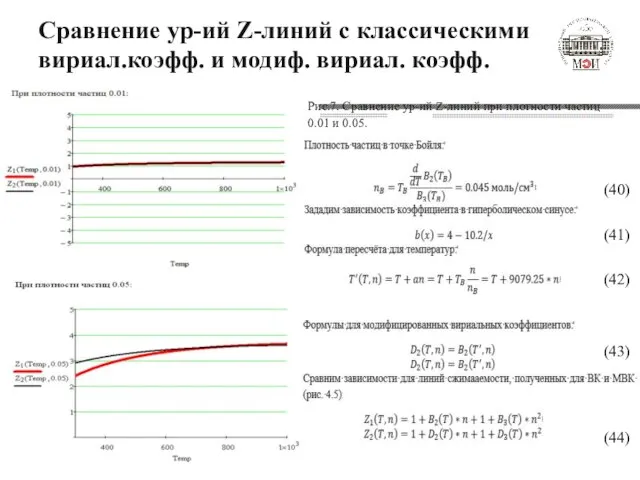
- 18. Сравнение ур-ий Z-линий с классическими вириал.коэфф. и модиф. вириал. коэфф. Рис.7. Сравнение ур-ий Z-линий при плотности
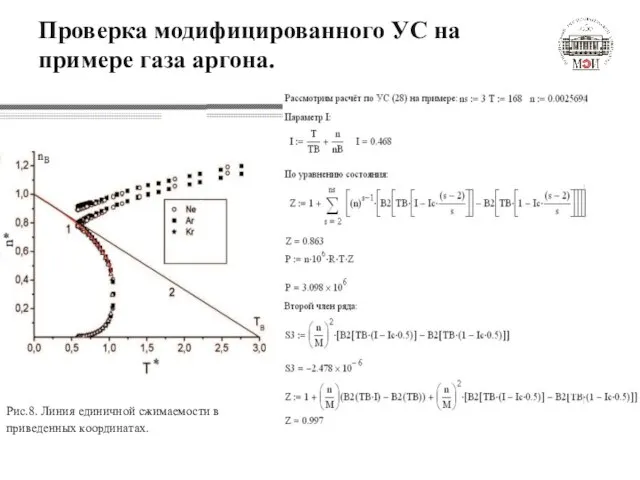
- 19. Проверка модифицированного УС на примере газа аргона. Рис.8. Линия единичной сжимаемости в приведенных координатах.
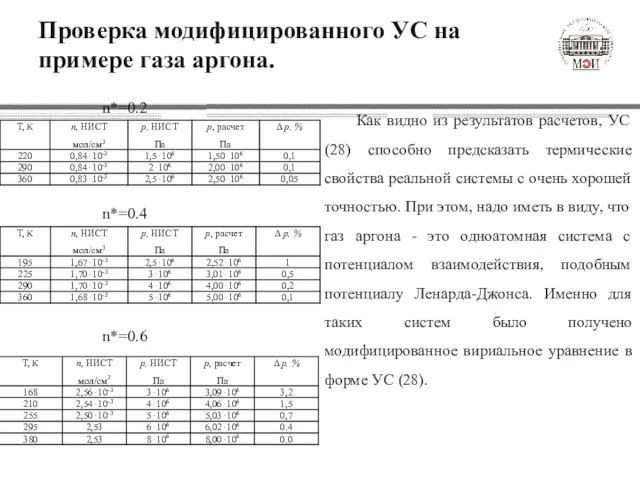
- 20. Проверка модифицированного УС на примере газа аргона. n*=0.2 n*=0.4 n*=0.6 Как видно из результатов расчетов, УС
- 21. Выводы 1) Теоретический расчёт второго вириального коэффициента аргона совпадает с экспериментальными данными НИСТ. Расчёт третьего вириального
- 23. Скачать презентацию











 Изучение содержания углекислого газа в классном помещении и определение оптимальных условий для проветривания. Муниципальное об
Изучение содержания углекислого газа в классном помещении и определение оптимальных условий для проветривания. Муниципальное об Гноеродные (пиогенные) кокки
Гноеродные (пиогенные) кокки Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Зат алмасу (көмірсу, май)
Зат алмасу (көмірсу, май) КОЛЕКЦІЯ ВОЛОКОН
КОЛЕКЦІЯ ВОЛОКОН  Самоцветы в реальной жизни и в мультике
Самоцветы в реальной жизни и в мультике Липиды. Тема 10
Липиды. Тема 10 Производные индола
Производные индола Химическая термодинамика
Химическая термодинамика Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Рецепты литературы в химических опытах
Рецепты литературы в химических опытах Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Что такое нефть и как она появилась?
Что такое нефть и как она появилась? Электрохимия. Электродика
Электрохимия. Электродика Вторая главная подгруппа ПС
Вторая главная подгруппа ПС Медь и сплавы
Медь и сплавы Химическое равновесие. Необратимые и обратимые реакции
Химическое равновесие. Необратимые и обратимые реакции Квантовая химия
Квантовая химия Уральские самоцветы
Уральские самоцветы Углеводы. Молекулярные формулы
Углеводы. Молекулярные формулы Гидроксид натрия
Гидроксид натрия Теория валентных связей
Теория валентных связей Природний газ
Природний газ Модуль Химия на кухне. Жиры
Модуль Химия на кухне. Жиры SNAP i.d. Workflow Value Proposition
SNAP i.d. Workflow Value Proposition Органическое топливо. Теплота сгорания топлива
Органическое топливо. Теплота сгорания топлива Свободные радикалы и болезни человека
Свободные радикалы и болезни человека Структура и текстура магматических пород
Структура и текстура магматических пород