Содержание
- 2. Изотонические растворы ( от гр. Isos – равный; tonus – давление ) Это растворы, у которых
- 3. Случаи, когда требование изотоничности обязательно : Растворы для внутрисосудистого введения Растворы для введения в спинномозговую и
- 4. Методы расчета изотонических концентраций растворов На основании газовых законов ( Вант – Гоффа); Криоскопический: по закону
- 5. На основании газовых законов (Вант – Гоффа) По уравнению Менделеева-Клапейрона Количество вещества (m), необходимое для V(мл)
- 7. Расчеты с применением изотонических эквивалентов по натрия хлориду Изотонический эквивалент ( Е ) лекарственного вещества по
- 8. Расчеты с применением изотонических эквивалентов по натрия хлориду Количество вещества m (г) для получения V (мл)
- 9. Требования к изотоническим растворам: Осмолярность – это характеристика растворов, выражающая их осмотическое давление через суммарную концентрацию
- 10. Требования к изотоническим растворам Наряду с понятием «осмолярность» используется понятие «осмоляльность». Отличие этих величин заключается в
- 13. Скачать презентацию










 Презентация по Химии "Явления природы.Физические явления. Химические явления." - скачать смотреть
Презентация по Химии "Явления природы.Физические явления. Химические явления." - скачать смотреть  Свободные радикалы и болезни человека
Свободные радикалы и болезни человека Презентация по Химии "Нефть. Крекинг" - скачать смотреть
Презентация по Химии "Нефть. Крекинг" - скачать смотреть  Презентация по Химии "Презентація на тему : «Нітратні добрива в продукції СГ. Їх вплив на наше здоров’я»" - скачать смотреть бе
Презентация по Химии "Презентація на тему : «Нітратні добрива в продукції СГ. Їх вплив на наше здоров’я»" - скачать смотреть бе Внесение минеральных удобрений
Внесение минеральных удобрений Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Газовая хроматография
Газовая хроматография Химия воды
Химия воды Презентация по Химии "Презентация Пестициды" - скачать смотреть
Презентация по Химии "Презентация Пестициды" - скачать смотреть  Изомеризация пентан-гексановой фракции
Изомеризация пентан-гексановой фракции Роль химии в жизни человека
Роль химии в жизни человека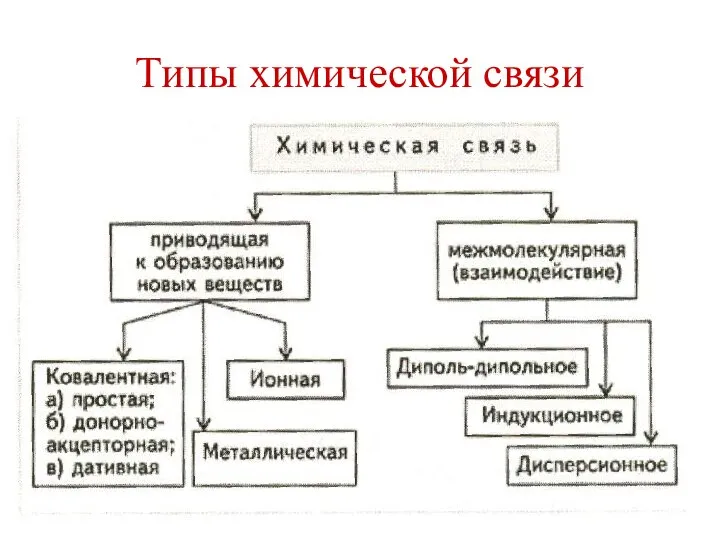 Типы химической связи
Типы химической связи  Химические свойства оксидов
Химические свойства оксидов Термодинамика. Химическое равновесие. Кинетика
Термодинамика. Химическое равновесие. Кинетика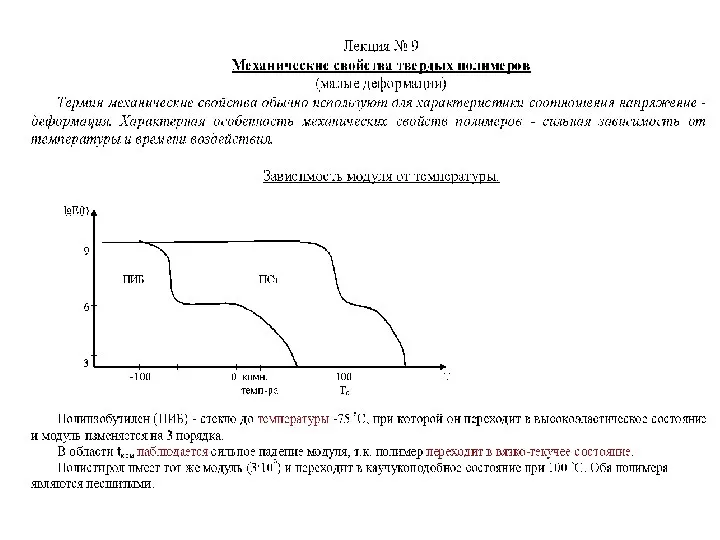 Механические свойства твердых полимеров, малые деформации. (Лекция 9)
Механические свойства твердых полимеров, малые деформации. (Лекция 9) Linear form of polyphenylsilsesquioxanes
Linear form of polyphenylsilsesquioxanes Сложные эфиры
Сложные эфиры Декаплінг. Ядерний ефект оверхаузера. Динамічні ефекти в ямр
Декаплінг. Ядерний ефект оверхаузера. Динамічні ефекти в ямр Изучение стереохимии циклических формалей глицерина методом ЯМР-спектроскопии
Изучение стереохимии циклических формалей глицерина методом ЯМР-спектроскопии Алкины. Физические и химические свойства
Алкины. Физические и химические свойства Место антацидов в современных схемах лечения кислотозависимых заболеваний
Место антацидов в современных схемах лечения кислотозависимых заболеваний Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Выделение низших олефинов. Разделение непредельных газов
Выделение низших олефинов. Разделение непредельных газов История мыловарения. Моющее действие мыла
История мыловарения. Моющее действие мыла Ерітінділер түрлері. Идеал ертітінділер және реал ерітінділер. Ерітіндінің пайыздық концентрациясына eсептер
Ерітінділер түрлері. Идеал ертітінділер және реал ерітінділер. Ерітіндінің пайыздық концентрациясына eсептер Обед под микроскопом. Минеральные вещества
Обед под микроскопом. Минеральные вещества Хлор. Состав. Строение
Хлор. Состав. Строение Этиленгликоль. Физические свойства
Этиленгликоль. Физические свойства