Содержание
- 2. Теории кислот и оснований Электролитическая теория С.Аррениуса Протолитическая теория Бренстеда - Лоури (кислота – донор протона,
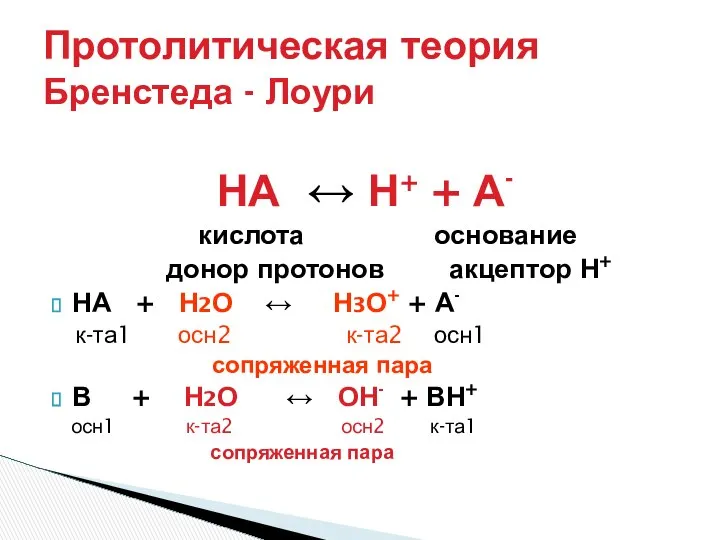
- 3. Протолитическая теория Бренстеда - Лоури НА ↔ Н+ + А- кислота основание донор протонов акцептор Н+
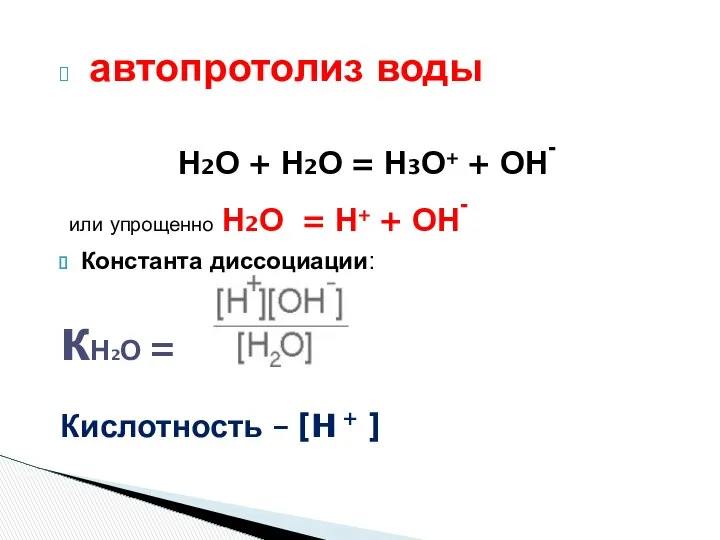
- 4. автопротолиз воды Н2О + Н2О = Н3О+ + ОН- или упрощенно Н2О = Н+ + ОН-
- 5. Вывод ионного произведения воды кН2О = =1.86 10 -16 [Н2О] = 1000/18= m /М=55,5 моль/л [Н+][ОН-]
- 6. Для удобства в расчетах пользуются величинами водородного и гидроксильного показателей рH и рОН, pH - power
- 7. [H+] = [OH-] = 10-7 моль/л рН = 7 нейтральная среда [H+] ‹ 10-7 моль/л рН
- 9. Кислотность раствора - [H+] рН = - lg C Сильные кислоты С → С [H+] =
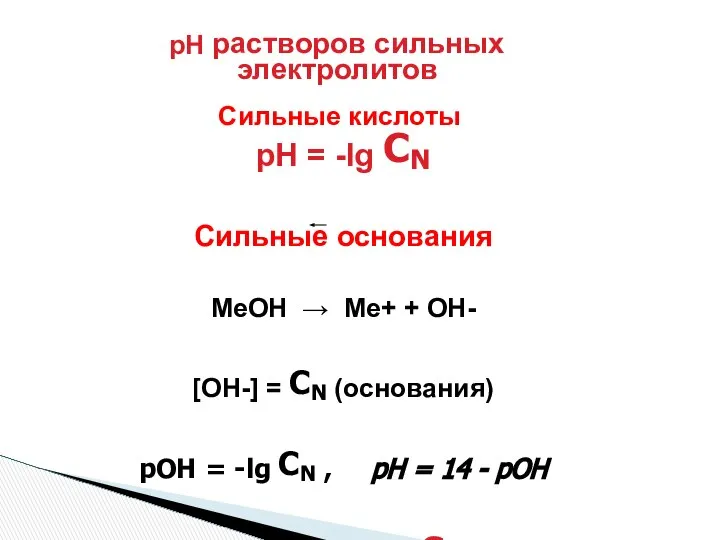
- 10. pH растворов сильных электролитов Сильные кислоты pH = -lg CN Сильные основания МеОН → Ме+ +
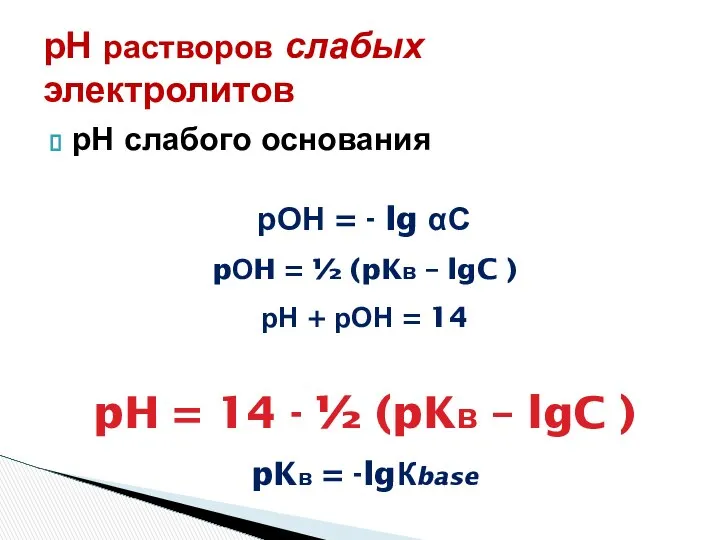
- 11. рН растворов слабых электролитов рН слабой кислоты рН = - lg αС pH = ½ (pKa
- 12. lg a = x 10x = a lg ab = lga + lgb lg a/b =
- 13. рН растворов слабых электролитов рН слабого основания рОН = - lg αС pОH = ½ (pKв
- 14. Протоны – катализаторы многих биохимических реакций Активность ферментов и гормонов зависит от рН Изменение рН ведет
- 15. Буферные растворы растворы, рН которых сохраняется при разбавлении водой или добавлении сильной кислоты или сильного основания
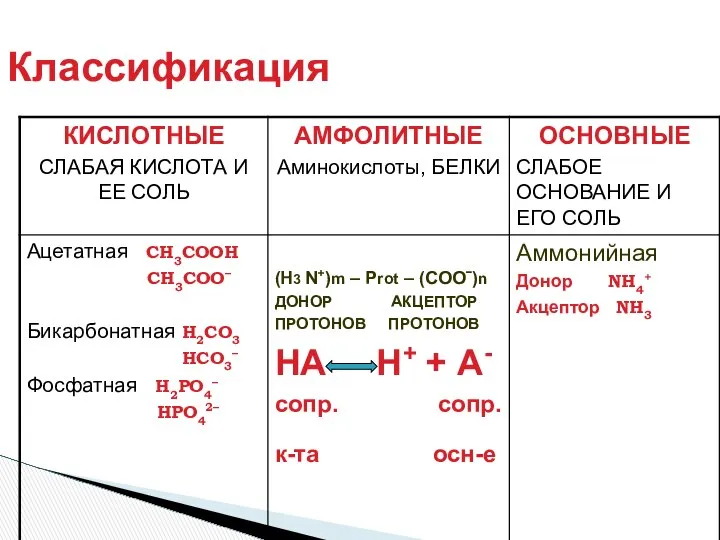
- 16. Классификация
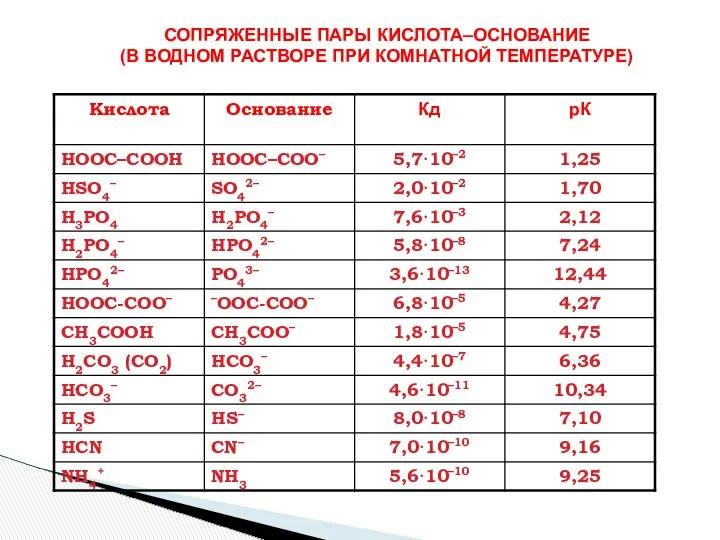
- 17. СОПРЯЖЕННЫЕ ПАРЫ КИСЛОТА–ОСНОВАНИЕ (В ВОДНОМ РАСТВОРЕ ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ)
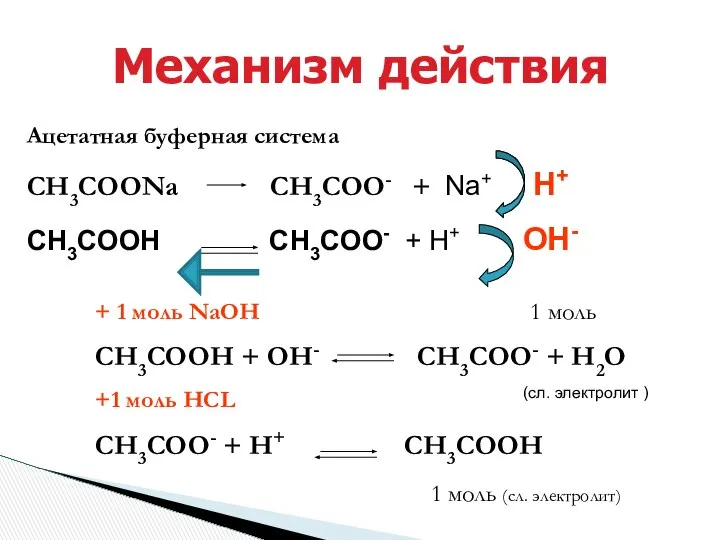
- 18. Механизм действия Ацетатная буферная система СН3СООNa СН3СОО- + Na+ Н+ СН3СООН СН3СОО- + Н+ ОН- +
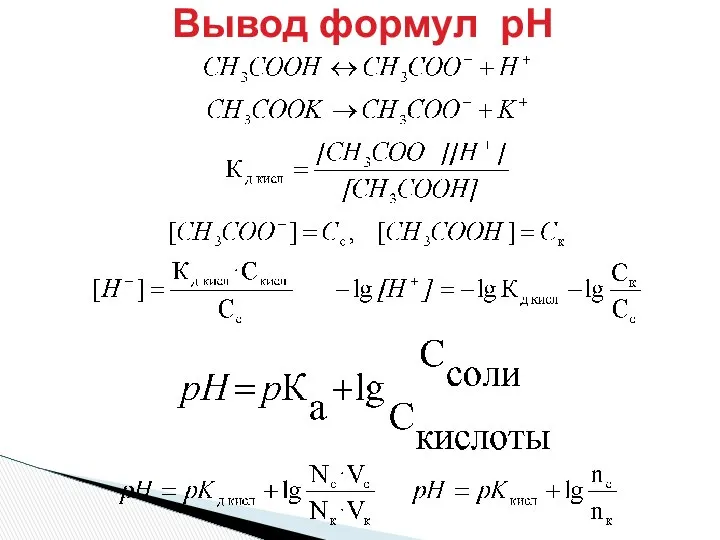
- 19. Вывод формул рН
- 20. Уравнение Гендерсона-Хассельбаха
- 21. приготовление БУФЕРНЫХ РАСТВОРОВ 1. Смешивание готовых растворов компонентов системы: -для кислотной буферной системы pH = pKa
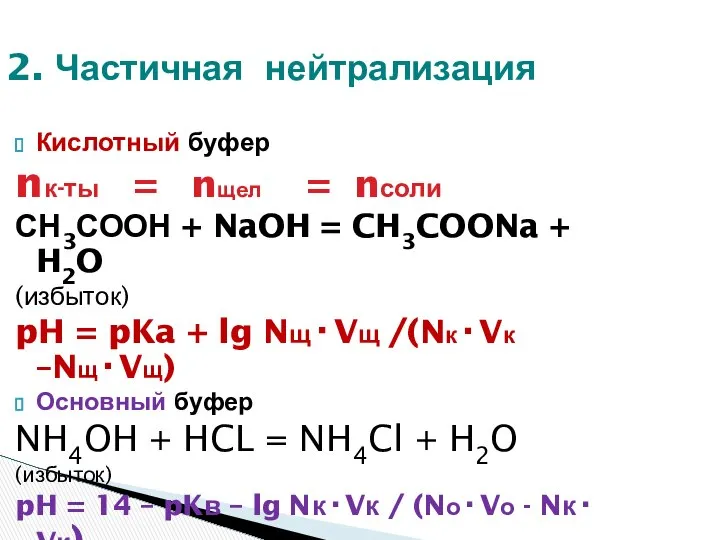
- 22. 2. Частичная нейтрализация Кислотный буфер nк-ты = nщел = nсоли СН3СООН + NaOH = CH3COONa +
- 23. БУФЕРНАЯ ЕМКОСТЬ МЕРА СПОСОБНОСТИ БУФЕРНОЙ СИСТЕМЫ ПРОТИВОСТОЯТЬ РЕАКЦИИ СРЕДЫ ПРИ ДОБАВЛЕНИИ КИСЛОТ ИЛИ ОСНОВАНИЙ ЕДИНИЦА ИЗМЕРЕНИЯ
- 24. БУФЕРНАЯ ЕМКОСТЬ ЗАВИСИТ : От количества компонентов 100 экв сол/100экв к-ты = 1 + 5 экв
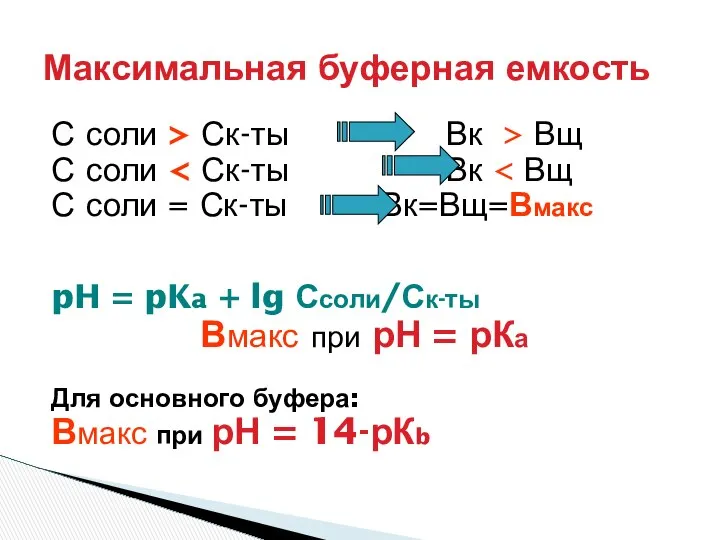
- 25. С соли > Ск-ты Вк > Вщ С соли С соли = Ск-ты Вк=Вщ=Вмакс pH =
- 26. Для приготовления буферного раствора с рН = 7.36 и максимальной емкостью необходимо использовать буферный раствор: 1)
- 27. БУФЕРНЫЕ СИСТЕМЫ ОРГАНИЗМА 1.Минеральные бикарбонатная (K) NaHCO3/H2CO3 фосфатная Na2HPO4/NaH2PO4 2. Белковые белковая гемоглобиновая 3. Аминокислотные
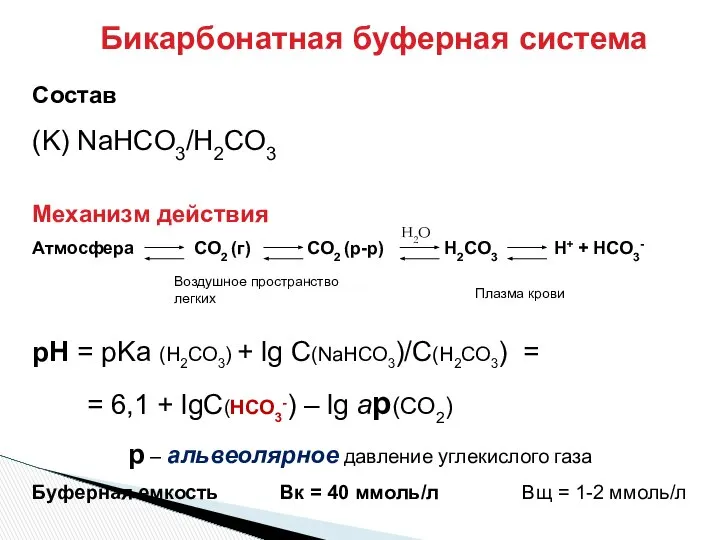
- 29. Бикарбонатная буферная система Состав (K) NaHCO3/H2CO3 Механизм действия Атмосфера СO2 (г) СO2 (р-р) H2СO3 H+ +
- 30. [НСО3–]:[СО2] = 20:1 Вк > Вщ Это отвечает особенностям метаболизма организма: Н2СО3 – до 13 моль/
- 31. [НСО3–] Щелочной резерв крови Число мл СО2, содержащееся в 100 мл крови (главным образом в виде
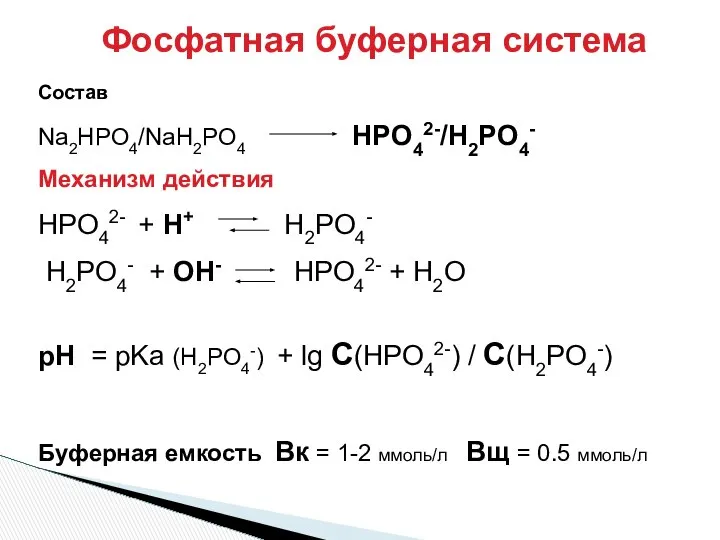
- 32. Фосфатная буферная система Состав Na2HPO4/NaH2PO4 HPO42-/H2PO4- Механизм действия HPO42- + H+ H2PO4- H2PO4- + OH- HPO42-
- 33. Сравнение мощности буферных систем крови УМЕНЬШЕНИЕ Гидрокарбонатная > Белковая > Фосфатная > Аминокислотная
- 34. Кооперативное действие буферных систем организма Kдисс.HHb рК = 8.2 рК = 6.1 рК = 6.95 Более
- 35. В легких: 1. HHb + O2→ HHbO2 2. HCO3ˉ + HHbO2 → HbO2ˉ + H2O +CO2↑
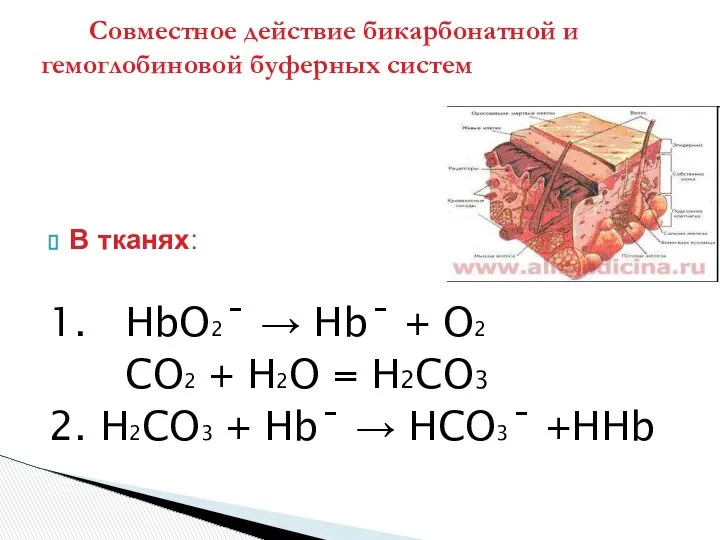
- 36. В тканях: 1. HbO2ˉ → Hbˉ + O2 CO2 + H2O = H2CO3 2. H2CO3 +
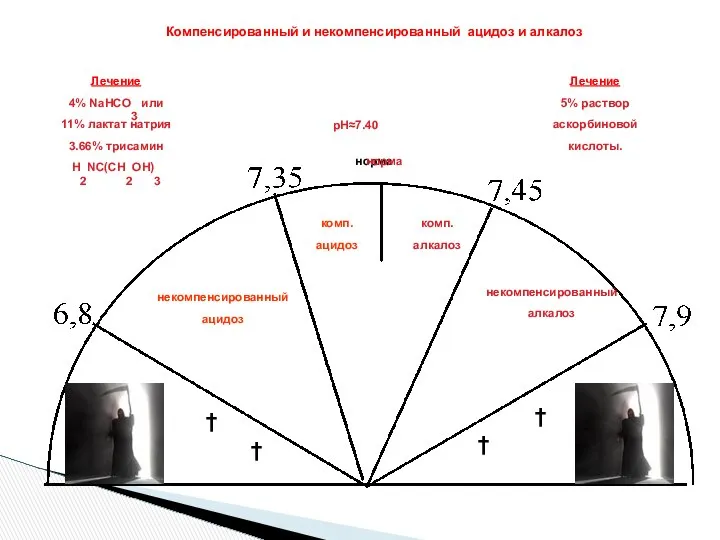
- 37. норма † † † † рН≈7.40 некомпенсированный ацидоз комп. ацидоз комп. алкалоз некомпенсированный алкалоз норма Компенсированный
- 41. Оцените кислотно-основное состояние крови больного на основании следующих показателей: р(СО2) = 55 мм рт.ст., рНплазмы крови
- 43. Скачать презентацию

![Вывод ионного произведения воды кН2О = =1.86 10 -16 [Н2О] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405647/slide-4.jpg)

![[H+] = [OH-] = 10-7 моль/л рН = 7 нейтральная среда](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405647/slide-6.jpg)

![Кислотность раствора - [H+] рН = - lg C Сильные кислоты](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405647/slide-8.jpg)











![[НСО3–]:[СО2] = 20:1 Вк > Вщ Это отвечает особенностям метаболизма организма:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405647/slide-29.jpg)
![[НСО3–] Щелочной резерв крови Число мл СО2, содержащееся в 100 мл](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405647/slide-30.jpg)






 Графические таблицы текущего цемента с 2 ПЛ
Графические таблицы текущего цемента с 2 ПЛ Марганец и его свойства
Марганец и его свойства 9 класс Урок №9. Углеводы. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А.
9 класс Урок №9. Углеводы. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А.  Круговорот серы в природе
Круговорот серы в природе Карбоновые кислоты
Карбоновые кислоты Химические свойства и получение насыщенных одноатомных спиртов
Химические свойства и получение насыщенных одноатомных спиртов Великие химики
Великие химики Липиды. Жиры
Липиды. Жиры Мило. Його склад, мийна дія. Синтетичні мийні засоби
Мило. Його склад, мийна дія. Синтетичні мийні засоби  Химиялық формула
Химиялық формула Буферные растворы. Буферная емкость
Буферные растворы. Буферная емкость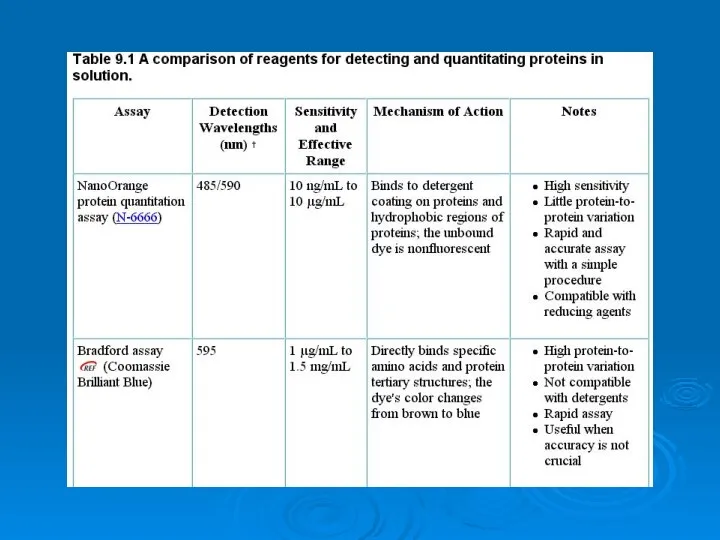 Analysis of proteins
Analysis of proteins Лекарственные вещества (определения и классификация)
Лекарственные вещества (определения и классификация) Валентные состояния атома углерода
Валентные состояния атома углерода Биологически активные вещества и их содержание в лекарственных растениях
Биологически активные вещества и их содержание в лекарственных растениях Нуклеиновые кислоты
Нуклеиновые кислоты «Знаки химических элементов. Относительная атомная масса химических элементов» Мартынова Полина Александровна, учитель хим
«Знаки химических элементов. Относительная атомная масса химических элементов» Мартынова Полина Александровна, учитель хим Презентация по Химии "Карбоновые кислоты 9 класс" - скачать смотреть
Презентация по Химии "Карбоновые кислоты 9 класс" - скачать смотреть  Микроэлементы. Химические элементы в клетках живых организмов. Химия и здоровье
Микроэлементы. Химические элементы в клетках живых организмов. Химия и здоровье Тема урока: «Карбонаты» Цель урока: Изучить химические свойства солей угольной кислоты – карбонатов и гидрокарбонатов; приобрес
Тема урока: «Карбонаты» Цель урока: Изучить химические свойства солей угольной кислоты – карбонатов и гидрокарбонатов; приобрес Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов
Разработка методов синтеза гомогенных катализаторов оксосинтеза бутиловых спиртов Технология получения гидропероксида изопропилбензола
Технология получения гидропероксида изопропилбензола Белоктар жөніңдегі ілім дамуының қысқаша тарихы
Белоктар жөніңдегі ілім дамуының қысқаша тарихы Презентация на тему: Молекулы
Презентация на тему: Молекулы Практикум по неорганической химии
Практикум по неорганической химии Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Устойчивость и коагуляция коллоидных растворов
Устойчивость и коагуляция коллоидных растворов Презентация Химический состав мороженного
Презентация Химический состав мороженного