Классификация дисперсных систем. Электрокинетические свойства и устойчивость коллоидных растворов. (Лекция 8)
Содержание
- 2. КЛАССИФИКАЦИЯ ДИСПЕРСНЫХ СИСТЕМ. ЭЛЕКТРОКИНЕТИЧЕСКИЕ СВОЙСТВА И УСТОЙЧИВОСТЬ КОЛЛОИДНЫХ РАСТВОРОВ Лекция №8 Лектор: к.х.н., доцент Иванова Надежда
- 3. Коллоидная химия ‒ … … наука о поверхностных явлениях и дисперсных системах. … наука о коллоидном
- 4. Основные понятия: Дисперсность ‒ мерой её служит удельная поверхность (Sуд). Sуд ‒ площадь раздела фаз, приходящаяся
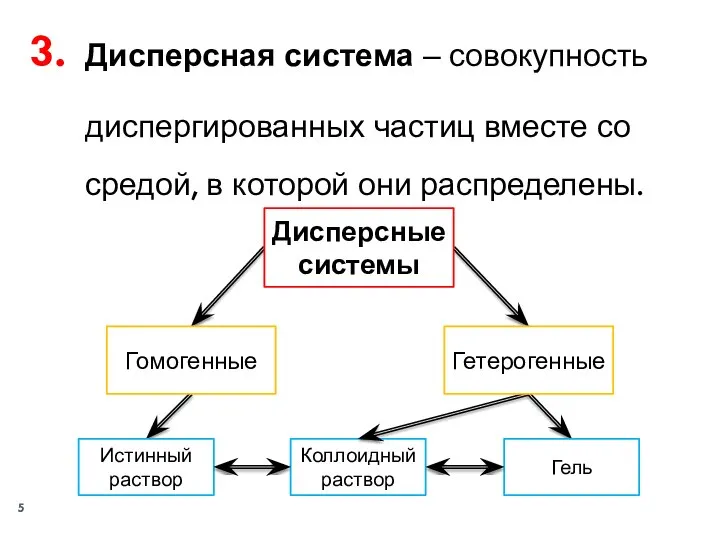
- 5. Дисперсная система ‒ совокупность диспергированных частиц вместе со средой, в которой они распределены. Дисперсные системы Гомогенные
- 6. Дисперсная фаза (ДФ) ‒ совокупность диспергированных частиц, размеры которых больше молекулярных. Дисперсионная среда (ДС) ‒ однородная
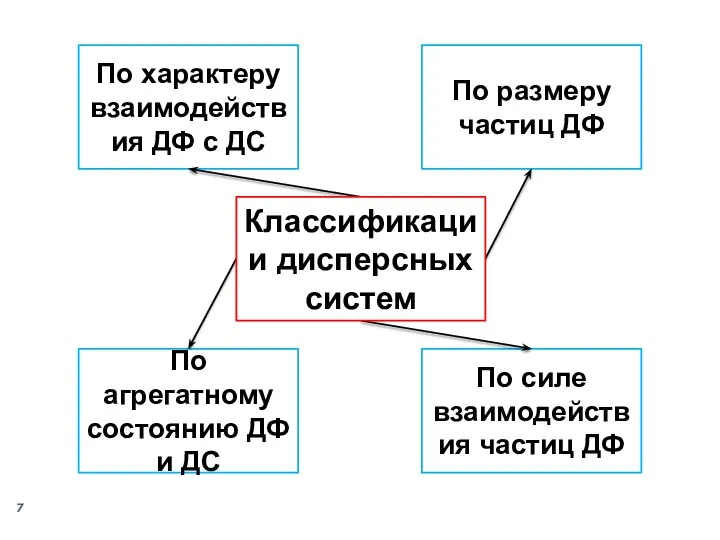
- 7. По размеру частиц ДФ По характеру взаимодействия ДФ с ДС По агрегатному состоянию ДФ и ДС
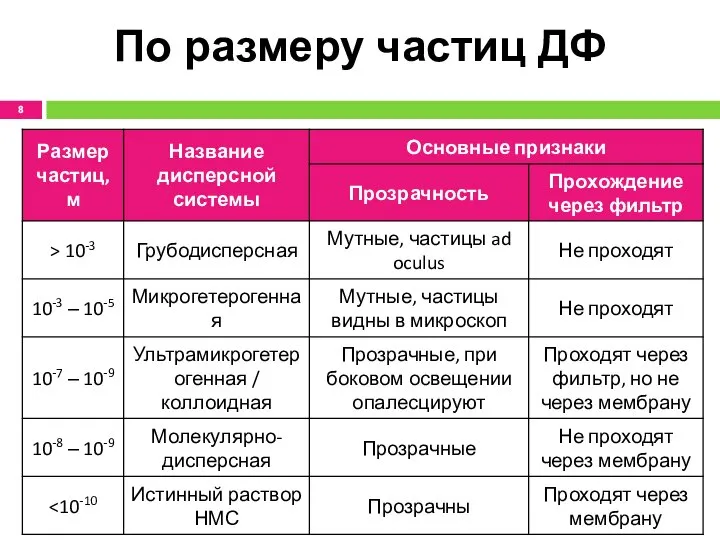
- 8. По размеру частиц ДФ
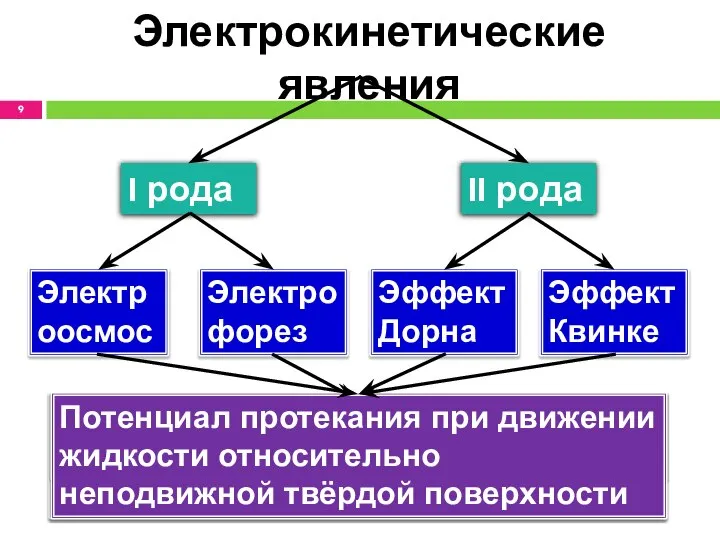
- 9. Электрокинетические явления I рода II рода Электрофорез Электроосмос Эффект Дорна Эффект Квинке Движение частиц ДФ в
- 10. Мицеллярная теория лиофобных золей Мицелла ‒ гетерогенная микросистема, состоящая из микрокристалла ДФ, окружённого сольватированными ионами стабилизатора.
- 11. Мицеллярная теория лиофобных золей – агрегат с адсорбированными на нём потенциалопределяющими ионами (ПОИ). – ионы, сообщающие
- 12. Мицеллярная теория лиофобных золей – ядро с адсорбционным слоем противоионов, являющаяся гигантским многозарядным ионом. Источником ПОИ
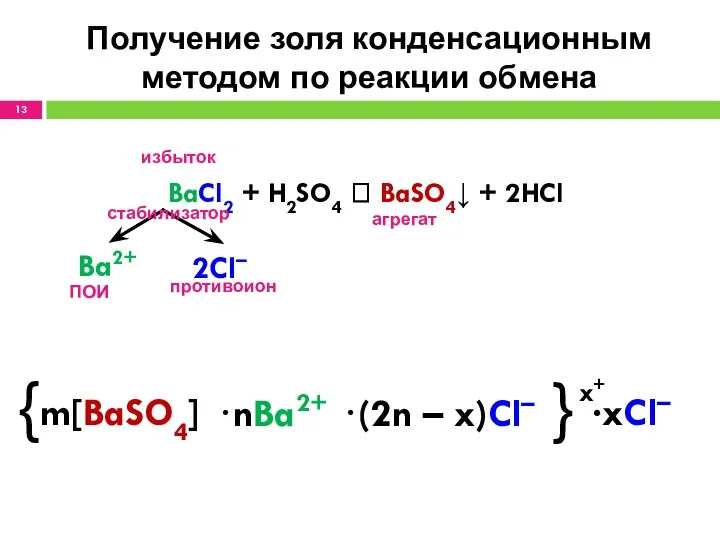
- 13. Получение золя конденсационным методом по реакции обмена BaCl2 + H2SO4 ? BaSO4↓ + 2HCl избыток агрегат
- 14. Мицелла {m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl– агрегат адсорбционный слой ядро гранула диффузионный слой
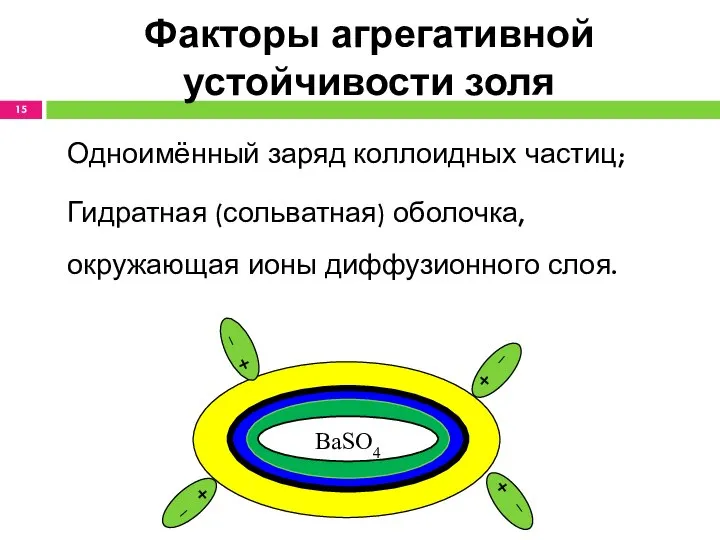
- 15. Факторы агрегативной устойчивости золя Одноимённый заряд коллоидных частиц; Гидратная (сольватная) оболочка, окружающая ионы диффузионного слоя. BaSO4
- 16. Возникновение ДЭС и потенциалов в мицелле {m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl– На границе
- 17. Возникновение ДЭС и потенциалов в мицелле По величине 0 ≤ ζ ζкрит. = ±30 мВ. При
- 18. Факторы, влияющие на ζ Концентрация стабилизатора. Состояние ИЭТ золя, ζ = 0. Золь разрушается. Концентрация посторонних
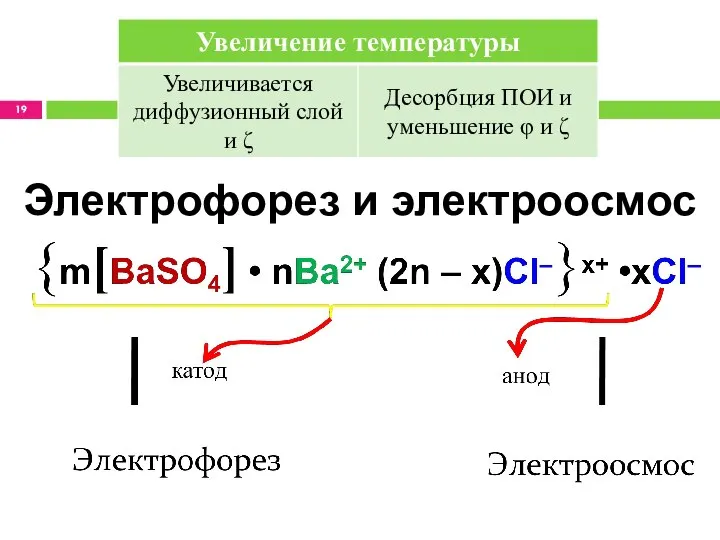
- 19. Электрофорез и электроосмос
- 20. Расчёт ζ Поскольку ζ обнаруживает себя при попадании мицеллы в электрическое поле, для его расчёта используются
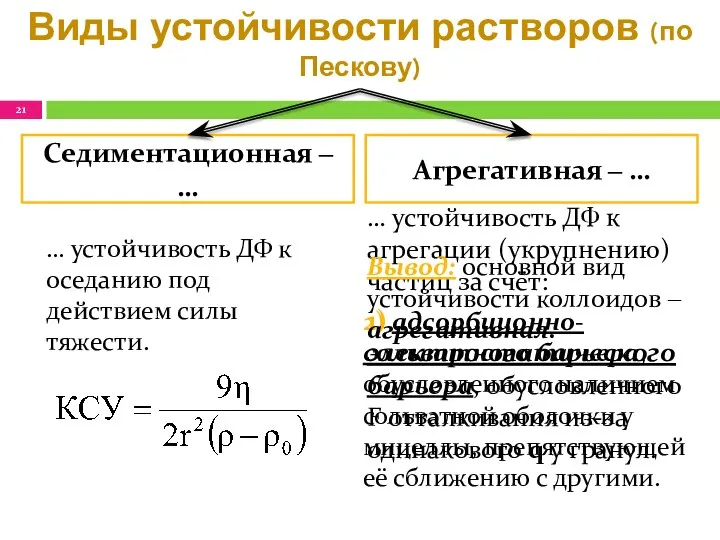
- 21. Виды устойчивости растворов (по Пескову) … устойчивость ДФ к агрегации (укрупнению) частиц за счёт: 1) электростатического
- 22. Коагуляция ‒ … … процесс слипания частиц, образование крупных агрегатов с потерей седиментационной и фазовой устойчивости
- 23. Факторы, вызывающие коагуляцию Увеличение концентрации золя приводит к уменьшению расстояния между частицами, на котором начинают действовать
- 24. Факторы, вызывающие коагуляцию Добавление электролитов наиболее сильное по 2-м причинам: из-за адсорбции ионов электролита на грануле
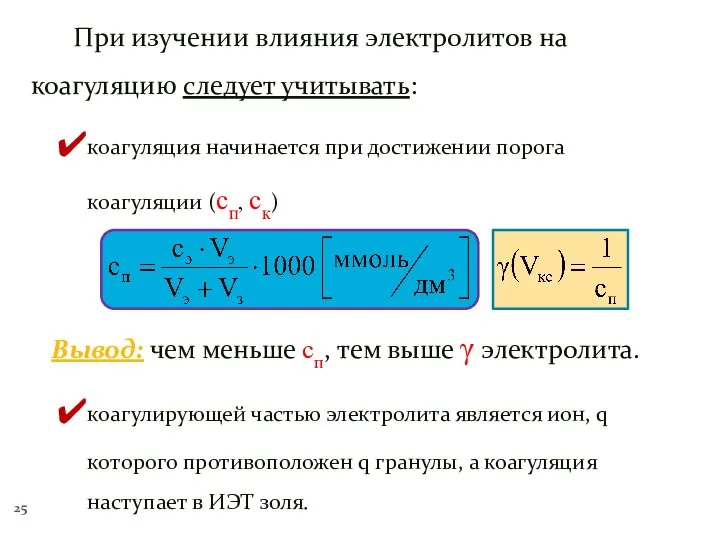
- 25. При изучении влияния электролитов на коагуляцию следует учитывать: коагуляция начинается при достижении порога коагуляции (сп, ск)
- 26. чем выше заряд коагулирующего иона, тем меньше сп и выше γ электролита. Правило Шульце ‒ Гарди
- 27. Правило Дерягина ‒ Ландау … … устанавливает связь между сп и зарядом коагулирующего иона. Теор.: Эксп.:
- 28. Способность ионов одного заряда к гидратации (лиотропные ряды) Факторы, вызывающие коагуляцию Li+ Na+ K+ Rb+ Cs+
- 29. Факторы, вызывающие коагуляцию «Ионы-партнёры», идущие в паре с коагулирующими ионами, уменьшают их γ в случае адсорбции
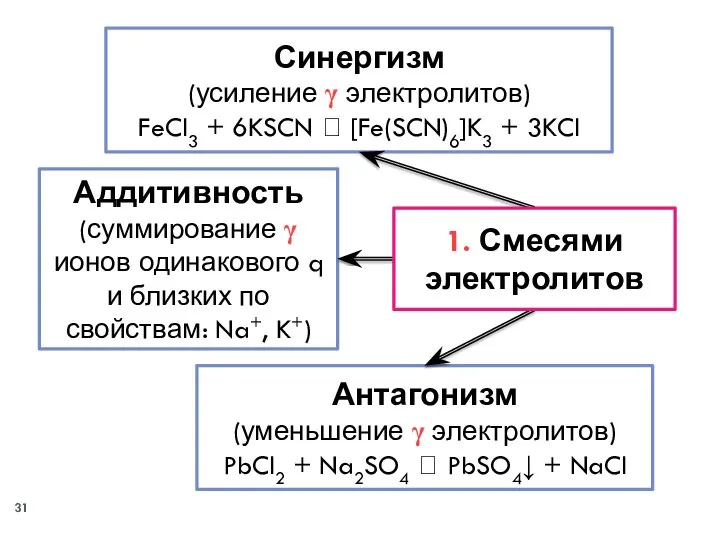
- 30. Смесями электролитов; Многозарядными ионами‒коагуляторами (чередование зон коагуляции); При смешивании коллоидов с гранулами разного по знаку заряда
- 31. Аддитивность (суммирование γ ионов одинакового q и близких по свойствам: Na+, K+) Антагонизм (уменьшение γ электролитов)
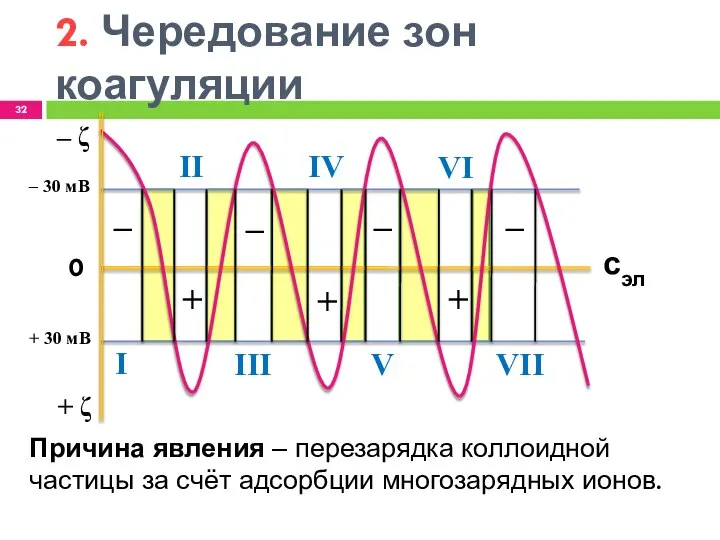
- 32. 2. Чередование зон коагуляции ‒ + + + ‒ ‒ ‒ ‒ ζ + ζ 0
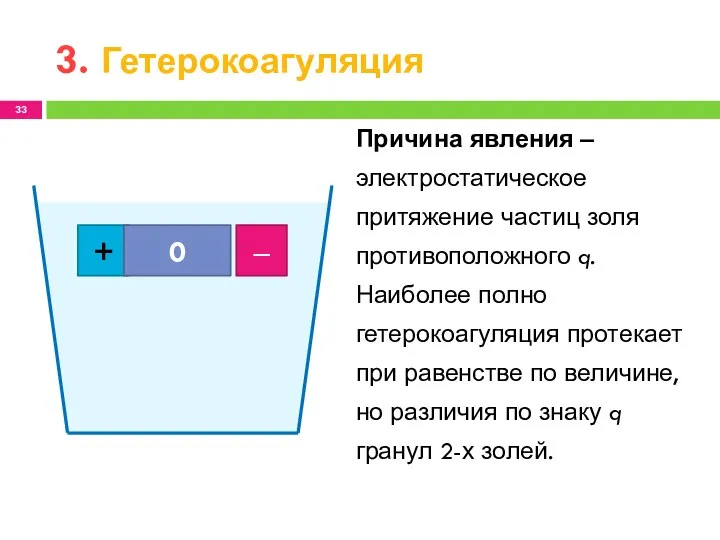
- 33. 3. Гетерокоагуляция + ‒ 0 Причина явления ‒ электростатическое притяжение частиц золя противоположного q. Наиболее полно
- 34. … вызвана добавлением очень малых количеств ВМС и понижает устойчивость коллоидов. … связана с особенностями ВМС:
- 35. Вывод: адсорбционный слой является механическим препятствием для иона ‒ коагулянта. …повышение устойчивости коллоидов добавлением ВМС в
- 36. Защитное число … … min масса ВМС (мг), достаточная для предотвращения 10 см3 гидрозоля от коагулирующего
- 37. Процесс перехода свежевыпавшего при коагуляции осадка во взвешенное состояние (золь) под влиянием пептизаторов ‒ б) адсорбция
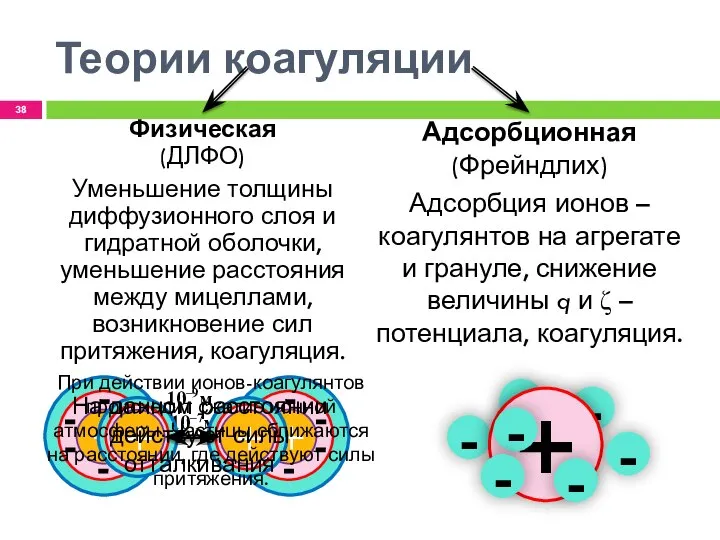
- 38. - - - Теории коагуляции Адсорбционная (Фрейндлих) Адсорбция ионов – коагулянтов на агрегате и грануле, снижение
- 40. Скачать презентацию







![Мицелла {m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl– агрегат адсорбционный](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408355/slide-13.jpg)
![Возникновение ДЭС и потенциалов в мицелле {m[BaSO4] • nBa2+ (2n –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408355/slide-15.jpg)















 Презентация по Химии "Гигиенические аспекты загрязнения пищевых продуктов чужеродными в-ми и меры профилактики" - скачать см
Презентация по Химии "Гигиенические аспекты загрязнения пищевых продуктов чужеродными в-ми и меры профилактики" - скачать см Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.
Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на. Рідкі кристали та їх властивості Підготувала Кравченко Дарина
Рідкі кристали та їх властивості Підготувала Кравченко Дарина  Взаимное влияние атомов в молекулах
Взаимное влияние атомов в молекулах Реакции по направлению процесса
Реакции по направлению процесса Классификация неорганических веществ. Оксиды. Автор: Калитина Тамара Михайловна Место работы: МОУ СОШ №3 с.Александров-Гай
Классификация неорганических веществ. Оксиды. Автор: Калитина Тамара Михайловна Место работы: МОУ СОШ №3 с.Александров-Гай  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Азотсодержащие органические соединения
Азотсодержащие органические соединения Типы химических реакций. Класс «оксиды»
Типы химических реакций. Класс «оксиды» Диссоциация кислот, щелочей и солей
Диссоциация кислот, щелочей и солей ОГЭ - 1. Экспериментальная» часть
ОГЭ - 1. Экспериментальная» часть Ртуть. Применение ртути и ее соединений
Ртуть. Применение ртути и ее соединений Слепочные материалы. Гипс
Слепочные материалы. Гипс Системы эвтектического типа
Системы эвтектического типа Разбираем задания
Разбираем задания Азот, свойства атома, химические и физические свойства
Азот, свойства атома, химические и физические свойства Пегматитовые месторождения
Пегматитовые месторождения Введение. Методы и средства обучения химии
Введение. Методы и средства обучения химии Электролиз расплавов и растворов электролитов
Электролиз расплавов и растворов электролитов Свойства химических элементов
Свойства химических элементов Место антацидов в современных схемах лечения кислотозависимых заболеваний
Место антацидов в современных схемах лечения кислотозависимых заболеваний Основы химической термодинамики. Термохимические расчеты
Основы химической термодинамики. Термохимические расчеты Культивирование растительных и животных клеток
Культивирование растительных и животных клеток Воздушные и тепловые свойства почв
Воздушные и тепловые свойства почв Химия в строительстве
Химия в строительстве Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти
Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти Методы пробоотбора и пробоподготовки
Методы пробоотбора и пробоподготовки Урок по химии в 11 классе. Провела Миронова О.А. МОУ Памятская СОШ.
Урок по химии в 11 классе. Провела Миронова О.А. МОУ Памятская СОШ.