Содержание
- 2. Амины алифатического ряда Амины - органические соединения, которые можно рассматривать как производные углеводородов, образованные в результате
- 3. Так как в аммиаке радикалами могут быть последовательно замещены все водородные атомы, существуют три группы аминов.
- 4. Амины могут содержать одну, две и более аминогрупп, соответственно различают моноамины, диамины и т.д. Следует иметь
- 5. С аминами тесно связаны органические вещества, являющиеся производными аммониевых соединений. Производные гидроксида аммония, содержащие в комплексном
- 6. [NH4]+ OH- гидроксид аммония гидроксид четырехзамещенного аммония (четвертичное аммониевое основание)
- 7. Номенклатура аминов По правилам Международной номенклатуры, если аминогруппа в соединении является главной, наличие ее обозначают окончанием
- 8. Для наименования первичных аминов или диаминов с первичными аминогруппами указанные окончания добавляются к названиям соответствующих одновалентных
- 9. Названия аминов могут быть произведены и от заместительных названий соответствующих углеводородов, тогда цифрами указывают атомы углерода
- 10. Названия вторичных и третичных аминов с одинаковыми радикалами образуются из названий этих радикалов и указывающих их
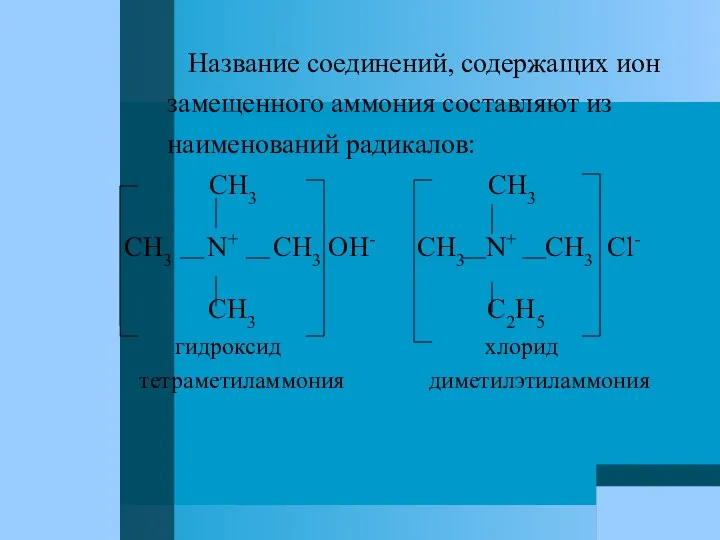
- 11. Название соединений, содержащих ион замещенного аммония составляют из наименований радикалов: CH3 CH3 CH3 N+ CH3 OH-
- 12. Химические свойства Как производные аммиака амины проявляют основные свойства и являются органическими основаниями. Подобно аммиаку амины
- 13. Водные растворы аминов можно представить как растворы гидроксидов замещенного аммония; в случае метиламина – гидроксида метиламмония
- 14. Под влиянием простейших алкильных радикалов основные свойства аминогруппы увеличиваются, поэтому амины жирного ряда являются более сильными
- 15. Увеличение основных свойств аминогруппы в аминах сравнительно с аммиаком объясняется электронодонорными свойствами алкильных радикалов, их способностью
- 16. Алкилы увеличивают общую электронную плотность атома азота, несущего неподеленную электронную пару, и, следовательно, его способность присоединять
- 17. CH3 NH2 + HCl CH3 NH3 Cl метиламин хлорид метиламмония CH3 NH2 + H2SO4 CH3 NH3
- 18. Едкие щелочи, как более сильные основания, вытесняют амины из их солей. CH3 NH3 Cl + NaOH
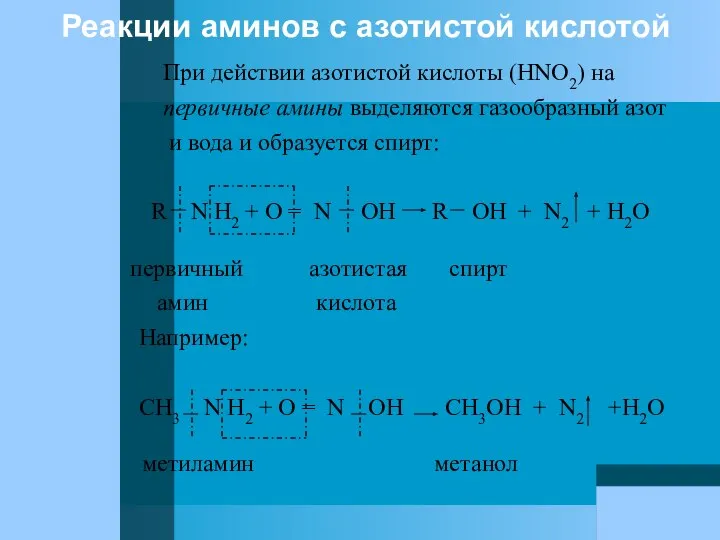
- 19. Реакции аминов с азотистой кислотой При действии азотистой кислоты (HNO2) на первичные амины выделяются газообразный азот
- 20. Вторичные амины при действии на них азотистой кислоты образуют нитрозамины: R R N H + HO
- 21. Например: CH3 CH3 N H + HO N = О N N = О +H2O CH3
- 22. Аминокислоты Аминокислотами называют карбоновые кислоты, в углеводородных радикалах которых один или несколько атомов водорода замещены остатками
- 23. Строение, изомерия и номенкулатура Изомерия аминокислот определяется положением аминогрупп по отношению к карбоксильным группам; строением углеродного
- 24. Простейшей является аминоуксусная (аминоэтановая) кислота; иначе ее называют глицином или гликоколом: CH3COOH H2N CH2 COOH уксусная
- 25. Химические свойства Вследствие наличия в молекулах аминокислот одновременно карбоксильных и аминогрупп они могут реагировать как кислоты
- 26. Амфотерность аминокислот Аминокислоты – амфотерные соединения, образующие соли как с кислотами, так и с основаниями. В
- 27. NH2 CH2 COOH + NaOH NH2 CH2 COONa + H2O натриевая соль глицина
- 28. Кислотная и основная группы внутри молекул аминокислот взаимодействуют друг с другом, благодаря этому молекулы аминокислот представляют
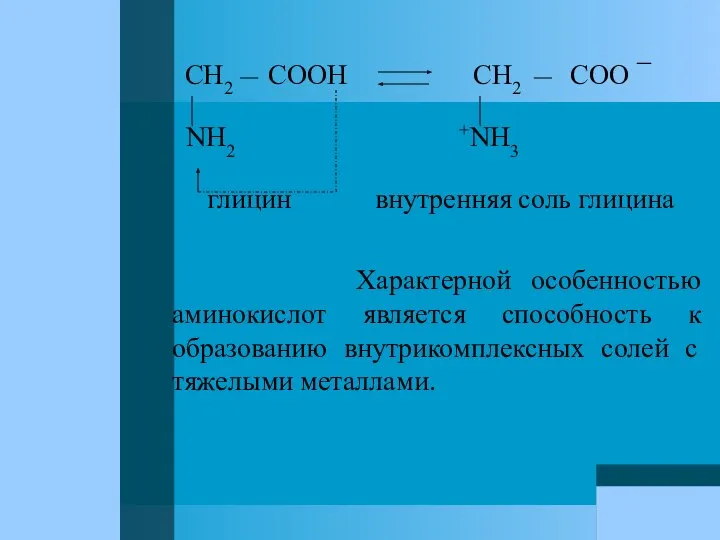
- 29. CH2 COOH CH2 COO ¯ NH2 +NH3 глицин внутренняя соль глицина Характерной особенностью аминокислот является способность
- 30. Реакции аминогрупп в аминокислотах Аминокислоты с первичными аминогруппами реагируют с азотистой кислотой подобно первичным аминам. СH3
- 31. Функциональные производные аминокислот Подобно незамещенным карбоновым кислотам, аминокислоты за счет карбоксильной группы образуют различные производные: сложные
- 32. Отличительные свойства α, β, γ и δ-аминокислот Различное взаимное расположение аминогрупп и карбоксильных групп в молекулах
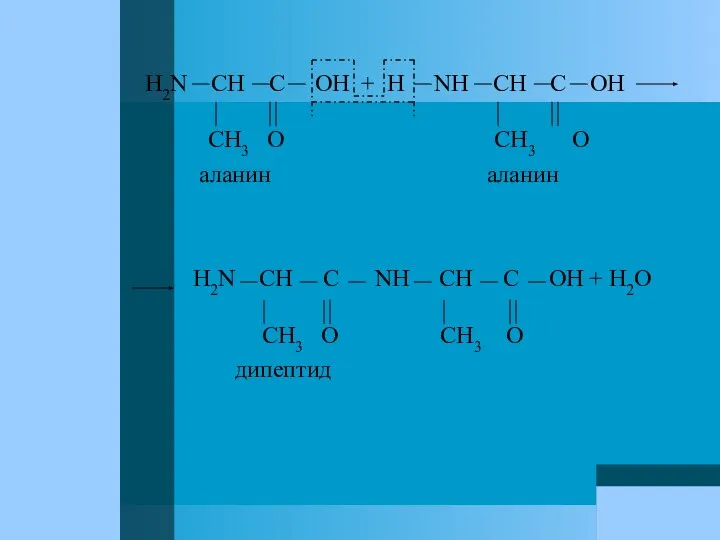
- 33. H2N CH C OH + H NH CH C OH CH3 O CH3 O аланин аланин
- 34. Таким же путем из многих аминокислотных молекул получают полипептиды. Образование полипептидов из α-аминокислот лежит в основе
- 35. Белковые вещества. Белковые вещества, или белки, представляют собой природные высокомолекулярные азотсодержащие органические соединения, очень сложные молекулы
- 36. В природе существует огромное множество различных белков. Они различаются по молекулярной массе, свойствам и той роли,
- 37. При нагревании с кислотами или со щелочами, а также при обычных температурах под действием специальных ферментов
- 38. Каждый организм из аминокислот, получаемых с белками пищи, синтезирует свои, необходимые ему белки. При этом из
- 39. Строение белков. Различные α-аминокислоты, образуя белки, соединяются за счет аминогрупп и карбоксильных групп при помощи группировки
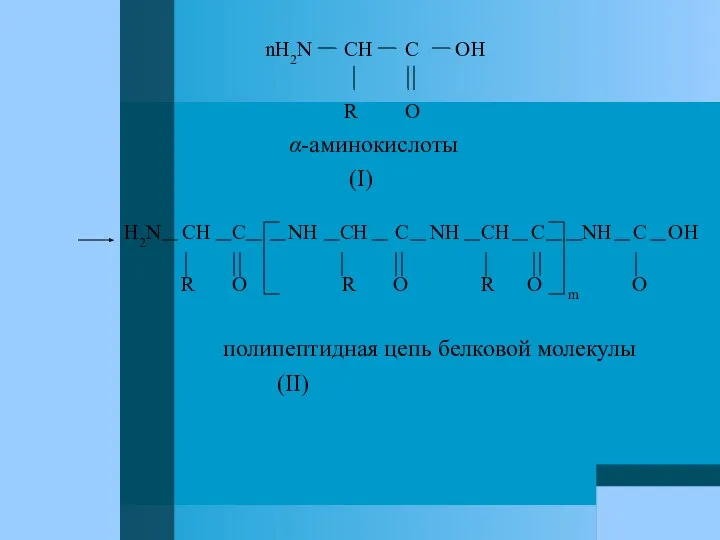
- 40. nH2N CH C OH R O α-аминокислоты (I) H2N CH C NH CH C NH CH
- 41. Таким образом, белки, являющиеся природными высокомолекулярными соединениями, представляют собой продукты поликонденсации α-аминокислот. Полипептидные цепи белков строятся
- 42. Природа белка определяется не только тем, какие аминокислоты входят в его состав, но особенно и тем,
- 43. Большое значение имеет образование между полипептидными цепями белков или между отдельными участками таких цепей водородных и
- 44. Характерная особенность полипептидных цепей многих белков – склонность закручиваться в спираль. Между отдельными витками спирали образуются
- 45. Спирали и нити вторичной структуры, а также неупорядоченные участки полипептидных цепей могут различным способом сгибаться и
- 46. Свойства белков. Белки – высокомолекулярные соединения. Некоторые из них обладают молекулярными массами порядка десятков (13000-68000), другие
- 47. Все белки нерастворимы в безводном спирте и других органических растворителях. Многие белки растворяются в воде и
- 48. Наличие различных функциональных групп в боковых ответвлениях полипептидных цепей придает белкам способность вступать во множество реакций;
- 49. Осаждение белков из растворов. При добавлении к водным растворам белков концентрированных растворов минеральных солей (например, сульфата
- 50. Другие реагенты – соли тяжелых металлов (сульфат меди, ацетат свинца), а также кислоты (азотная, уксусная, пикриновая,
- 51. Цветные реакции белков. Биуретовая реакция. При взаимодействии в щелочной среде с солями меди (CuSO4) все белки
- 52. Таким образом, биуретовая реакция белков подтверждает наличие в их молекулах пептидных связей. Эту реакцию дают и
- 53. Ксантопротеиновая реакция. Если белки или их растворы нагревают с концентрированной азотной кислотой, они окрашиваются в желтый
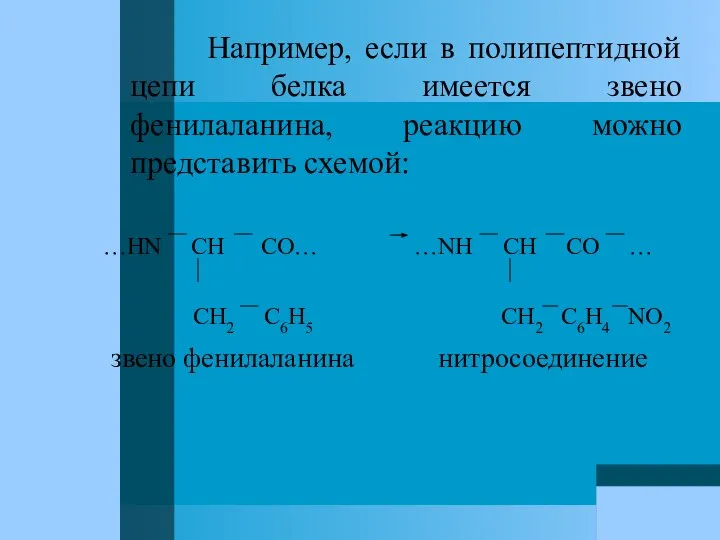
- 54. Например, если в полипептидной цепи белка имеется звено фенилаланина, реакцию можно представить схемой: …HN CH CO…
- 55. В отличие от биуретовой реакции ксантопротеиновую реакцию дают не все белки, поскольку в некоторых из них
- 56. Классификация белков. Среди белков различают две основные группы веществ: а) протеины, или простые белки, состоящие только
- 57. Среди протеинов выделяют несколько подгрупп, отличающихся преимущественно по растворимости. Протеиды подразделяют на подгруппы в зависимости от
- 58. Белковые вещества классифицируются также по форме их молекул: а) фибриллярные (волокнистые) белки, молекулы которых имеют нитевидную
- 59. Ароматические амины Производные ароматических углеводородов, содержащие в бензольном ядре взамен атома водорода остаток аммиака – аминогруппу,
- 60. Номенклатура и изомерия Для многих ароматических аминов употребительны тривиальные названия. Простейший ароматический амин – производное бензола
- 61. Простейшими гомологами анилина являются аминопроизводные толуола CH3 C6H4 NH2, называемые толуидинами; они существуют в виде орто-,
- 62. Толуидины по названию радикалов толуола можно назвать о-, м- и n-толиламинами. Ароматические амины, в которых, как
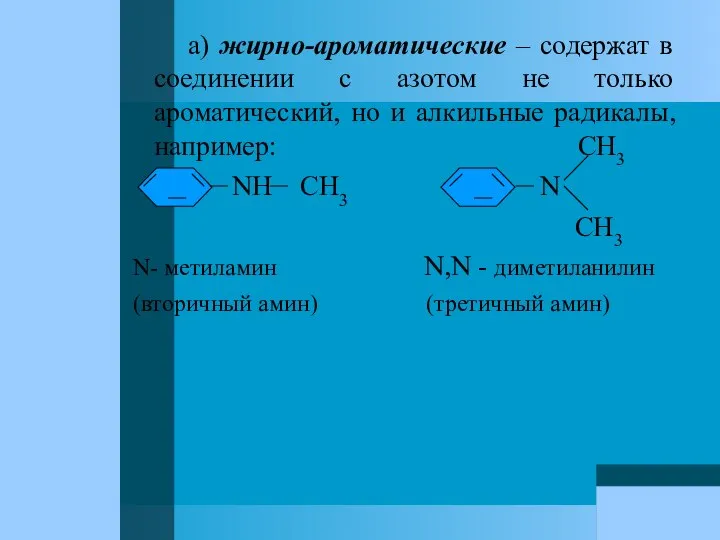
- 63. а) жирно-ароматические – содержат в соединении с азотом не только ароматический, но и алкильные радикалы, например:
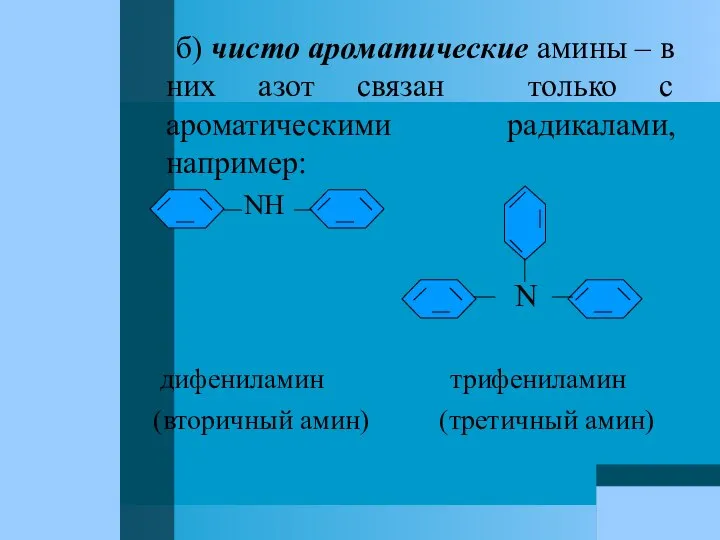
- 64. б) чисто ароматические амины – в них азот связан только с ароматическими радикалами, например: NH N
- 65. Химические свойства Реакции за счет аминогруппы Подобно аминам жирного ряда, ароматические амины проявляют свойства оснований и
- 66. Основные свойства у ароматических аминов гораздо менее выражены, чем у аминов жирного ряда, что объясняется влиянием
- 67. Реакции с азотистой кислотой Первичные ароматические амины в реакции с азотистой кислотой (HNO2) отличаются от первичных
- 68. Третичные ароматические амины, в отличии от третичных аминов жирного ряда, взаимодействуют с азотистой кислотой. Третичная аминогруппа
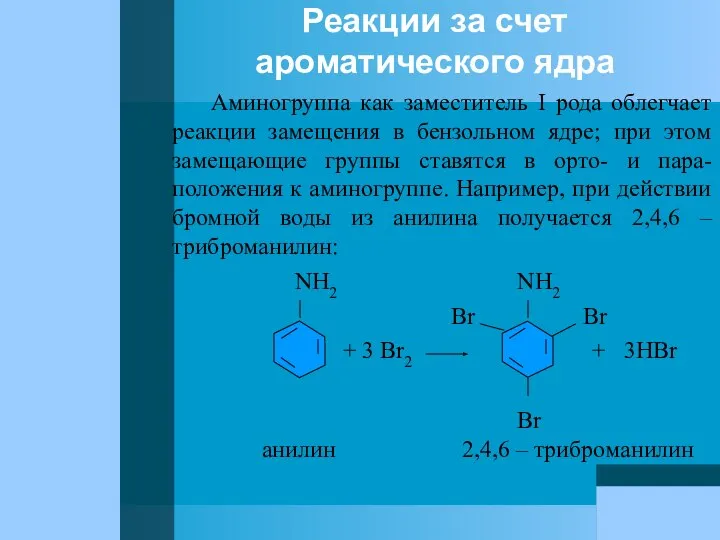
- 69. Реакции за счет ароматического ядра Аминогруппа как заместитель I рода облегчает реакции замещения в бензольном ядре;
- 70. Действие окислителей. Под влиянием аминогруппы бензольное ядро теряет устойчивость к действию окислителей, и ароматические амины легко
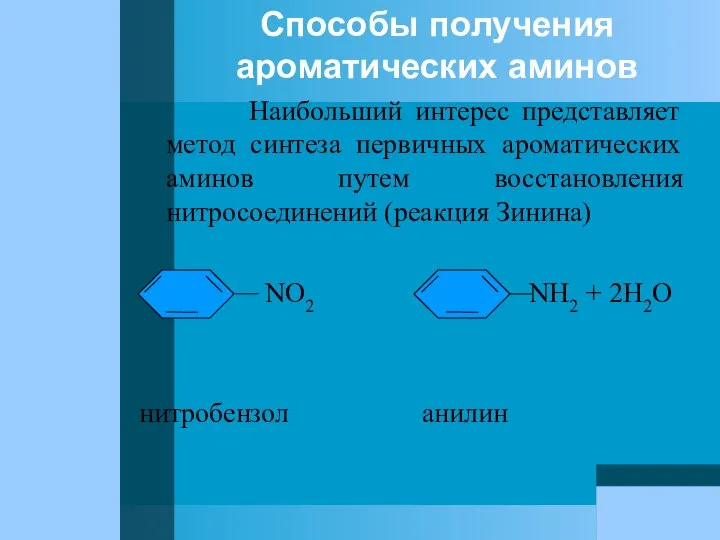
- 71. Способы получения ароматических аминов Наибольший интерес представляет метод синтеза первичных ароматических аминов путем восстановления нитросоединений (реакция
- 72. Ароматические диазосоединения и азосоединения (азокрасители) Среди производных первичных ароматических аминов одними из наиболее важных являются диазосоединения
- 73. В диазосоединениях азогруппа связана только с одним ароматическим углеводородным радикалом (Ar) и с какой-нибудь группой, присоединенной
- 74. Диазосоединения существуют в нескольких формах, легко превращающихся одна в другую. Вещества, отвечающие формуле Ar N =
- 75. Под действием щелочей соли диазония вновь переходят в диазогидроксиды: + Ar N N Cl¯ + NaOH
- 76. Простейшее ароматическое диазосоединение является производным бензола. Соответствующая соль диазония, существующая в солянокислой среде, называется хлоридом бензолдиазония
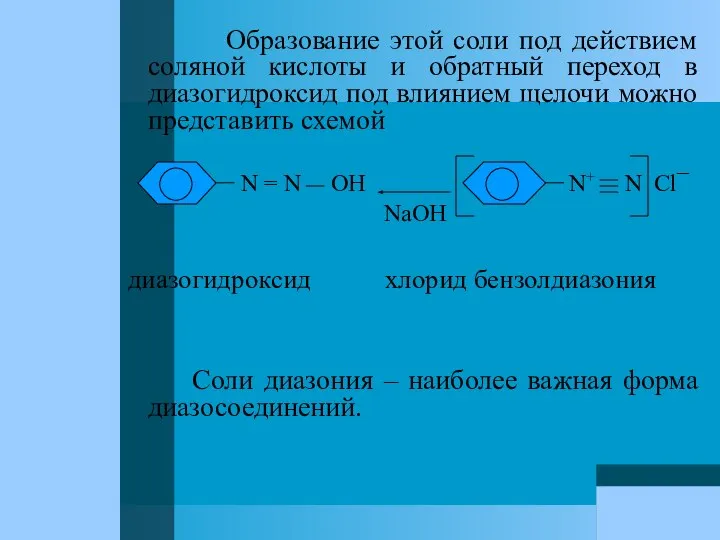
- 77. Образование этой соли под действием соляной кислоты и обратный переход в диазогидроксид под влиянием щелочи можно
- 78. Получение ароматических диазосоединений Диазосоединения получаются при диазотировании первичных ароматических аминов, т.е. при действии на них азотистой
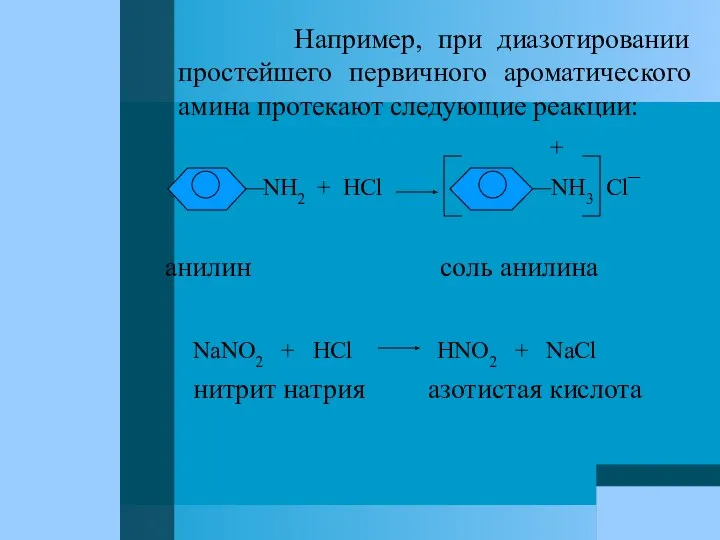
- 79. Например, при диазотировании простейшего первичного ароматического амина протекают следующие реакции: + NH2 + HCl NH3 Cl¯
- 80. + NH3 Cl¯ + HO N = O N ≡ N Cl¯+ +H2O соль анилина азотистая
- 81. Химические свойства диазосоединений Соли диазония – весьма реакционноспособные вещества. Используя их как промежуточные продукты, из первичных
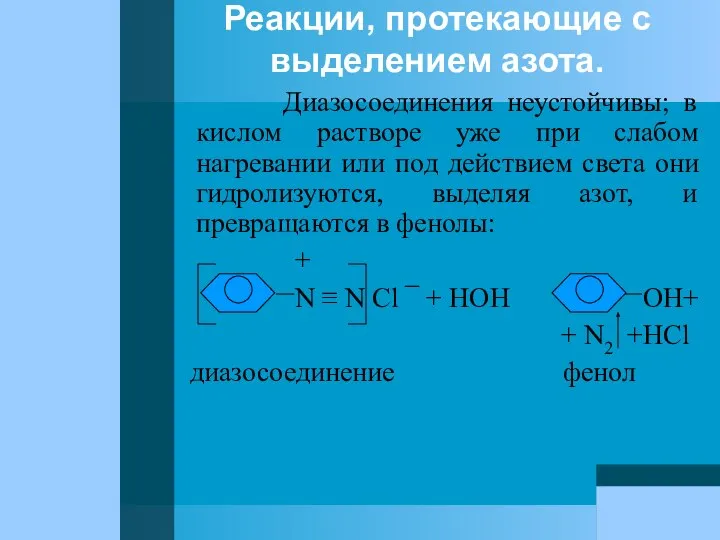
- 82. Реакции, протекающие с выделением азота. Диазосоединения неустойчивы; в кислом растворе уже при слабом нагревании или под
- 83. Если соль диазония – хлорид, бромид или иодид – нагревать с соответствующей солью меди (CuCl, CuBr,
- 84. Реакции, протекающие без выделения азота. Среди реакций этого типа наиболее важны реакции взаимодействия солей диазония с
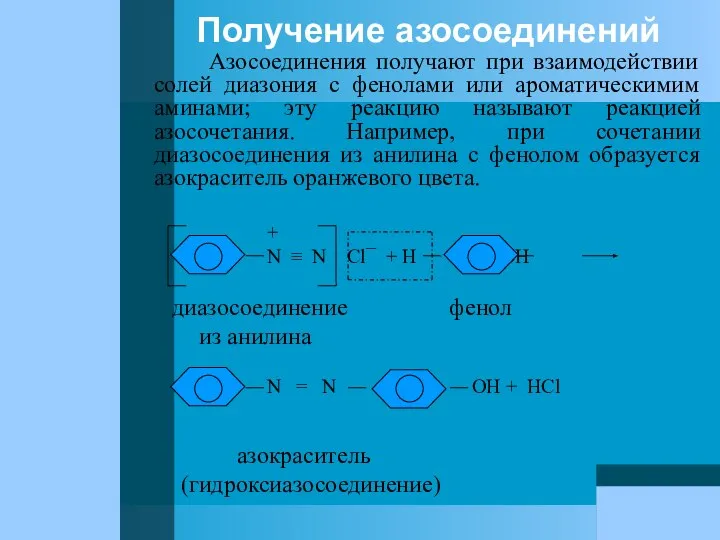
- 85. Получение азосоединений Азосоединения получают при взаимодействии солей диазония с фенолами или ароматическимим аминами; эту реакцию называют
- 86. Если то же диазосоединение взаимодействует с диметиланилином (ароматическим амином), то получается азокраситель желтого цвета. С фенолами
- 87. Полная схема синтеза азокрасителя (азосоединения), известного под названием паракрасный. В качестве диазосостаавляющей берется n -нитроанилин, а
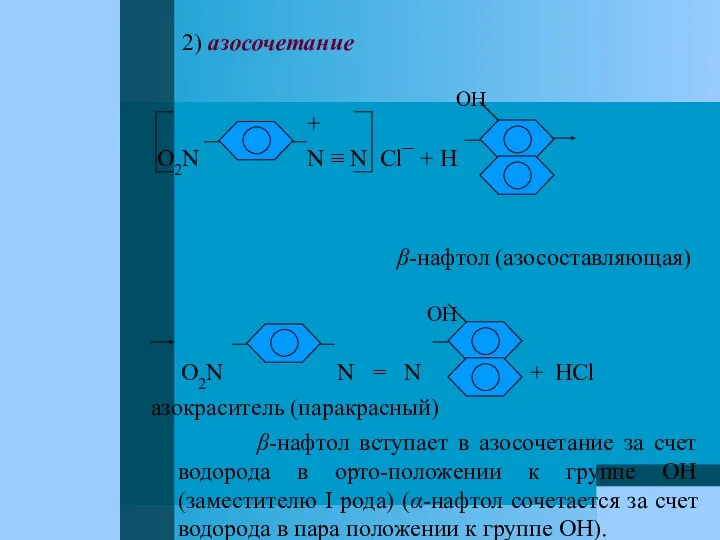
- 88. 2) азосочетание OH + O2N N ≡ N Cl¯ + H β-нафтол (азосоставляющая) OH O2N N
- 90. Скачать презентацию




![[NH4]+ OH- гидроксид аммония гидроксид четырехзамещенного аммония (четвертичное аммониевое основание)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395310/slide-5.jpg)



































































 Ферроцен. Свойства, получение и применение
Ферроцен. Свойства, получение и применение Гетероциклические соединения
Гетероциклические соединения Уравнение материального баланса для элементарного объема проточного химического реактора
Уравнение материального баланса для элементарного объема проточного химического реактора Технология производства и свойства искусственных волокон
Технология производства и свойства искусственных волокон Биохимия нервной ткани. Биологические мембраны
Биохимия нервной ткани. Биологические мембраны Элементы VIIА-группы (галогены). Группа самых электроотрицательных элементов
Элементы VIIА-группы (галогены). Группа самых электроотрицательных элементов Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола
Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола Органические вещества спирты
Органические вещества спирты Тема 3
Тема 3 Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості Каталитический риформинг
Каталитический риформинг Тепловой эффект химических реакций
Тепловой эффект химических реакций Э.М. Спиридонов. Эволюция минералов цинка в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов цинка в зоне гипергенеза Алкадиены
Алкадиены Жидкие кристаллы
Жидкие кристаллы Сероводоро́д, сернистый водород (H2S) (физические свойства)
Сероводоро́д, сернистый водород (H2S) (физические свойства) Химический состав микроорганизмов-деструкторов
Химический состав микроорганизмов-деструкторов Изделия на основе углеволокон
Изделия на основе углеволокон Рассмотрение продуктов цинкового производства при помощи аналитических методов анализа
Рассмотрение продуктов цинкового производства при помощи аналитических методов анализа ЛЕКЦИЯ 2. МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЙ и КЛЕТОЧНЫЙ УРОВНИ ОРГАНИЗАЦИИ ЖИЗНИ. ГЕНЕТИЧЕСКИЙ МАТЕРИАЛ и его ХАРАКТЕРИСТИКИ. РЕПЛИКАЦИ
ЛЕКЦИЯ 2. МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЙ и КЛЕТОЧНЫЙ УРОВНИ ОРГАНИЗАЦИИ ЖИЗНИ. ГЕНЕТИЧЕСКИЙ МАТЕРИАЛ и его ХАРАКТЕРИСТИКИ. РЕПЛИКАЦИ Спирти. Феноли. Етери
Спирти. Феноли. Етери Зинин Николай Николаевич
Зинин Николай Николаевич Инструментальные методы анализа
Инструментальные методы анализа Презентация по Химии "Классификация и номенклатура неорганических соединений" - скачать смотреть
Презентация по Химии "Классификация и номенклатура неорганических соединений" - скачать смотреть  Знание химии в строительном деле на бытовом уровне
Знание химии в строительном деле на бытовом уровне Синтез олигомеров этиленгликоля и терефталевой кислоты
Синтез олигомеров этиленгликоля и терефталевой кислоты Нефть в США. История. Запасы и прогноз
Нефть в США. История. Запасы и прогноз Презентация по Химии "Азотная кислота и ее соли" - скачать смотреть
Презентация по Химии "Азотная кислота и ее соли" - скачать смотреть