Содержание
- 2. Кристаллические вещества состоят из огромного количества очень маленьких кристалликов, имеющих абсолютно одинаковое строение. Кристаллические вещества характеризуются
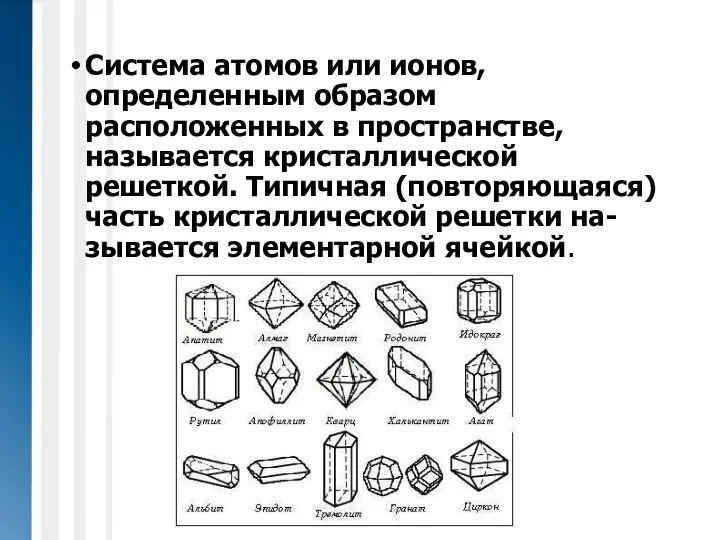
- 3. Система атомов или ионов, определенным образом расположенных в пространстве, называется кристаллической решеткой. Типичная (повторяющаяся) часть кристаллической
- 4. Огромное разнообразие кристаллических решеток подразделено на 7 больших систем, называемых СИНГОНИЯМИ (по геометрической форме кристаллов)
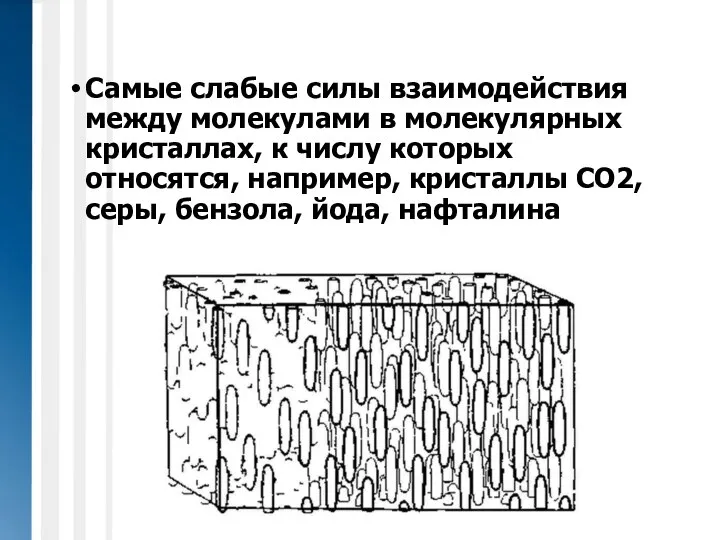
- 5. Самые слабые силы взаимодействия между молекулами в молекулярных кристаллах, к числу которых относятся, например, кристаллы СО2,
- 6. Ионная Составляющая кристаллической решетки – ионы с противоположными зарядами, взаимодействуют через электростатические силы притяжения и электростатические
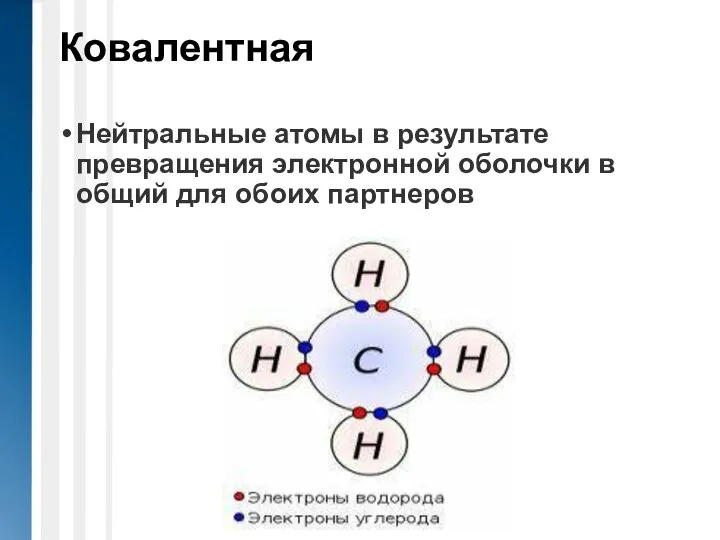
- 7. Ковалентная Нейтральные атомы в результате превращения электронной оболочки в общий для обоих партнеров
- 8. Металлическая Металлическая структура может быть представлена как ионная решетка, распределение в газе из квази-свободных электронов. Связь
- 10. Скачать презентацию




 Растворы
Растворы Теплота горения
Теплота горения Физико-химиеские методы анализа (ФХМА)
Физико-химиеские методы анализа (ФХМА) Хімія в житті суспульства
Хімія в житті суспульства Решение задач в химии (ОГЭ, ЕГЭ, олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, олимпиады) Природный газ, состав применение в качестве топлива
Природный газ, состав применение в качестве топлива Алканы
Алканы Пути обмена глюкозо-6 фосфата в тканях. Анаэробное расщепление глюкозы. Спиртовое брожение. Метаболизм этанола. (Тема 2)
Пути обмена глюкозо-6 фосфата в тканях. Анаэробное расщепление глюкозы. Спиртовое брожение. Метаболизм этанола. (Тема 2) Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі
Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі Алкины
Алкины Презентация по Химии "Коррозия металлов и способы ее устранения" - скачать смотреть
Презентация по Химии "Коррозия металлов и способы ее устранения" - скачать смотреть  Чистячі засоби для ванної кімнати та кафелю
Чистячі засоби для ванної кімнати та кафелю Оксиды
Оксиды Тест «Природный газ»
Тест «Природный газ» Гетерогенные реакции в растворах электролитов
Гетерогенные реакции в растворах электролитов Нуклеиновые кислоты Френсис Крик и Джеймс Уитсон рядом со своей моделью ДНК (© A. Barrington Brown/Science Source/Photo Researchers, Inc.)
Нуклеиновые кислоты Френсис Крик и Джеймс Уитсон рядом со своей моделью ДНК (© A. Barrington Brown/Science Source/Photo Researchers, Inc.)  Синтез и исследование метилольных и хлорметильных производных аллантоина
Синтез и исследование метилольных и хлорметильных производных аллантоина Теория нитрования
Теория нитрования Химические свойства металлов
Химические свойства металлов Биохимия. Химический состав организма
Биохимия. Химический состав организма Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации
Основные понятия химической термодинамики. Первый закон термодинамики Физическая и коллоидная химия и ее значение для фармации Нафта-чорне золото
Нафта-чорне золото  Дисперсные системы. Коллоидные растворы
Дисперсные системы. Коллоидные растворы Задача №5. Свинцовый водопровод. Команда «Карбораны»
Задача №5. Свинцовый водопровод. Команда «Карбораны» Фенольно-изоцианатная композиция
Фенольно-изоцианатная композиция Химия в быту
Химия в быту Химия и организм человека
Химия и организм человека Use of chlorine
Use of chlorine