Содержание
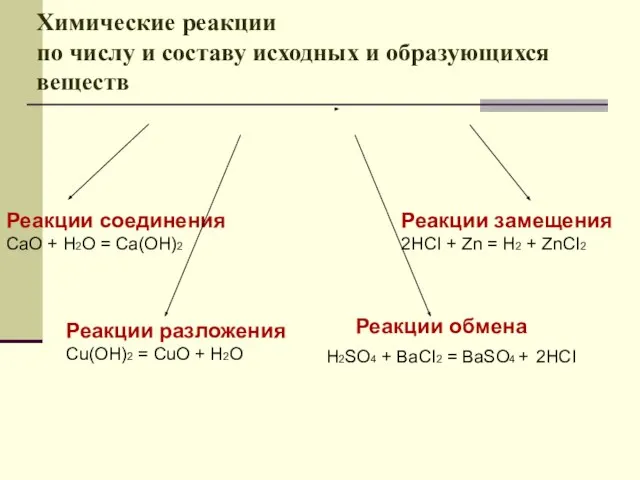
- 2. Химические реакции по числу и составу исходных и образующихся веществ Реакции соединения CaO + H2O =
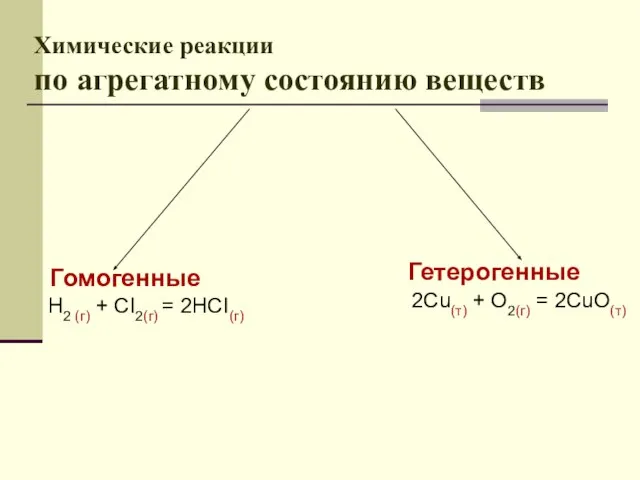
- 3. Химические реакции по агрегатному состоянию веществ Гомогенные H2 (г) + CI2(г) = 2HCI(г) Гетерогенные 2Cu(т) +
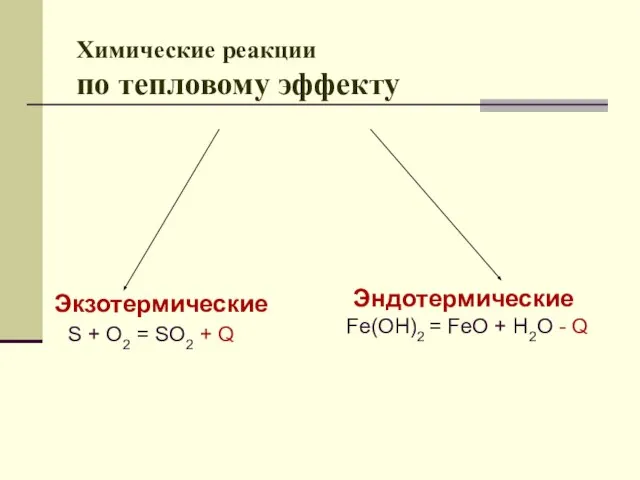
- 4. Химические реакции по тепловому эффекту Экзотермические S + O2 = SO2 + Q Эндотермические Fe(OH)2 =
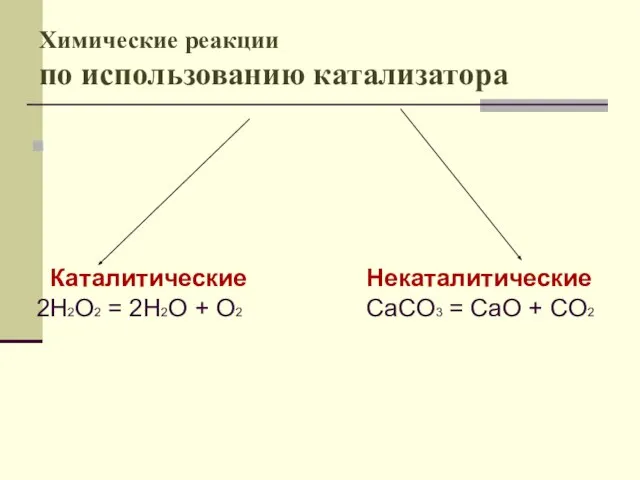
- 5. Химические реакции по использованию катализатора Каталитические 2H2O2 = 2H2O + O2 Некаталитические CaCO3 = CaO +
- 6. Химические реакции по направлению Обратимые 2SO2 + O2 2SO3 Необратимые 4P + 5O2 = 2P2O5
- 7. Химические реакции по изменению степени окисления Не окислительно -восстановительные +2 +4 -2 +2 -2 +4 -2
- 9. Скачать презентацию
 Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Электродные процессы
Электродные процессы Решение экспериментальных задач по теме металлы
Решение экспериментальных задач по теме металлы Презентация ГАЛОГЕНЫ И ИХ СОЕДИНЕНИЯ
Презентация ГАЛОГЕНЫ И ИХ СОЕДИНЕНИЯ  Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Коррозия металлов и способы защиты от неё. (11 класс)
Коррозия металлов и способы защиты от неё. (11 класс) Выполнил: А. М. Галенко, учитель химии МОУ СОШ № 67 г. Волгограда
Выполнил: А. М. Галенко, учитель химии МОУ СОШ № 67 г. Волгограда  Обмен и функции нуклеотидов
Обмен и функции нуклеотидов Катализаторы на носителях, получаемые методом пропитки
Катализаторы на носителях, получаемые методом пропитки Строение атома. (Лекция 2-3)
Строение атома. (Лекция 2-3) Сероводоро́д, сернистый водород (H2S) (физические свойства)
Сероводоро́д, сернистый водород (H2S) (физические свойства) Базиты. Химический состав
Базиты. Химический состав Застосування нафти та нафтопродуктів Презентацію підготували учениці 11-В класу Кузнецовської гімназії Турик Даша та Коновал
Застосування нафти та нафтопродуктів Презентацію підготували учениці 11-В класу Кузнецовської гімназії Турик Даша та Коновал  Обобщение и систематизация знаний по теме Химическая связь и строение атома
Обобщение и систематизация знаний по теме Химическая связь и строение атома Реакции ионного обмена
Реакции ионного обмена Кальцій
Кальцій Последствия применения удобрений в сельском хозяйстве
Последствия применения удобрений в сельском хозяйстве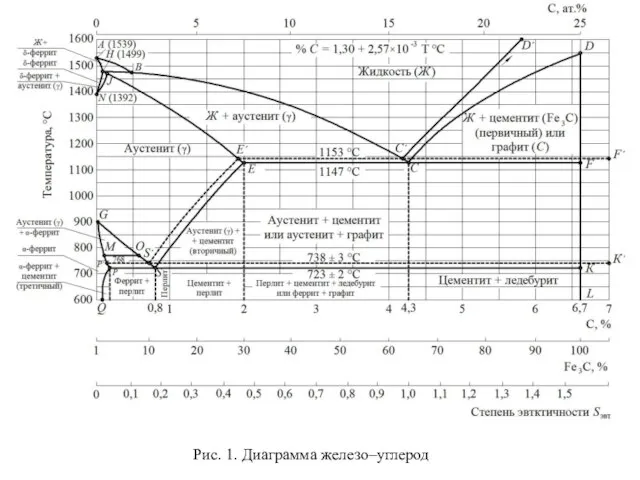 Чугуны и стали
Чугуны и стали Применение 3D-принтеров для решения химических задач
Применение 3D-принтеров для решения химических задач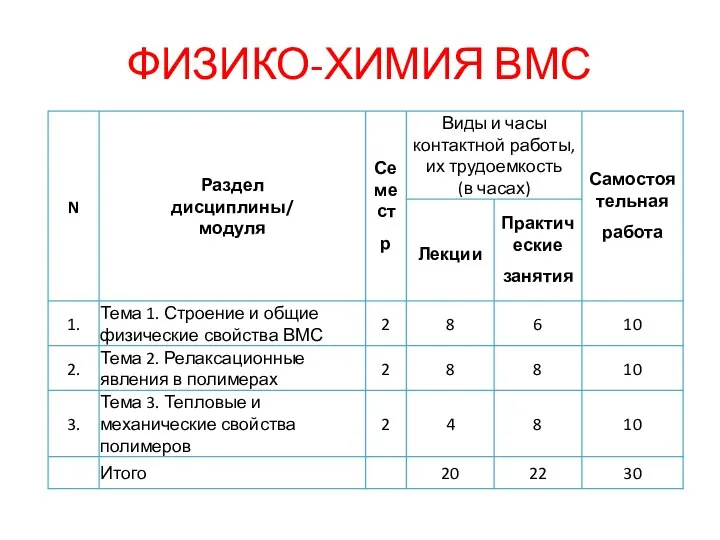 Строение и общие физические свойства ВМС. Релаксационные явления в полимерах. Тепловые и механические свойства полимеров
Строение и общие физические свойства ВМС. Релаксационные явления в полимерах. Тепловые и механические свойства полимеров Химическая связь
Химическая связь Композиционные материалы для изоляции электрических машин
Композиционные материалы для изоляции электрических машин Кислоты. Состав кислот, их классификация и физические свойства
Кислоты. Состав кислот, их классификация и физические свойства Обмен белков и аминокислот. Азотистый баланс. (Лекция 14)
Обмен белков и аминокислот. Азотистый баланс. (Лекция 14) Классификация неорганических веществ
Классификация неорганических веществ Области применения спиртов
Области применения спиртов Гидролиз солей
Гидролиз солей Гормоны. Механизм действия гормонов
Гормоны. Механизм действия гормонов