Содержание
- 2. УМК «ХИМИЯ» Тема лекции: Химическая связь Лектор – Иванов М.Г. Разработчик – Данилова Д.А.
- 3. Цель лекции: изложение проблемы химической связи и строения молекул в рамках современной химической теории Компетенции, формируемые
- 4. СОДЕРЖАНИЕ Виды химической связи Ковалентная связь квантово-механическое описание строения молекул метод валентных схем механизмы образования ковалентной
- 5. Химическая связь Химическая связь – это различные виды взаимодействия, обуславливающие устойчивое существование многоатомных соединений (молекул, ионов,
- 6. Ковалентная связь Квантово-механическое описание строения молекул В основе лежит решение волнового уравнения Шредингера для соответствующей системы.
- 7. Ковалентная связь Квантово-механическое описание строения молекул Образование химической связи между атомами в молекуле Н2 обусловлено тем,
- 8. Ковалентная связь Метод валентных связей (ВС) В основе метода ВС лежат следующие допущения Ковалентная химическая связь
- 9. Ковалентная связь Механизмы образования ковалентной связи 1. Обменный механизм Атомы предоставляют на образование химической связи одноэлектронные
- 10. Ковалентная связь Свойства связи Энергия связи Длина связи Направленность химической связи Кратность связи Насыщаемость связи Полярность
- 11. Ковалентная связь 1. Энергия связи Энергия связи – энергия, которая выделяется при образовании химической связи из
- 12. Ковалентная связь 3. Направленность химической связи Поскольку электронные орбитали направлены в про-странстве определенным образом, то и
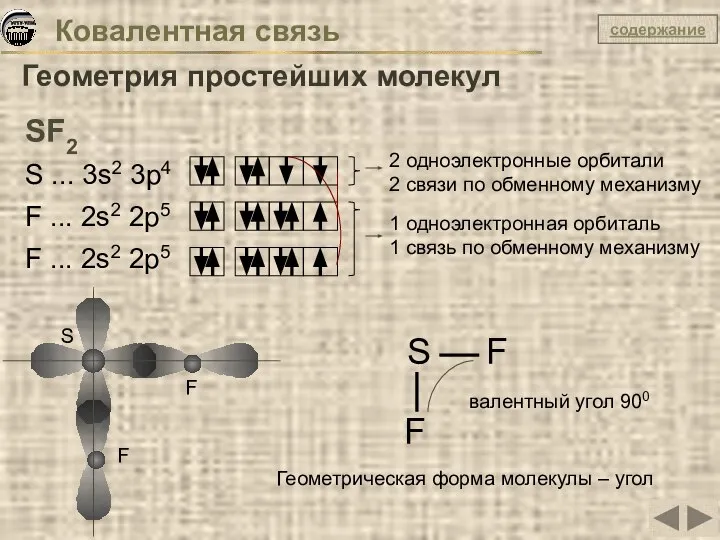
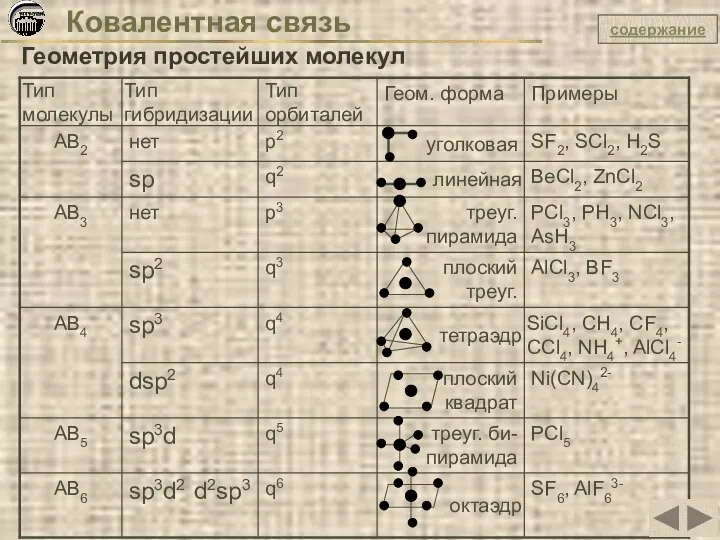
- 13. Ковалентная связь Геометрия простейших молекул SF2 S ... 3s2 3p4 F ... 2s2 2p5 F ...
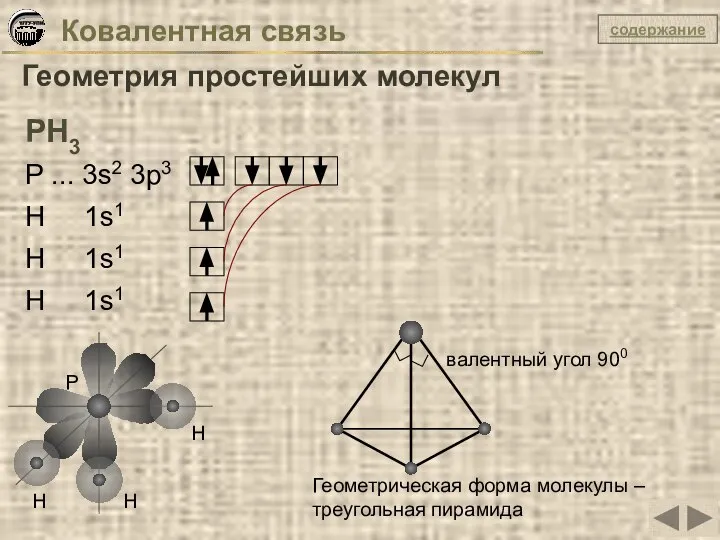
- 14. Ковалентная связь Геометрия простейших молекул РН3 Р ... 3s2 3p3 Н 1s1 Н 1s1 Н 1s1
- 15. Гибридизация – это представление о выравнивании валентных атомных орбиталей по форме и по энергии Ковалентная связь
- 16. Ковалентная связь Гибридизация BeCl2 Be ...2s2 Be* ...2s1 2p1 Be* - может образовать две связи по
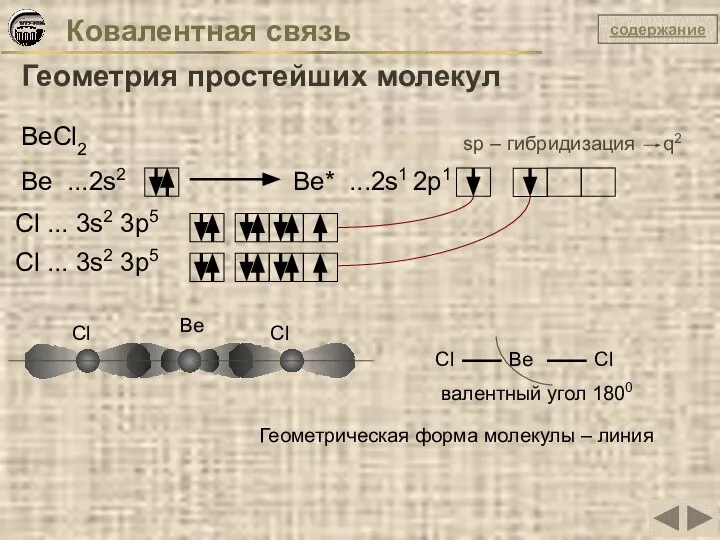
- 17. Ковалентная связь Геометрия простейших молекул BeCl2 Be ...2s2 Be* ...2s1 2p1 Сl ... 3s2 3p5 Cl
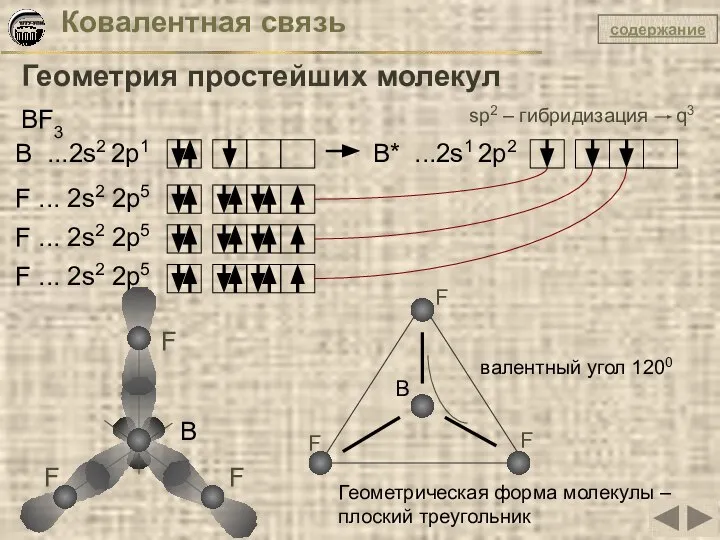
- 18. Ковалентная связь Геометрия простейших молекул BF3 B ...2s2 2p1 B* ...2s1 2p2 F ... 2s2 2p5
- 19. Ковалентная связь Геометрия простейших молекул SiCl4 Si ...3s2 3p2 Si* ...3s1 3p3 Cl ... 3s2 3p5
- 20. Ковалентная связь Геометрия простейших молекул содержание
- 21. Ковалентная связь 4. Кратность связи В зависимости от способа перекрывания электронных облаков различают σ-, π-, δ-связи
- 22. Ковалентная связь π – связь р - р d - р d - d Условное обозначение
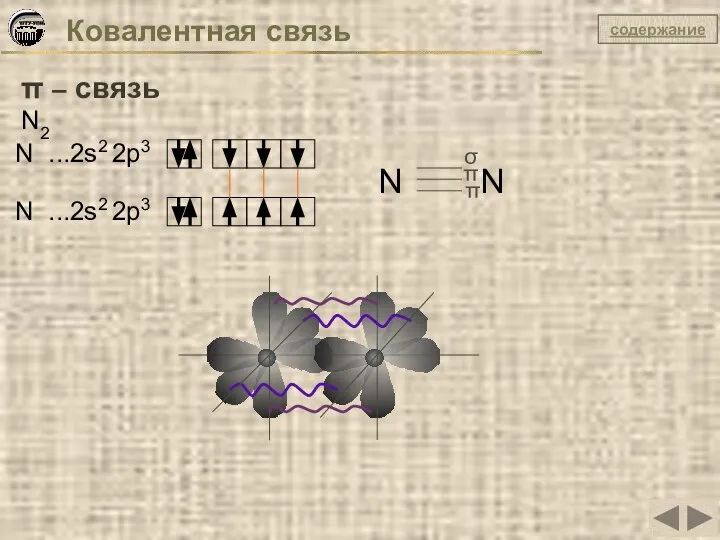
- 23. Ковалентная связь π – связь N2 N ...2s2 2p3 N ...2s2 2p3 N N π σ
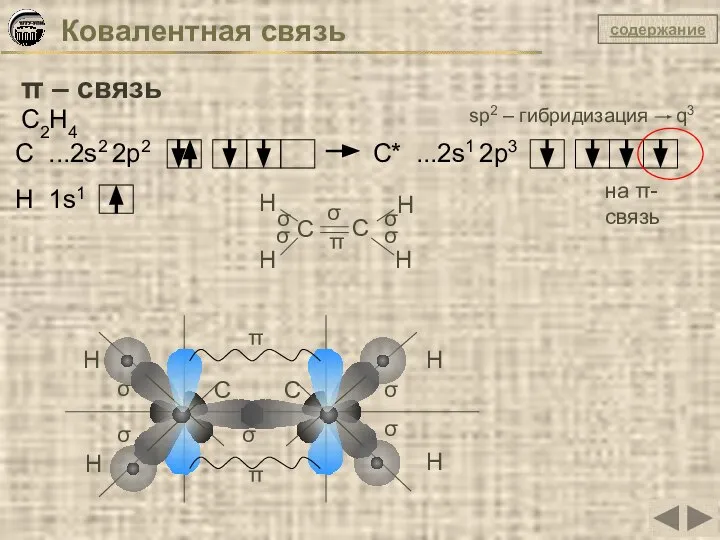
- 24. Ковалентная связь π – связь C2H4 C ...2s2 2p2 C* ...2s1 2p3 sp2 – гибридизация q3
- 25. Ковалентная связь 5. Насыщаемость связи. Валентность. Насыщаемость – способность атома взаимодействовать только с определенным числом атомов
- 26. Ковалентная связь Валентные возможности элементов I период H 1s1 1 ковалентная связь обменный механизм В =
- 27. Ковалентная связь Валентные возможности элементов II период Be ...2s2 Be* ...2s1 2p1 2 ковалентные связи по
- 28. Ковалентная связь Валентные возможности элементов II период C ...2s2 2p2 C* ...2s1 2p3 Вmax=4 C C
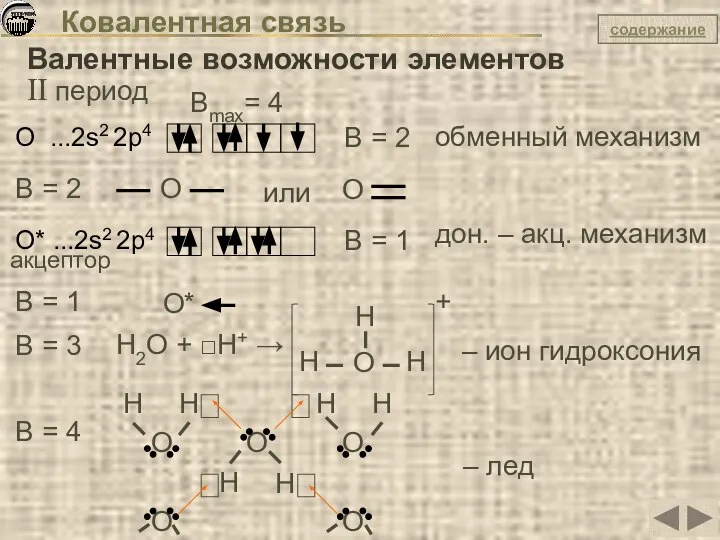
- 29. Ковалентная связь Валентные возможности элементов II период О ...2s2 2p4 B = 2 обменный механизм Вmax=
- 30. Ковалентная связь Валентные возможности элементов III период s p d – 9 валентных орбиталей Практически В
- 31. Ковалентная связь Валентные возможности элементов Координационное число – число атомов соседей данного элемента max к.ч. =
- 32. Ковалентная связь Правила составления валентных схем Оценить валентные возможности всех атомов в данном соединении в невозбужденном
- 33. Ковалентная связь Правила составления валентных схем 4. В молекулах кислот водород всегда присоединяется к кислотообразующему элементу
- 34. Ковалентная связь Правила составления валентных схем Cl2O7 Cl ... 3s2 3p5 О ...2s2 2p4 О* ...2s2
- 35. Ковалентная связь 6. Полярность связи. Полярность молекул. Степень окисления элементов. Неполярная ковалентная связь – связь, образованная
- 36. Ковалентная связь Полярность молекул. Если молекула обладает собственным постоянным дипольным моментом, то такая молекула полярна. Для
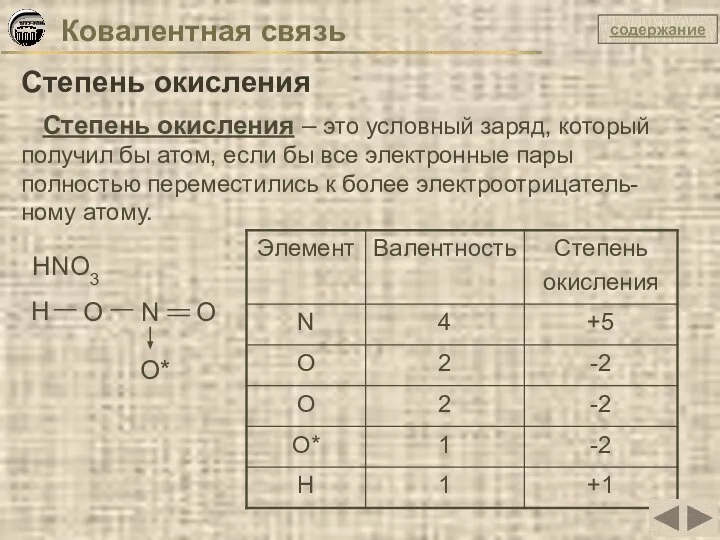
- 37. Ковалентная связь Степень окисления Степень окисления – это условный заряд, который получил бы атом, если бы
- 38. Ионная связь Осуществляется путем электростатического взаимо-действия между ионами. Ионная связь предельный случай ковалентной полярной связи, когда
- 39. Металлическая связь Связь между положительно заряженными остовами атомов осуществляется коллек-тивом валентных электронов, относи-тельно свободно перемещающихся по
- 40. Водородная связь Связь через атом водорода сильно электроотрицатель-ных атомов, имеющих очень малые радиусы (F, O, N).
- 41. Силы межмолекулярного взаимодействия Природа этих сил определяется электростатическим взаимодействием диполей 1. Ориентационное взаимодействие взаимодействие между полярными
- 42. Учение о химической связи – основополагающая проблема современной химии. Знание о природе взаимодействия атомов в веществе,
- 43. Глинка Н.Л. Общая химия: учеб. пособие для вузов / Н. Л. Глинка ; под ред. А.
- 45. Скачать презентацию

































 Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Химия в сельском хозяйстве.
Химия в сельском хозяйстве.  Аминспирттер және олардың биологиялық ролі.Элементорганикалық қосылыстар және олардың қасиеті
Аминспирттер және олардың биологиялық ролі.Элементорганикалық қосылыстар және олардың қасиеті Полимеризация бутилена и пропилена
Полимеризация бутилена и пропилена Чистые вещества и смеси (продолжение)
Чистые вещества и смеси (продолжение) Методы анализа вещества
Методы анализа вещества Типы химических реакций в неорганической и органической химии
Типы химических реакций в неорганической и органической химии Синтез и структура медьсодержащих и серебросодержащих соединений пектина и хитозана
Синтез и структура медьсодержащих и серебросодержащих соединений пектина и хитозана Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна
Проект – дослідження мило Dove Роботу виконала учениця 11 класу Бабенко Аліна Віталіївна  Пена и пенообразователи. Назначение, виды, состав и свойства
Пена и пенообразователи. Назначение, виды, состав и свойства Многоликая уксусная кислота
Многоликая уксусная кислота Распознавание химических соединений
Распознавание химических соединений Формирование ответственного отношения школьников к окружающей среде родного края на уроках химии и во внеурочное время.
Формирование ответственного отношения школьников к окружающей среде родного края на уроках химии и во внеурочное время.  Бионеорганическая химия. Комплексообразование в организме. (Лекция 3)
Бионеорганическая химия. Комплексообразование в организме. (Лекция 3) Глюкоза, ее строение и свойства
Глюкоза, ее строение и свойства Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М
Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М Лаки. Эмали. Красочные составы
Лаки. Эмали. Красочные составы Презентация по Химии "ЛИПИДНЫЙ ОБМЕН" - скачать смотреть бесплатно
Презентация по Химии "ЛИПИДНЫЙ ОБМЕН" - скачать смотреть бесплатно Строение атома
Строение атома Коррозия железа
Коррозия железа Презентація на тему: “Нітратна кислота” Підготував: Учень 10-А класу Луцької ЗОШ № 25 Матвійчук Роман
Презентація на тему: “Нітратна кислота” Підготував: Учень 10-А класу Луцької ЗОШ № 25 Матвійчук Роман  Искусственные или технические битумы
Искусственные или технические битумы Роль минеральных веществ в организме человека
Роль минеральных веществ в организме человека Оксид фосфора P2O5
Оксид фосфора P2O5 Методы выращивания кристаллов
Методы выращивания кристаллов Оборудование для дистилляции мисцеллы
Оборудование для дистилляции мисцеллы Химические свойства алкадиенов и алкинов
Химические свойства алкадиенов и алкинов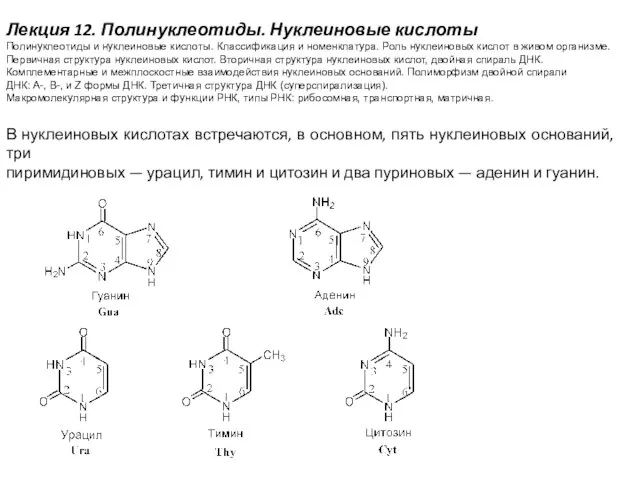 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты