Содержание
- 2. * Содержание: 1. Химический элемент. 2. Тренировочный материал для изучения знаков химических элементов. 3. Чтение химических
- 3. * Содержание: 12. Степень окисления. 13. Классификация неорганических веществ. 14. Кристаллические решетки. 15. Чистые вещества и
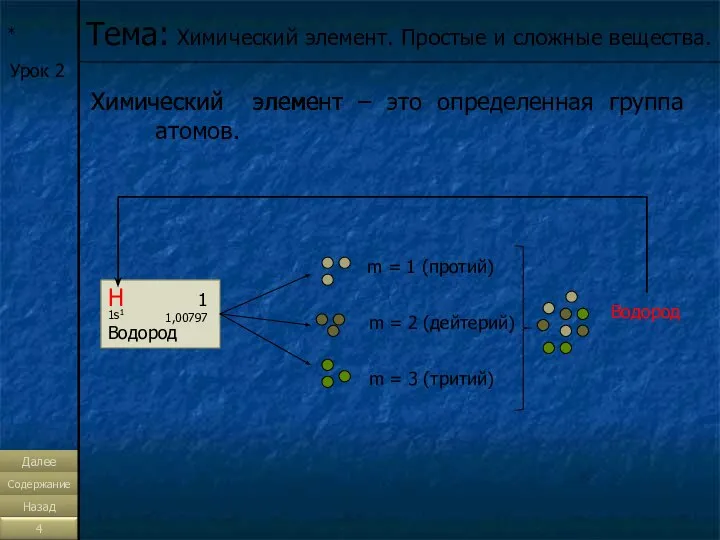
- 4. * Химический элемент – это определенная группа атомов. m = 1 (протий) m = 2 (дейтерий)
- 5. * Урок 5-6 Тема: Строение периодической системы. Знаки химических элементов. Тренировочный материал к изучению знаков химических
- 6. * Тема: Химические формулы. Урок 7 Чтение химических формул. Примеры: NH3 – молекула эн аш три
- 7. * Урок 11 Составление химических формул по валентности. Правило нахождения валентности: - У металла валентность ставится
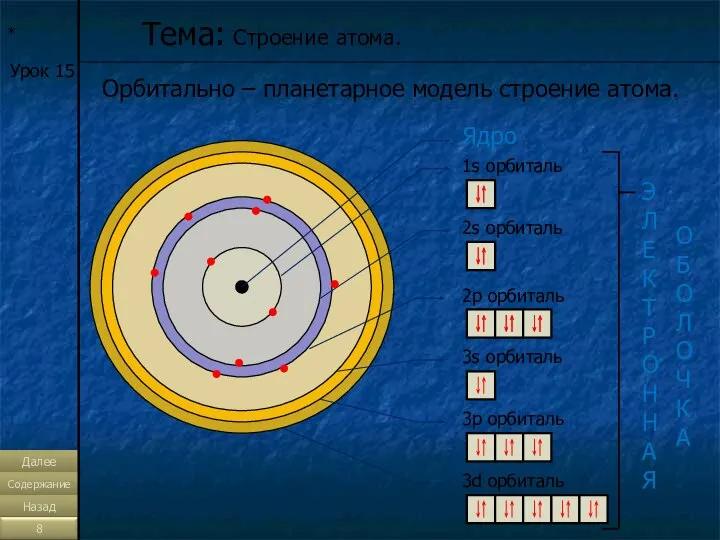
- 8. * Урок 15 Орбитально – планетарное модель строение атома. Тема: Строение атома. Ядро 1s орбиталь 2s
- 9. * Урок 17 Тема: Строение электронных оболочек атомов. Электронная оболочка – это совокупность электронов, двигающихся вокруг
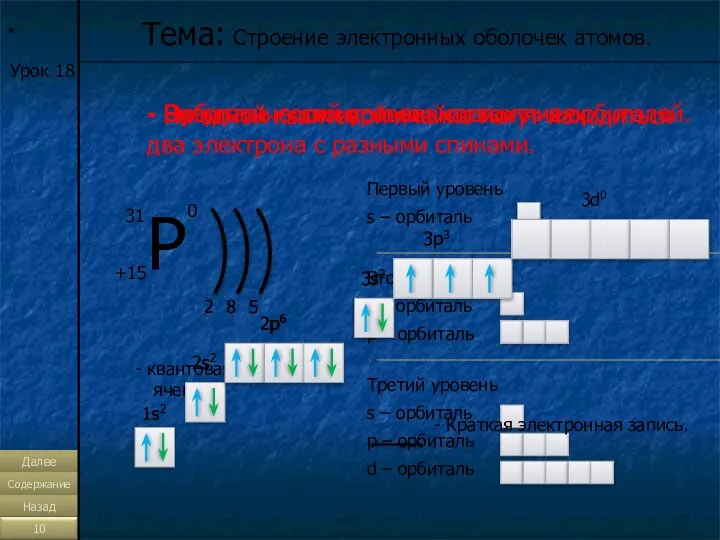
- 10. * Урок 18 Тема: Строение электронных оболочек атомов. - Энергетический уровень состоит из орбиталей. 2 8
- 11. * Урок 20 Тема: Ионы и ионная химическая связь. Химическая связь, образующуюся между ионами, называется ионной.
- 12. * Урок 21 Тема: Ковалентная связь между одинаковыми атомами неметаллов. Химическая связь, возникающая в результате образования
- 13. * Тема: Ковалентная полярная химическая связь. Химическая связь, возникающая в результате образования общих электронных пар, называется
- 14. * Тема: Молярный объем газов. Урок 31 Молярный объем (Vm) (л/моль). Vm – буквенное обозначение молярного
- 15. * Тема: Степень окисления. Урок 34 Степень окисления – это заряд приобретаемый элементом в соединении, в
- 16. * Классификация веществ. Вещества Простые Сложные Оксиды Основания Соли Кислоты Металлы Неметаллы Оксиды Оксиды – это
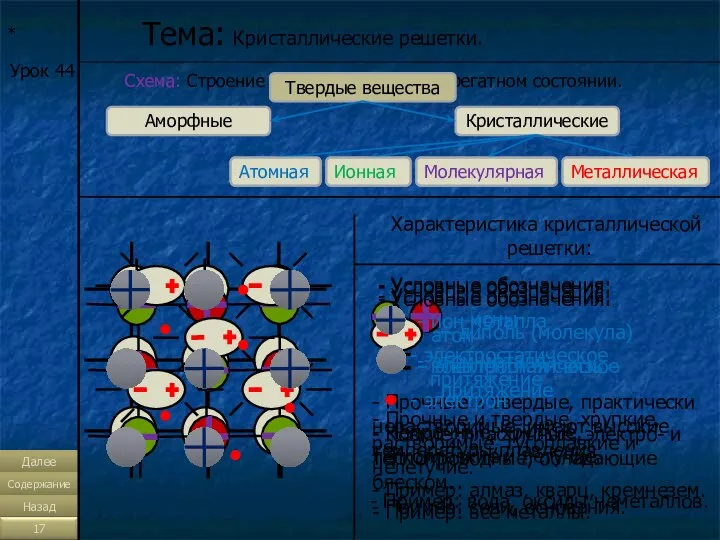
- 17. * Тема: Кристаллические решетки. Урок 44 Схема: Строение веществ в твердом агрегатном состоянии. Твердые вещества Аморфные
- 18. * Тема: Чистые вещества и смеси. Урок 45 Виды смесей. Схема: Вещества Чистые Смеси Однородные Неоднородные
- 19. * Уравнение химической реакции – это условная запись химического процесса, посредством химических знаков и символов. Пример:
- 20. * СОСТАВЛЕНИЕ УРАВНЕНИЙ ХИМИЧЕСКИХ РЕАКЦИЙ Пример: Составить уравнение реакции взаимодействия фосфора и кислорода. 1. В левой
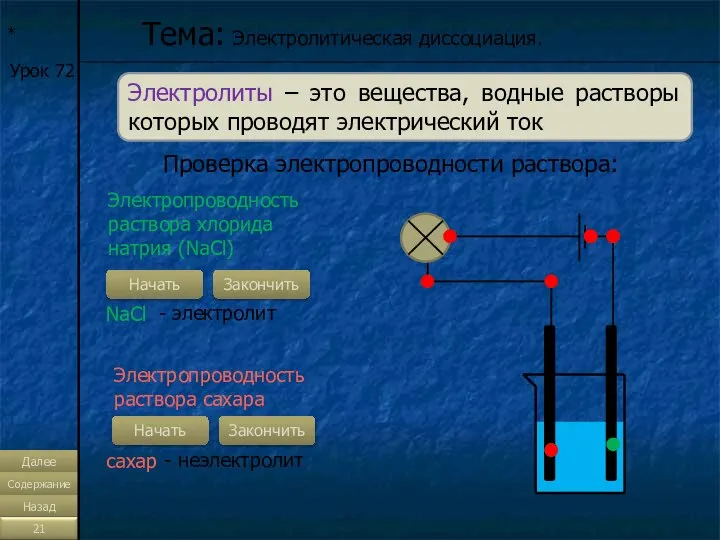
- 21. * Тема: Электролитическая диссоциация. Урок 72 Электролиты – это вещества, водные растворы которых проводят электрический ток
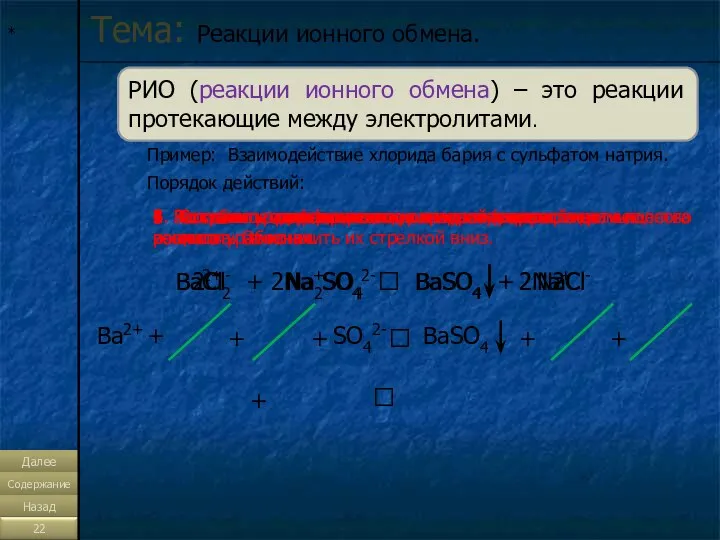
- 22. * Тема: Реакции ионного обмена. Пример: Взаимодействие хлорида бария с сульфатом натрия. BaCl2 + Na2SO4 ?
- 23. * Тема: Условия протекания реакций ионного обмена. I. Если образуется осадок. BaCl2 + Na2SO4 ? BaSO4
- 25. Скачать презентацию
















 Коллоидное состояние вещества
Коллоидное состояние вещества Презентация по Химии "Спирты" - скачать смотреть _
Презентация по Химии "Спирты" - скачать смотреть _ Вторая фаза метаболизма ксенобиотиков и эндогенных соединений
Вторая фаза метаболизма ксенобиотиков и эндогенных соединений Диаграмма состояния железо–углерод
Диаграмма состояния железо–углерод Непредельные углеводороды
Непредельные углеводороды Алкены.10 класс
Алкены.10 класс Сплавы. Свойства сплавов
Сплавы. Свойства сплавов Химическая технология органических веществ
Химическая технология органических веществ Алкины
Алкины Начало нанотехнологической эры. Фуллерены
Начало нанотехнологической эры. Фуллерены Фазовое равновесие в насыщенном растворе малорастворимого электролита
Фазовое равновесие в насыщенном растворе малорастворимого электролита Инсулин гормон жизни
Инсулин гормон жизни  Роль химии в сохранении окружающей среды
Роль химии в сохранении окружающей среды Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии
Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии Презентация по Химии "Органическая химия" - скачать смотреть
Презентация по Химии "Органическая химия" - скачать смотреть  Коллоидная химия
Коллоидная химия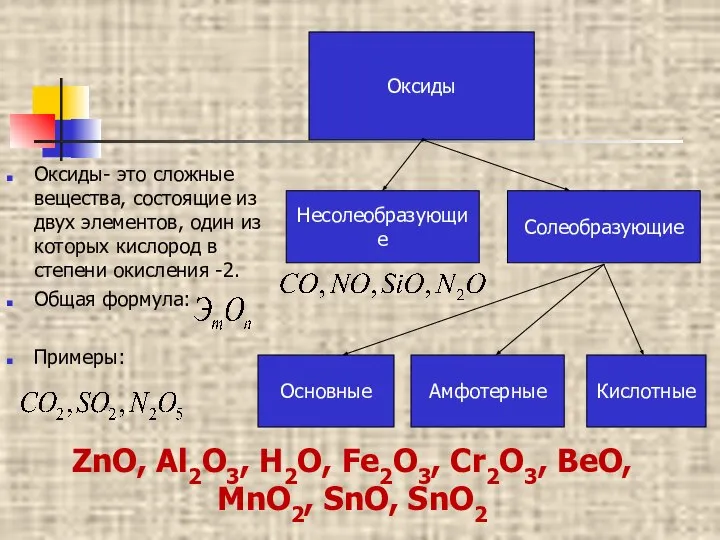 Оксиды. Классификация неорганических веществ
Оксиды. Классификация неорганических веществ Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий
Выявление уровня токсичности почв пришкольного участка и прилежащих к нему территорий Технология кварцевого стекла
Технология кварцевого стекла Химиялық тепе-теңдік
Химиялық тепе-теңдік Біохімічний склад кормів - первинний показник їх технологічної й продуктивної можливості
Біохімічний склад кормів - первинний показник їх технологічної й продуктивної можливості Стекла. Структура и свойства
Стекла. Структура и свойства Емтихан сұрақтары
Емтихан сұрақтары Методы разделения белковых смесей. Электрофорез
Методы разделения белковых смесей. Электрофорез Косметические средства. Виды, состав и влияние на организм
Косметические средства. Виды, состав и влияние на организм Зависимость стадии конверсии метана от технологических параметров процесса в производстве метанола
Зависимость стадии конверсии метана от технологических параметров процесса в производстве метанола Получение этилена и изучение его свойств
Получение этилена и изучение его свойств Классификация неорганических веществ. Степень окисления
Классификация неорганических веществ. Степень окисления