Содержание
- 3. В различных реакциях, протекающих в растворе, мы обнаруживаем участие неизменных группировок атомов, выступающих либо в виде
- 4. Результатом реакции между растворами сульфата железа(II) и гексацианоферрата(III) калия является образование синего осадка турнбулевой сини .
- 5. Реакция между растворами хлорида железа(III) и роданида аммония наблюдается характерное ярко – красное окрашивание. Ион Fe3+
- 6. Реакция между растворами сульфата меди(II) и гидроксида аммония является образование ярко –голубого осадка. Ион Cu2+ взаимодействует
- 7. Поскольку у d- элементов в большинстве случаев остается незаполненным последний электронный слой, то можно предположить, что
- 8. Природу химических связей в комплексах, их строение и принципы их образования объясняет координационная теория Альфреда Вернера,
- 9. В каждом комплексном ионе имеется центральный атом -комплексообразователь, вокруг которого располагаются координированные им ионы и молекулы.
- 10. 3. Координационные атомы находятся во внутренней сфере комплексных соединений. Они называются лигандами (аддентами). 4. Центральный атом
- 11. [NH4] Cl лиганд центральный атом координационное число
- 12. Координационное число Внутренняя сфера Центральный атом Лиганд Внешняя сфера [Cu(NH3)4]SO4
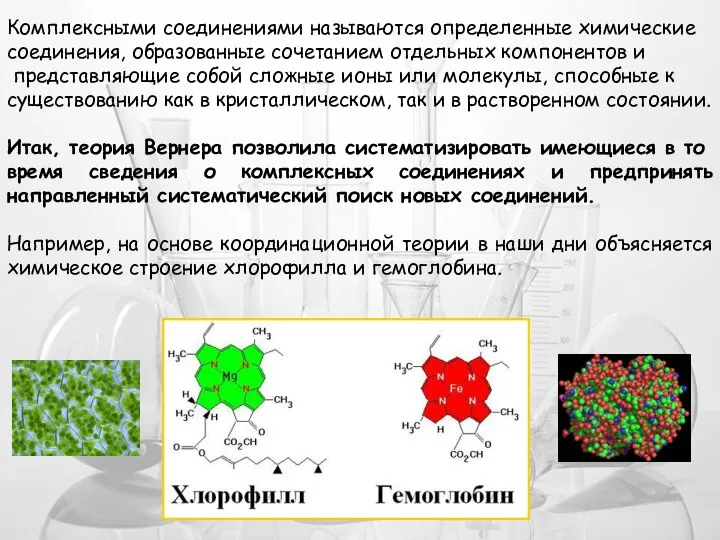
- 13. Комплексными соединениями называются определенные химические соединения, образованные сочетанием отдельных компонентов и представляющие собой сложные ионы или
- 14. Комплексообразователями могут быть как металлы, так и неметаллы. Но наиболее типичные комплексообразователи-катионы d-элементов Координационные соединения образованы
- 15. Свободные орбитали атомов кобальта являются вакантными для неподелённой электронной пары азота в молекуле аммиака. Так происходит
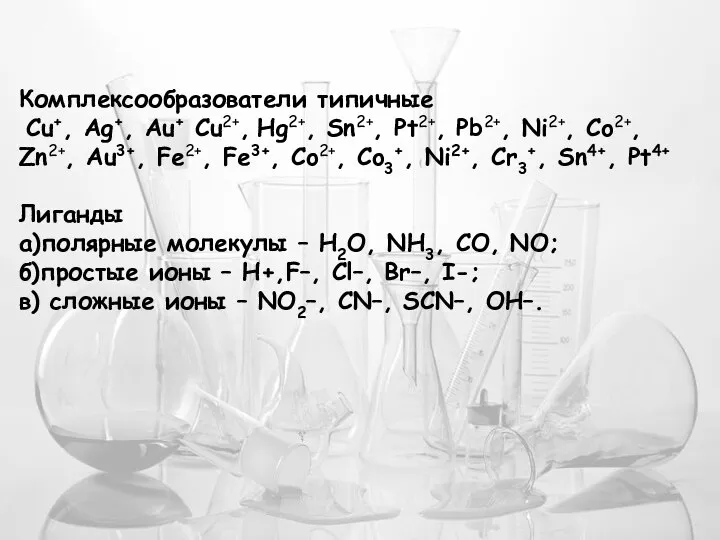
- 16. Комплексообразователи типичные Cu+, Ag+, Au+ Cu2+, Hg2+, Sn2+, Pt2+, Pb2+, Ni2+, Co2+, Zn2+, Au3+, Fe2+, Fe3+,
- 17. Диссоциация. [ Cu(NH3)4]SO4 ↔ [Cu(NH3)4]2+ + SO42- K3[Co(NO2)6]↔ 3 K+ + [Co(NO2)6]3- Комплексные ионы диссоциируют как
- 18. Реакции по центральному иону: а). обменные: [Ag(NH3)2] Cl + KJ ↔ AgJ↓ + KCl + 2NH3
- 19. Аналитическая химия . Используются в аналитической химии для идентификации неорганических и органических веществ. Первые вещества, отнесенные
- 20. Получение покрытий электрохимическим методом. Всем известны декоративные и защитные покрытия на металлических изделиях – оцинкованных, луженых,
- 21. Краски. Лаки. Цвет хаки, например, возникает при обработке хлопчатобумажных тканей солями железа и хрома, а затем
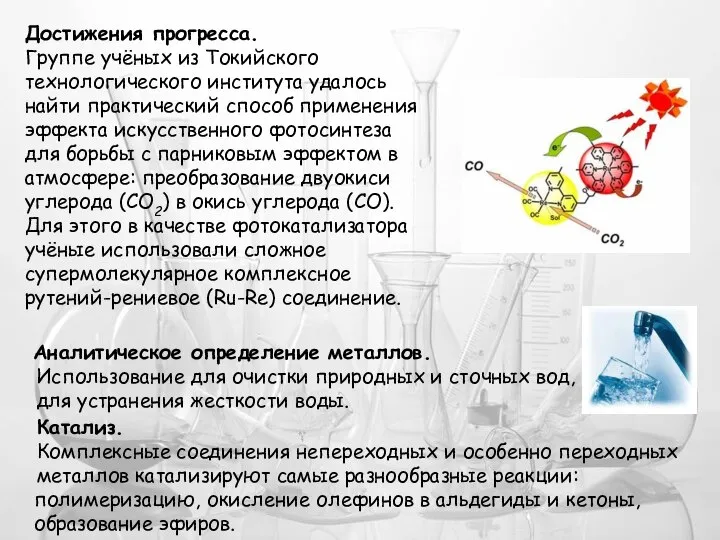
- 22. Достижения прогресса. Группе учёных из Токийского технологического института удалось найти практический способ применения эффекта искусственного фотосинтеза
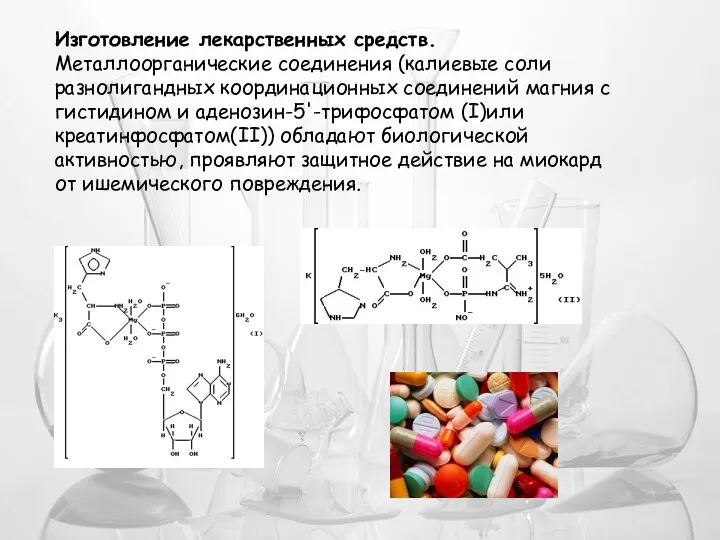
- 23. Изготовление лекарственных средств. Металлоорганические соединения (калиевые соли разнолигандных координационных соединений магния с гистидином и аденозин-5'-трифосфатом (I)или
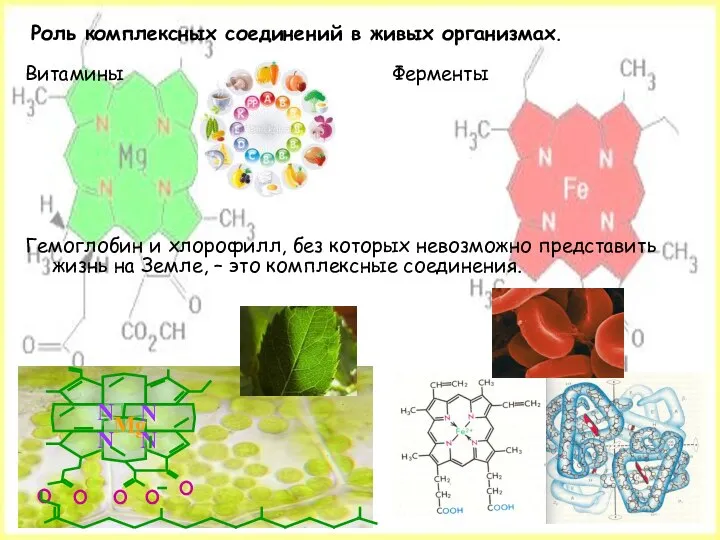
- 24. Роль комплексных соединений в живых организмах. Витамины Ферменты Гемоглобин и хлорофилл, без которых невозможно представить жизнь
- 25. Ионный контроль. В различных производствах возникают мешающие ионы металлов, которые удаляются или маскируются комплексами. Содержащиеся в
- 27. Скачать презентацию









![[NH4] Cl лиганд центральный атом координационное число](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405280/slide-10.jpg)
![Координационное число Внутренняя сфера Центральный атом Лиганд Внешняя сфера [Cu(NH3)4]SO4](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405280/slide-11.jpg)


![Диссоциация. [ Cu(NH3)4]SO4 ↔ [Cu(NH3)4]2+ + SO42- K3[Co(NO2)6]↔ 3 K+ +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405280/slide-16.jpg)
![Реакции по центральному иону: а). обменные: [Ag(NH3)2] Cl + KJ ↔](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1405280/slide-17.jpg)




 Внесение удобрений разбрасыванием
Внесение удобрений разбрасыванием Номенклатура органических соединений
Номенклатура органических соединений Презентація уроку «Різноманітність речовин. Поняття про прості та складні речовини, неорганічні та органічні речовини» Підготув
Презентація уроку «Різноманітність речовин. Поняття про прості та складні речовини, неорганічні та органічні речовини» Підготув Химические реакции
Химические реакции  Комплексные соединения
Комплексные соединения Химические свойства алкенов
Химические свойства алкенов Структурно-механiчнi (реологiчнi) властивостi харчових мас
Структурно-механiчнi (реологiчнi) властивостi харчових мас Химическая кинетика. (Лекция 4)
Химическая кинетика. (Лекция 4) Ископаемое сырье органической химии
Ископаемое сырье органической химии L-2-Chemical bonds
L-2-Chemical bonds Возникновение и развитие понятия «валентность» в период с 1850 по 1865 гг
Возникновение и развитие понятия «валентность» в период с 1850 по 1865 гг Нанотехнології в нашому житті. Загроза цивілізації, або стрибок у майбутнє
Нанотехнології в нашому житті. Загроза цивілізації, або стрибок у майбутнє Фізичні та хімічні явища. Хімічні реакції та явища, що їх супроводжують
Фізичні та хімічні явища. Хімічні реакції та явища, що їх супроводжують  Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Презентация по химии Галогены в организме человека
Презентация по химии Галогены в организме человека Презентация по Химии "Многоатомные спирты" - скачать смотреть бесплатно_
Презентация по Химии "Многоатомные спирты" - скачать смотреть бесплатно_ Решение экспериментальных задач по теме "Подгруппы азота и углерода"
Решение экспериментальных задач по теме "Подгруппы азота и углерода" Определение ректификации
Определение ректификации Степень окисления
Степень окисления Люминесцентный анализ
Люминесцентный анализ Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований
Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований Презентация по Химии "Витаминный алфавит" - скачать смотреть
Презентация по Химии "Витаминный алфавит" - скачать смотреть  Исследование свойств и применение в медицине алкалоидов. Извлечение алкалоидов из травы белены черной.
Исследование свойств и применение в медицине алкалоидов. Извлечение алкалоидов из травы белены черной. Периодическая система химических элементов Д.И. Менделеева и строение атома
Периодическая система химических элементов Д.И. Менделеева и строение атома Комплексні сполуки
Комплексні сполуки Нуклеиновые кислоты
Нуклеиновые кислоты Презентация по Химии "В даний час з нафти отримують тисячі продуктів." - скачать смотреть бесплатно
Презентация по Химии "В даний час з нафти отримують тисячі продуктів." - скачать смотреть бесплатно Белки простые и сложные
Белки простые и сложные