Содержание
- 2. Химическая кинетика – раздел физической химии, в котором химические превращения веществ изучаются как процессы, протекающие во
- 3. Прямая задача – определение скоростей химических реакций и концентраций участников этих реакций в любой момент времени
- 4. ХИМИЧЕСКАЯ КИНЕТИКА Химическая реакция – процесс, при котором происходит разрыв существующих связей и образование новых Необходимо:
- 5. Молекулярность, определяется числом частиц (молекул, атомов, ионов), принимающих участие в элементарном акте химической реакции Мономолекулярные реакции
- 6. Скорость гетерогенной реакции ХИМИЧЕСКАЯ КИНЕТИКА Скорость химической реакции определяется числом соударений (элементарных актов химической реакции), приводящих
- 7. ХИМИЧЕСКАЯ КИНЕТИКА 2 H2O2 = 2 H2O + O2 α C(H2O2), моль/л τ, с А Средняя
- 8. Скорость химической реакции зависит от ХИМИЧЕСКАЯ КИНЕТИКА Природы реагирующих веществ Концентрации реагирующих веществ Температуры Наличия катализатора
- 9. ХИМИЧЕСКАЯ КИНЕТИКА (К. Гульдберг, П.Вааге, 1867 г. Норвегия) скорость химической реакции при постоянной температуре прямо пропорциональна
- 10. Константа скорости химической реакции НЕ ЗАВИСИТ от концентраций (парциальных давлений) участников реакции ХИМИЧЕСКАЯ КИНЕТИКА и ЗАВИСИТ
- 11. ХИМИЧЕСКОЕ И ФАЗОВОЕ РАВНОВЕСИЕ Химическое равновесие - состояние системы, в котором скорость прямой реакции (v1) равна
- 12. Молекулярность определяется по числу молекул одновременное соударение которых приводит к химическому взаимодействию ХИМИЧЕСКАЯ КИНЕТИКА Порядок реакции
- 13. Порядок реакции устанавливается экспериментально при обработке данных кинетических исследований и основан на решении кинетического уравнения ХИМИЧЕСКАЯ
- 14. Необратимые реакции 0-ого порядка А → В n = 0 где k - константа скорости необратимой
- 15. Необратимые реакции 0-ого порядка А → В ХИМИЧЕСКАЯ КИНЕТИКА Графическое определение константы скорости необратимой реакции 0-го
- 16. Необратимые реакции 0-ого порядка ХИМИЧЕСКАЯ КИНЕТИКА Время (период) полупревращения (полураспада) - время, в течение которого концентрация
- 17. ХИМИЧЕСКАЯ КИНЕТИКА интегрируем k τ, c Необратимые реакции 1-ого порядка А → В n = 1
- 18. Порядок реакции устанавливается экспериментально при обработке данных кинетических исследований и основан на решении кинетического уравнения ХИМИЧЕСКАЯ
- 19. ХИМИЧЕСКАЯ КИНЕТИКА правило Вант-Гоффа γ - температурный коэффициент скорости реакции Якоб Хендрик Вант-Гофф При повышении температуры
- 20. Зависимость скорости химической реакции от температуры ХИМИЧЕСКАЯ КИНЕТИКА Допущения Аррениуса - реагировать могут не все молекулы,
- 21. Зависимость скорости химической реакции от температуры ХИМИЧЕСКАЯ КИНЕТИКА Eа, кДж – минимальная энергия необходимая для протекания
- 22. Аналитический метод Определение энергии активации ХИМИЧЕСКАЯ КИНЕТИКА
- 23. Графический метод Определение энергии активации ХИМИЧЕСКАЯ КИНЕТИКА
- 24. ХИМИЧЕСКАЯ КИНЕТИКА Катализатор – вещество, увеличивающее скорость химической реакции и не расходующееся в процессе взаимодействия Гомогенный
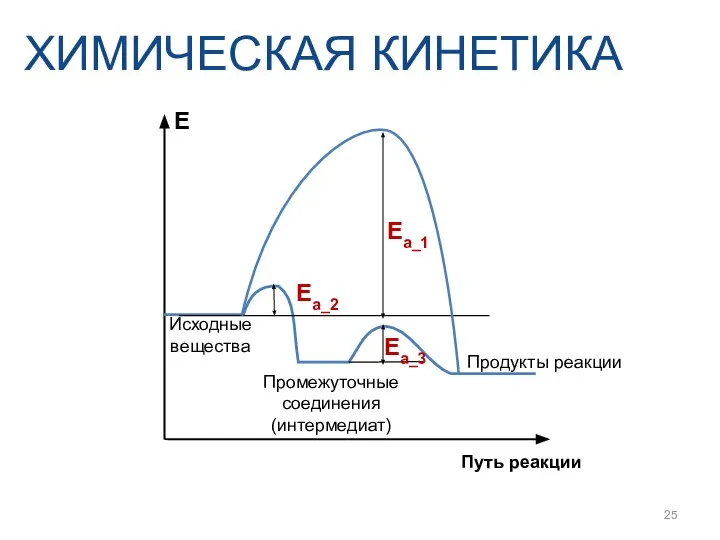
- 25. ХИМИЧЕСКАЯ КИНЕТИКА Ea_1 Ea_3 Ea_2 E Путь реакции Продукты реакции Промежуточные соединения (интермедиат) Исходные вещества
- 26. ХИМИЧЕСКАЯ КИНЕТИКА Сложные реакции - химические реакции, протекающие более чем в одну стадию Общая скорость таких
- 27. ХИМИЧЕСКАЯ КИНЕТИКА Классификация сложных реакций Последовательные реакции сложные реакции, протекающие таким образом, что вещества, образующиеся в
- 28. ХИМИЧЕСКАЯ КИНЕТИКА Классификация сложных реакций Цепные реакции реакции, состоящие из ряда взаимосвязанных стадий, когда частицы, образующиеся
- 29. ХИМИЧЕСКАЯ КИНЕТИКА Классификация сложных реакций Б.П. Белоусов А.М. Жаботинский Этого не может быть, потому что этого
- 30. ХИМИЧЕСКАЯ КИНЕТИКА Кинетика твердофазных реакций Механизм разрыва связи Связь между двумя атомами может разрываться по Гомолитическому
- 32. Скачать презентацию




























 Презентация по химии на тему: Бром
Презентация по химии на тему: Бром  Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7)
Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7) Основания. Гидроксид лития
Основания. Гидроксид лития Государственные лаборатории по контролю качества лекарственных средств. Основные элементы надлежащей лабораторной практики
Государственные лаборатории по контролю качества лекарственных средств. Основные элементы надлежащей лабораторной практики Воздух, его состав и значение
Воздух, его состав и значение Роль химии в сохранении окружающей среды
Роль химии в сохранении окружающей среды Моделирование химико-технологических процессов. Лекция № 1-2
Моделирование химико-технологических процессов. Лекция № 1-2 Цифровые лаборатории «Архимед» в изучении биологии и химии
Цифровые лаборатории «Архимед» в изучении биологии и химии Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Минералогия литофильных редких элементов. Вводные замечания
Минералогия литофильных редких элементов. Вводные замечания Строение органических молекул. (Лекция 2)
Строение органических молекул. (Лекция 2) Химическая связь. Урок 34-37
Химическая связь. Урок 34-37 Производные карбоновых кислот
Производные карбоновых кислот Цікаві факти про воду
Цікаві факти про воду  Презентация по Химии "Волокна" - скачать смотреть бесплатно
Презентация по Химии "Волокна" - скачать смотреть бесплатно Пропан, C3H8
Пропан, C3H8 Строение атома
Строение атома Химические элементы
Химические элементы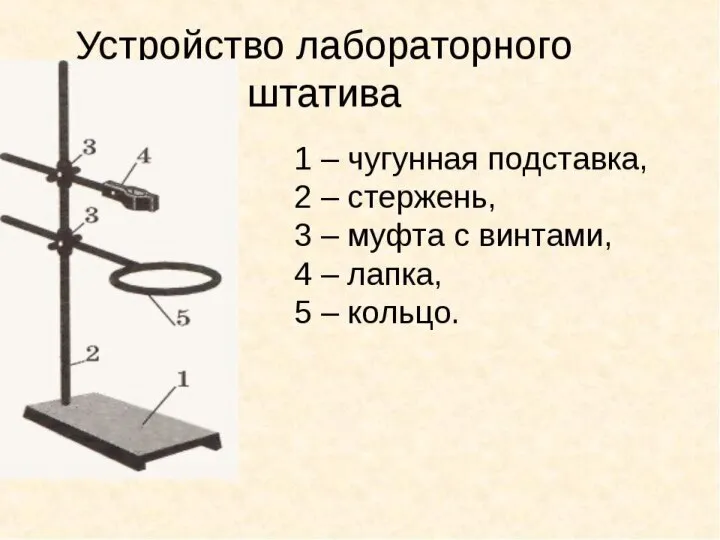 Устройство лабораторного штатива
Устройство лабораторного штатива Породы кислого состава
Породы кислого состава Кислоты
Кислоты Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Теория Кристаллического Поля
Теория Кристаллического Поля Электролиз. 9 класс
Электролиз. 9 класс Расчеты по химическим уравнениям. Алгоритм решения расчетных задач
Расчеты по химическим уравнениям. Алгоритм решения расчетных задач Метод электронного баланса для уравнивания окислительно-восстановительных реакций
Метод электронного баланса для уравнивания окислительно-восстановительных реакций Переработка угля
Переработка угля Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі