Содержание
- 2. Plan: 1. Introducere. Date istorice. 2. Electrovalenţa. 3. Covalenţa. 3.1. Teoria electronică a covalenţei. 3.2. Teoria
- 3. 1. Date importante în evoluţia teoriilor despre legăturile chimice În sec. XVIII filozofii au folosit noţiunea
- 4. Deşi proprietăţile substanţelor sunt infinit de variate, cercetarea acestora a dus la concluzia, că ele pot
- 8. Formarea combinaţiilor ionice respectă regulile empirice ale lui Fajans (1924), după care, un atom trece cu
- 9. Prin studierea substanţelor ionice în stare solidă prin metoda difracţiei razelor X, a fost dovedită existenta
- 10. Configuraţiile electronice ale ionilor simpli sunt: tipice: identice cu configuraţia electronică a heliului, 1s2 la: H−,
- 11. Caracteristicile legăturii ionice este de natură fizică şi constă din atracţia preponderent electrostatică între ioni; este
- 12. Proprietăţile substanţelor ionice au caracter salin (majoritatea sunt săruri); au puncte de topire (Tt) şi de
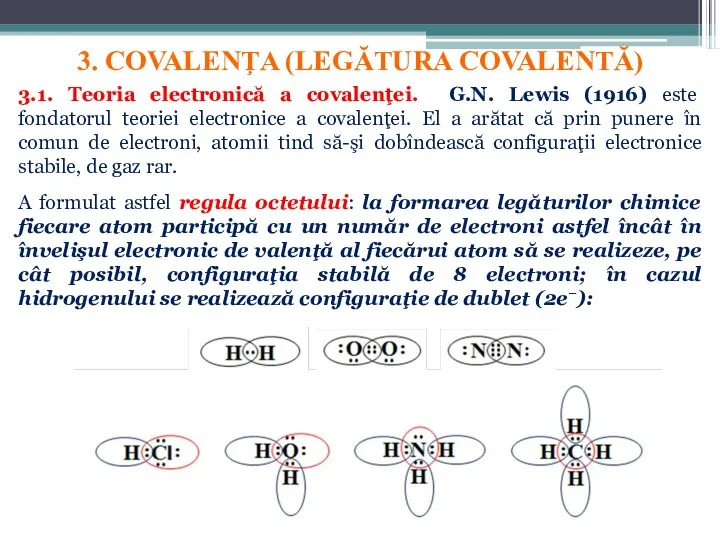
- 13. 3. COVALENŢA (LEGĂTURA COVALENTĂ) 3.1. Teoria electronică a covalenţei. G.N. Lewis (1916) este fondatorul teoriei electronice
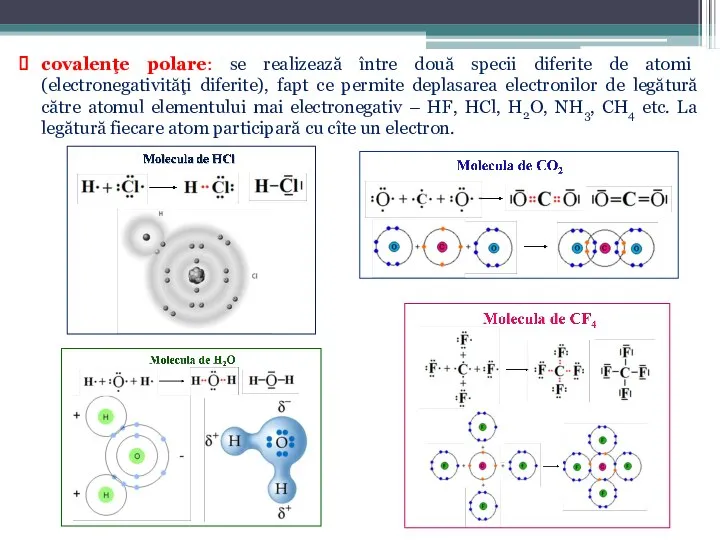
- 16. covalenţe polare: se realizează între două specii diferite de atomi (electronegativităţi diferite), fapt ce permite deplasarea
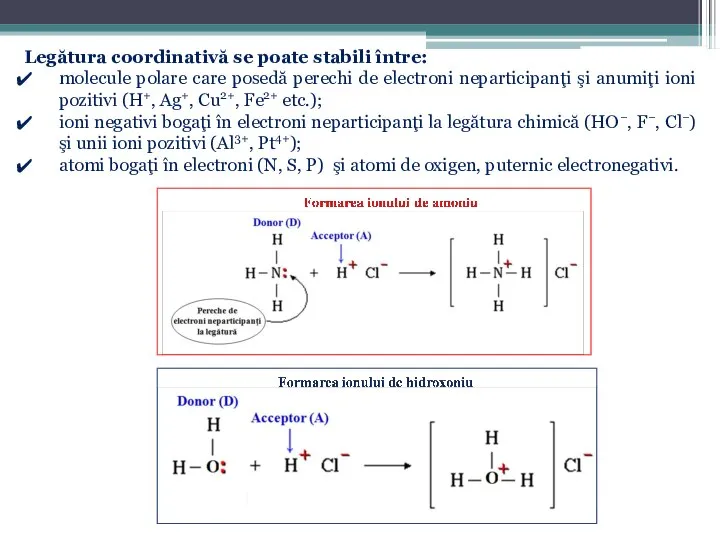
- 18. Legătura coordinativă se poate stabili între: molecule polare care posedă perechi de electroni neparticipanţi şi anumiţi
- 19. La formarea legăturii coordinative pot participa şi electronii aflaţi pe un nivel imediat inferior (interior) electronilor
- 20. Caracteristici ale covalenţei numărul covalenţelor este egal cu numărul de electroni puşi în comun (cuplaţi). ia
- 21. Regula octetului se respectă şi în moleculele poliatomice, ca, de exemplu, moleculele acizilor. Fie în calitate
- 22. 5. Din configuraţia stratului de valenţă al atomului de oxigen în stare fundamentală se observă că
- 23. Uneori pentru a diferenţia legăturile formate după mecanism de schimb de cele formate după mecanism donor-acceptor,
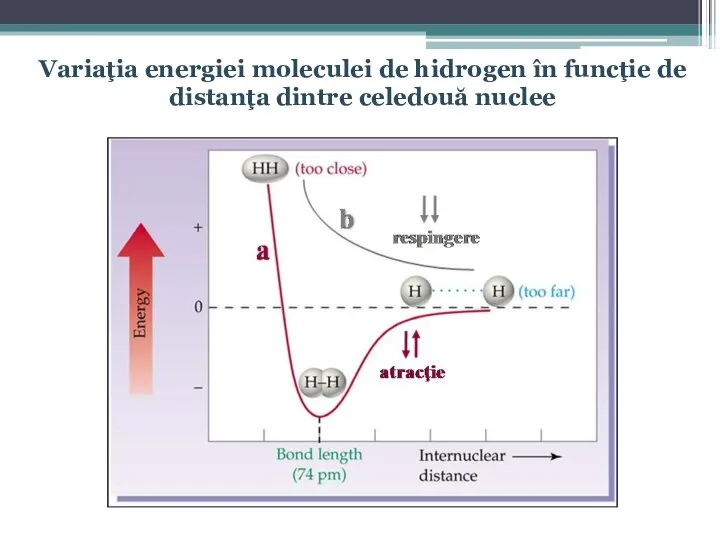
- 25. Variaţia energiei moleculei de hidrogen în funcţie de distanţa dintre celedouă nuclee
- 26. Conform mecanicii cuantice formarea legăturii chimice decurge prin cîteva etape: redistribuirea orbitalelor atomice; suprapunerea (întrepătrunderea) orbitalilor
- 27. Există două metode matematice de tratare a legăturii chimice: Metoda (teoria) legăturii de valenţă (LV) –
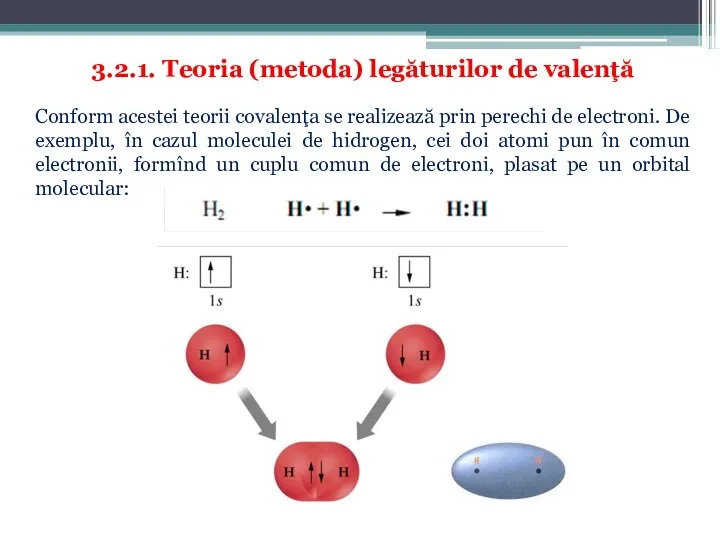
- 28. 3.2.1. Teoria (metoda) legăturilor de valenţă Conform acestei teorii covalenţa se realizează prin perechi de electroni.
- 29. 1. Molecula de BeCl2. Configuraţia electronică a învelişului de valenţă a atomului de clor este 3s23p5:
- 30. Hibridizarea este redistribuirea orbitalilor de diferită formă şi energie ai unui atom cu formarea orbitalilor echivalenţi
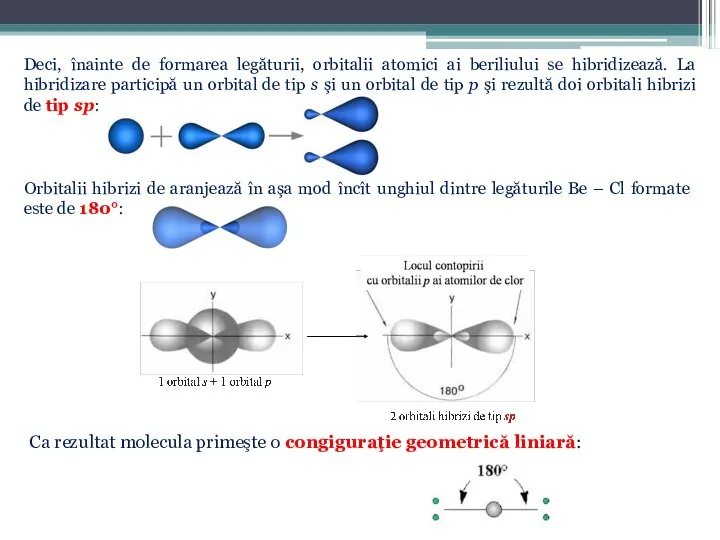
- 31. Deci, înainte de formarea legăturii, orbitalii atomici ai beriliului se hibridizează. La hibridizare participă un orbital
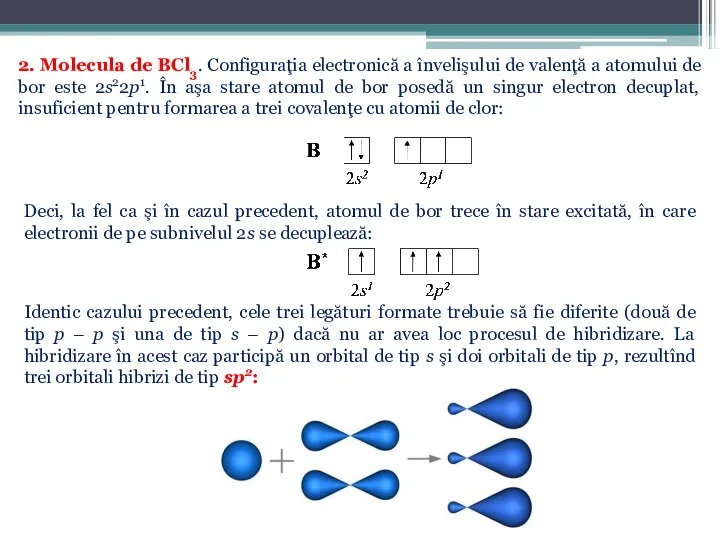
- 32. 2. Molecula de BCl3. Configuraţia electronică a învelişului de valenţă a atomului de bor este 2s22p1.
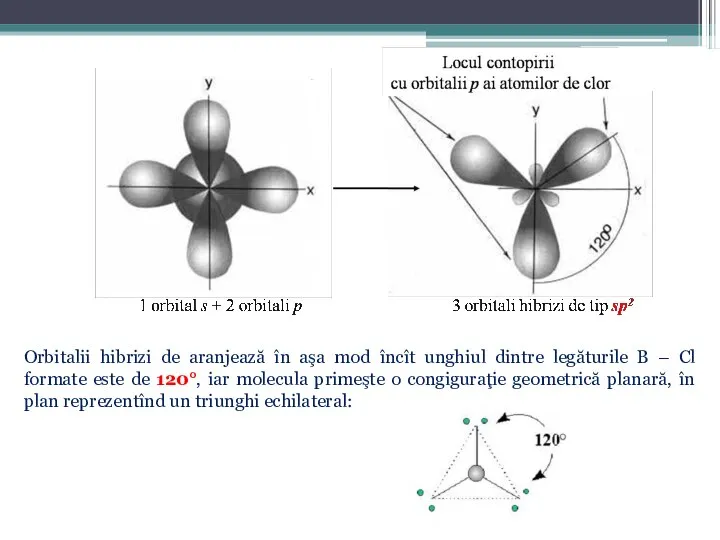
- 33. Orbitalii hibrizi de aranjează în aşa mod încît unghiul dintre legăturile B – Cl formate este
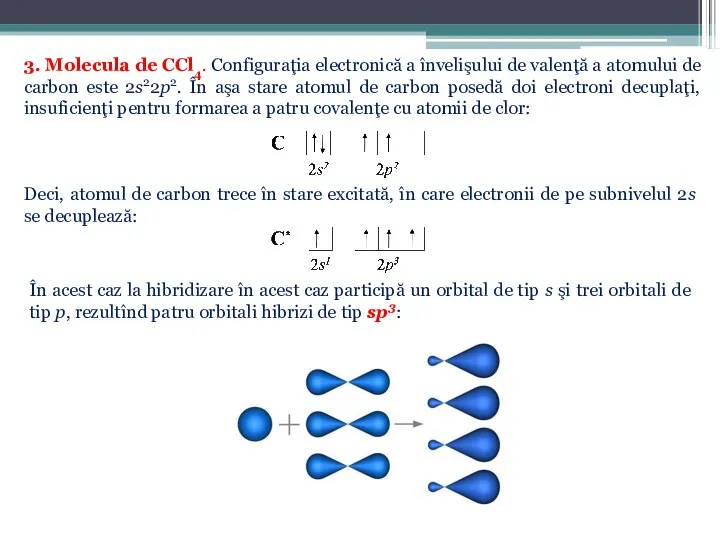
- 34. 3. Molecula de CCl4. Configuraţia electronică a învelişului de valenţă a atomului de carbon este 2s22p2.
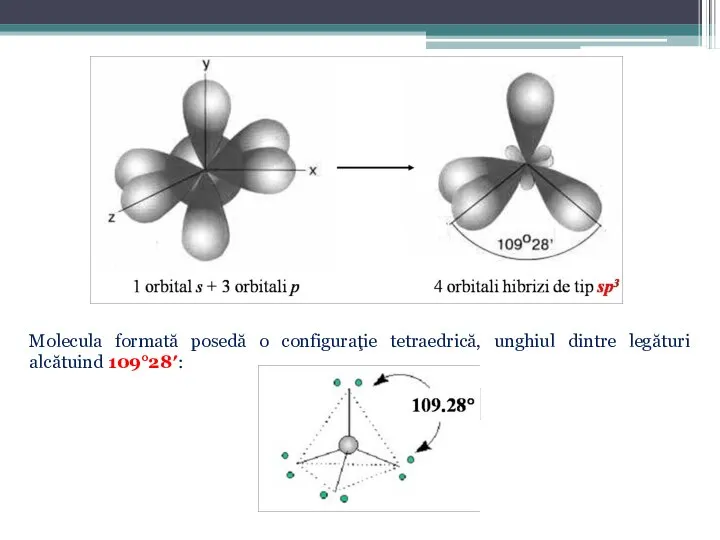
- 35. Molecula formată posedă o configuraţie tetraedrică, unghiul dintre legături alcătuind 109°28′:
- 36. 4. Molecula de PCl5. Configuraţia electronică a învelişului de valenţă a atomului de fosfor este 3s23p3.
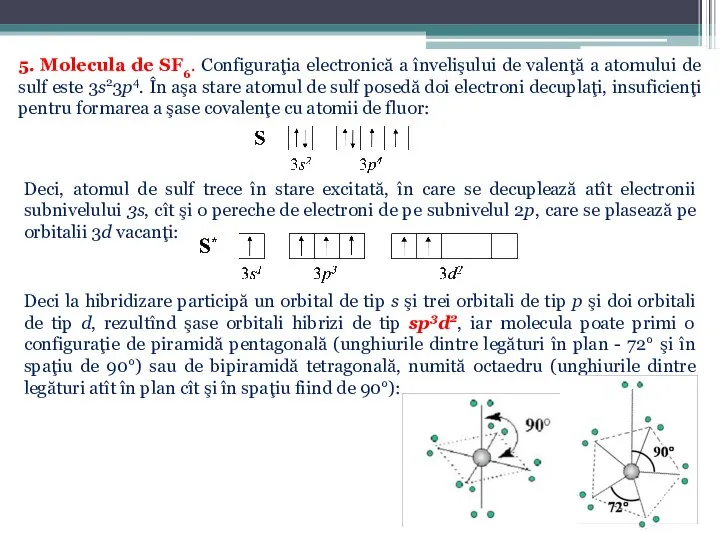
- 37. 5. Molecula de SF6. Configuraţia electronică a învelişului de valenţă a atomului de sulf este 3s23p4.
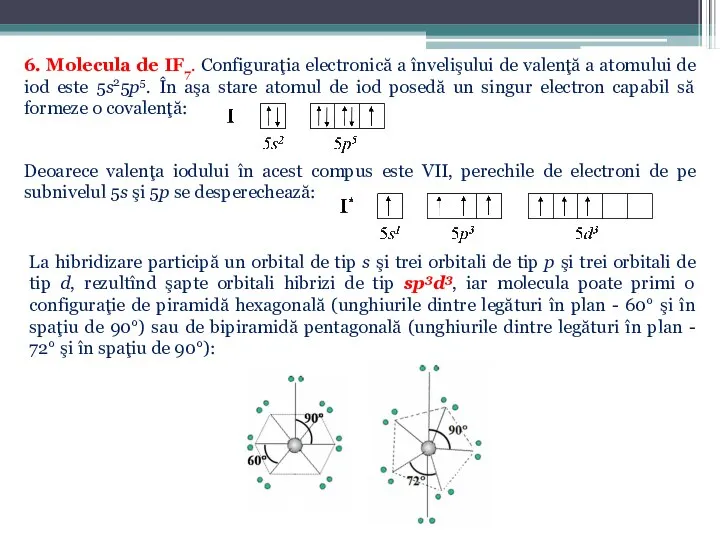
- 38. 6. Molecula de IF7. Configuraţia electronică a învelişului de valenţă a atomului de iod este 5s25p5.
- 39. 7. Molecula de NH3. În molecula de amoniac legătura chimică se realizează prin trei covalenţe între
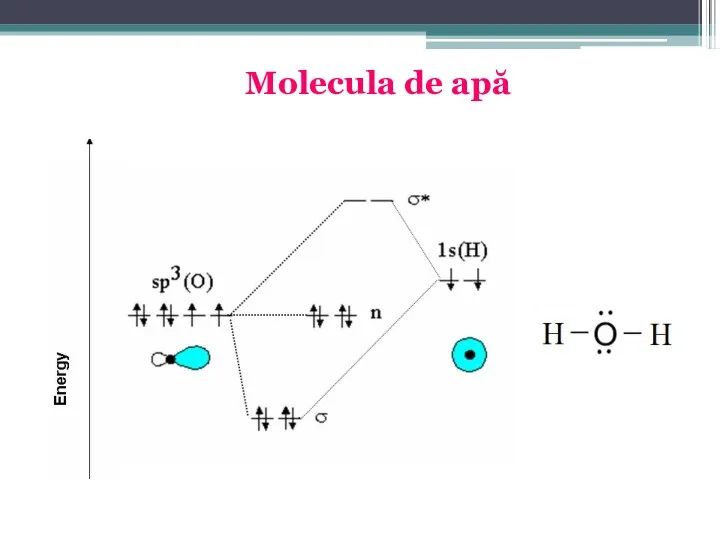
- 40. 8. Molecula de H2O. În molecula de apă legătura chimică se realizează prin două covalenţe între
- 41. Pentru a stabili tipul hibridizării şi, respectiv, forma spaţială a moleculei, se procedează în următorul mod:
- 42. Relaţia tipul de hibridizare – formă spaţială
- 43. Pentru a stabili tipul de hibridizare în moleculele poliatomice se folosesc formulele electronice ale acestora. De
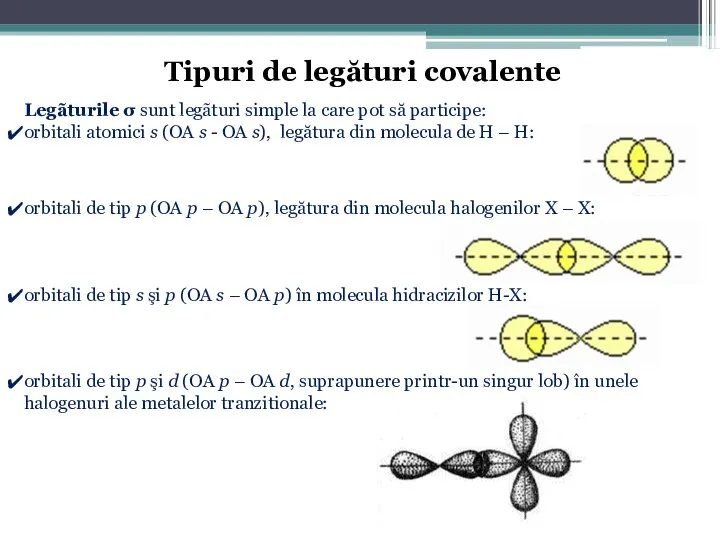
- 46. Legãturile δ sunt mai rar întâlnite, se formează prin suprapunerea concomitentã a câte 4 lobi ai
- 47. 3.2.2. Teoria (metoda) orbitalilor moleculari În acest model se porneşte de la existenţa orbitalilor electronici atomici,
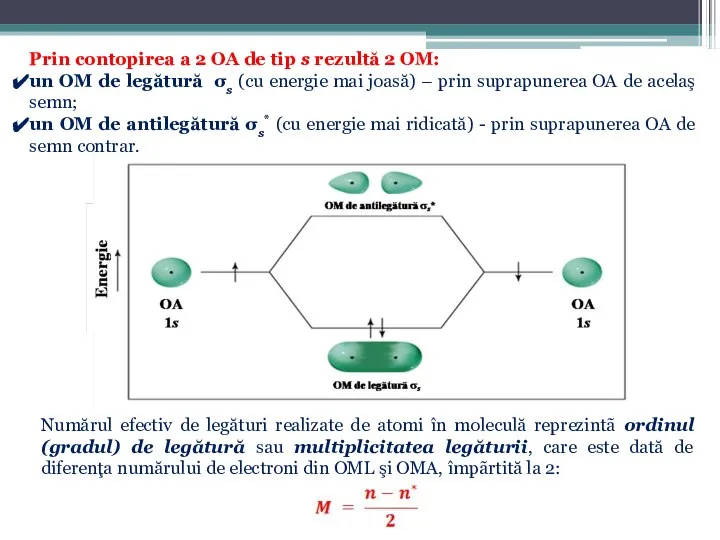
- 48. Prin contopirea a 2 OA de tip s rezultă 2 OM: un OM de legătură σs
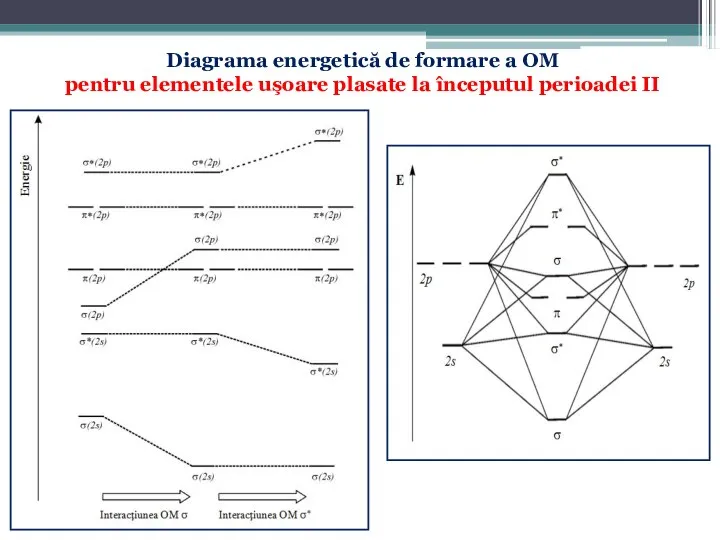
- 58. Diagrama energetică de formare a OM pentru elementele uşoare plasate la începutul perioadei II
- 59. Diagrama energetică a OM pentru molecula de B2 şi C2 (fază gazoasă!!!)
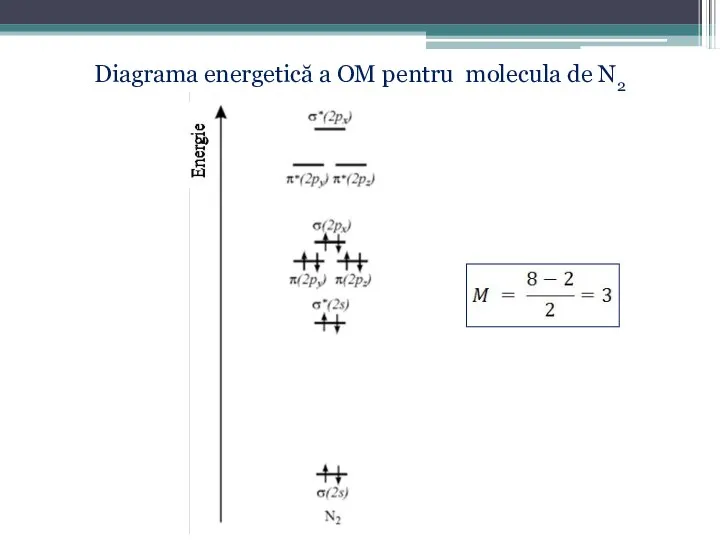
- 60. Diagrama energetică a OM pentru molecula de N2
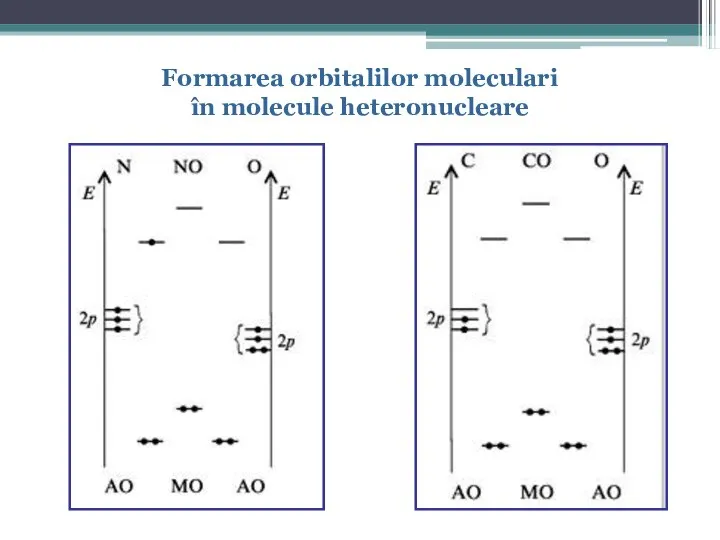
- 62. Formarea orbitalilor moleculari în molecule heteronucleare
- 66. 3.3. Proprietăţile covalenţei şi a substanţelor cu legătură covalentă este rigidă, deoarece atomii legaţi covalent ocupă
- 67. Substanţele covalente (moleculare) se prezintă în toate cele trei stări de agregare. Multe din ele sunt
- 68. Proprietăţile substanţelor cu legătură covalentă depind în mare măsură de tipul reţelei cristaline. De exemplu este
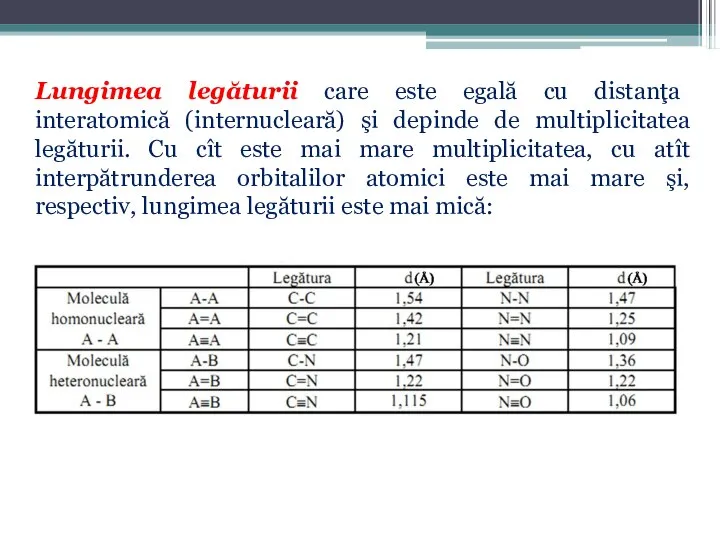
- 69. Lungimea legăturii care este egală cu distanţa interatomică (internucleară) şi depinde de multiplicitatea legăturii. Cu cît
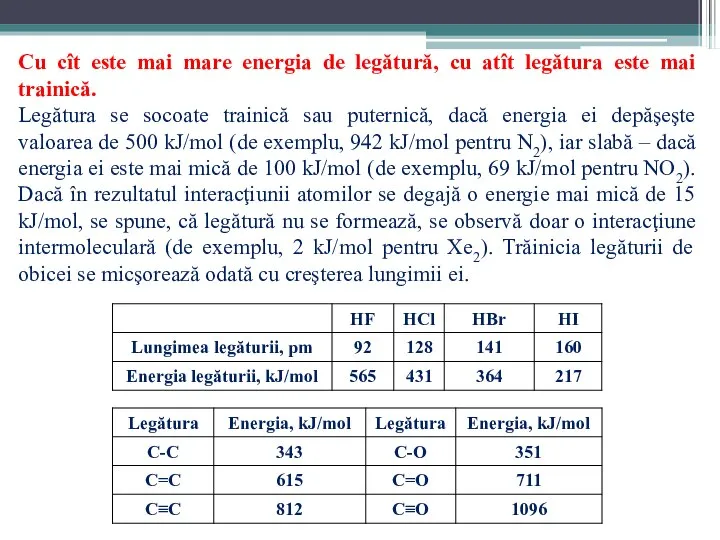
- 70. Energia E0, necesară pentru a rupe legătura dintre atomi şi ai îndepărta unul de altul la
- 71. Cu cît este mai mare energia de legătură, cu atît legătura este mai trainică. Legătura se
- 72. 4. LEGĂTURA METALICĂ Metalele se deosebesc fundamental de celelalte substanţe, atît sub formă elementară cît şi
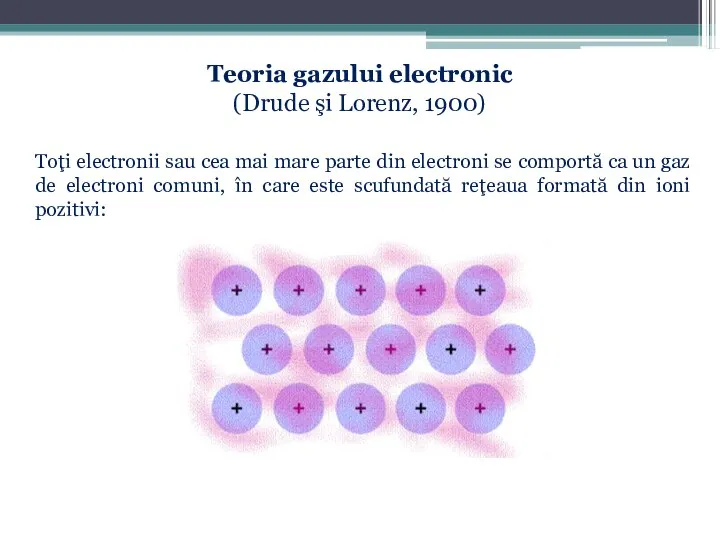
- 73. Teoria gazului electronic (Drude şi Lorenz, 1900) Toţi electronii sau cea mai mare parte din electroni
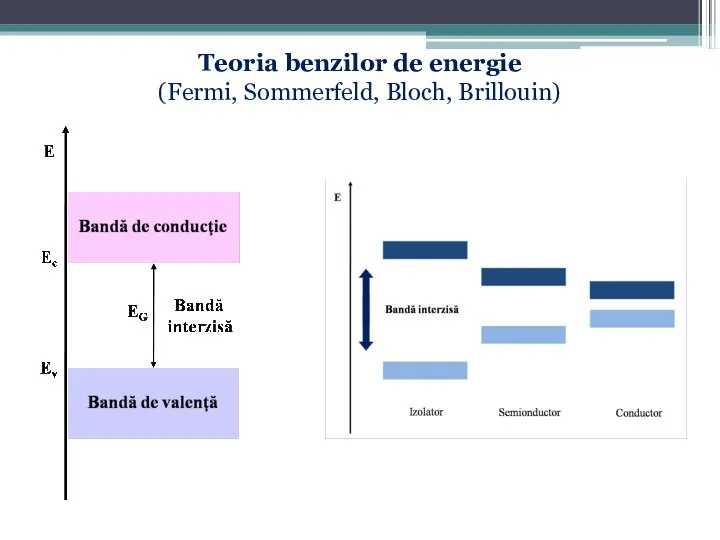
- 74. Teoria benzilor de energie (Fermi, Sommerfeld, Bloch, Brillouin)
- 75. 6. INTERACŢIUNI INTERMOLECULARE Forțe van der Waals Faptul că gazele compuse din atomi (He, Ar, Ne
- 77. Скачать презентацию










































 Круговорот азота в природе
Круговорот азота в природе ЛР и ЛРС содержащие фитоэкдизоны
ЛР и ЛРС содержащие фитоэкдизоны Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию ки
Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию ки Координационные соединения
Координационные соединения Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Соединения галогенов
Соединения галогенов Азот и фосфор
Азот и фосфор Химическая технология органических веществ
Химическая технология органических веществ Каталитикалық риформинг
Каталитикалық риформинг Аминокислоты
Аминокислоты Роботу виконав: Желєзний Влад
Роботу виконав: Желєзний Влад  Основания, их состав, номенклатура и основные представители
Основания, их состав, номенклатура и основные представители Элементный, фракционный и химический состав нефти. Классификация нефтей
Элементный, фракционный и химический состав нефти. Классификация нефтей Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3)
Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3) Минералы алюминия
Минералы алюминия Основания: классификация и свойства в свете ТЭД
Основания: классификация и свойства в свете ТЭД Ионная полимеризация. Катионная полимеризация
Ионная полимеризация. Катионная полимеризация Материаловедение. Основы металловедения
Материаловедение. Основы металловедения Изотермический процесс в реакционном объеме. (Тема 6.2)
Изотермический процесс в реакционном объеме. (Тема 6.2) Фенолы Простые эфиры
Фенолы Простые эфиры Альдегиды вокруг нас
Альдегиды вокруг нас Минералы. Определение минералов
Минералы. Определение минералов Курс хімії за 11 клас
Курс хімії за 11 клас Презентация по Химии "Атоми,молекули, йони, хімічні елементи, їхні назви й символи" - скачать смотреть бесплатно
Презентация по Химии "Атоми,молекули, йони, хімічні елементи, їхні назви й символи" - скачать смотреть бесплатно НАШ НЕБЕЗПЕЧНИЙ ПОБУТ Презентація на тему того,про що ми не думаємо у повсякденному житті.
НАШ НЕБЕЗПЕЧНИЙ ПОБУТ Презентація на тему того,про що ми не думаємо у повсякденному житті.  Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные
Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные Кремний и его соединения
Кремний и его соединения Презентация по Химии "Химия. Классификация химических реакций" - скачать смотреть бесплатно
Презентация по Химии "Химия. Классификация химических реакций" - скачать смотреть бесплатно