Содержание
- 2. План лекции: Использование ОВР в аналитической химии. Типы ОВР. Количественное описание ОВР. Константа равновесия ОВР. Устойчивость
- 3. Использование ОВР в аналитической химии При пробоподготовке для переведения в раствор пробы. Для разделения смеси ионов.
- 4. Например, при гипоксии (состояние кислородного голодания) происходит замедление транспорта Н+ и е – в дыхательной цепи
- 5. Типы ОВР 1. Межмолекулярные – изменяются степени окисления (С.О.) атомов элементов, входящих в состав разных веществ:
- 6. 2. Внутримолекулярные – окислитель и восстановитель - атомы одной молекулы:
- 7. 3. Самоокисления – самовосстановления (диспропорционирования) – один и тот же элемент повышает и понижает С.О. Cl2
- 8. Количественное описание ОВР Например, чем сильнее основание, тем больше его сродство в протону. Также и сильный
- 9. Рассматривая ОВ пару в целом, можно записать схематичное уравнение реакции: Ox + nē = Red Равновесие
- 10. При температуре 298 К уравнение Нернста принимает вид:
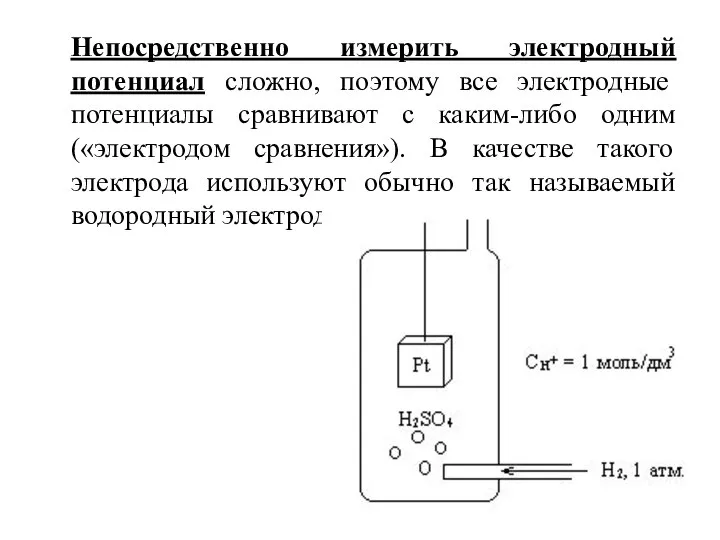
- 11. Непосредственно измерить электродный потенциал сложно, поэтому все электродные потенциалы сравнивают с каким-либо одним («электродом сравнения»). В
- 12. В уравнении Нернста можно использовать вместо активностей ионов их концентрации, но тогда необходимо знать коэффициенты активностей
- 13. На силу окислителя и восстановителя могут влиять: значение рН, реакции осаждения реакции комплексообразования. Тогда свойства редокс-пары
- 14. Для расчета реального потенциала полуреакций, получаемых сочетанием ОВР и реакций осаждения, используются формулы: ∙ если окисленная
- 15. ∙ если восстановленная форма представляет собой малорастворимое соединение:
- 16. Сочетание ОВР и реакций комплексообразования ∙ если окисленная форма связана в комплекс:
- 17. ∙ если восстановленная форма связана в комплекс:
- 18. ∙ если обе формы связаны в комплекс:
- 19. Сочетание ОВР и реакций протонирования если протонируется окисленная форма:
- 20. если протонируется восстановленная форма:
- 21. если протонируются обе формы:
- 22. если реакция протекает по следующему уравнению: Ox + mH+ + nē = Red + H2O тогда
- 23. Константа равновесия ОВР Расчет константы равновесия для реакции: Sn2+ + 2Fe3+ = Sn4+ + 2Fe2+ Константа
- 24. Выражения для реальных ОВ потенциалов каждой редокс-пары будут выглядеть следующим образом:
- 25. В условиях равновесия:
- 26. Проведя математические операции, получим: К = 1021
- 27. Используя приведенное вычисление константы равновесия, получим для любого обратимого ОВ процесса при 20 0С следующее уравнение:
- 28. Например, в цериметрии (окислитель Се4+): Fe2+ + Се4+ = Fe3+ + Се3+ К = 1011,4 =
- 30. Скачать презентацию


























 Золото. Свойство золота
Золото. Свойство золота Д. И. Менделеев человек - загадка Автор: Ким Н. В. учитель химии 2008 год.
Д. И. Менделеев человек - загадка Автор: Ким Н. В. учитель химии 2008 год.  Сутегі. Оттегі. Сутекті алу және оның қасиеттерін зерттеу
Сутегі. Оттегі. Сутекті алу және оның қасиеттерін зерттеу Полярография және оның фармацияда қолданылуы
Полярография және оның фармацияда қолданылуы Нуклеиновые кислоты
Нуклеиновые кислоты Наука химия
Наука химия Тема:Хімія
Тема:Хімія  Электролитическая диссоциация
Электролитическая диссоциация Кадмий (Cadmium)
Кадмий (Cadmium) Мұнай құрамындағы тұздың мөлшерін анықтау
Мұнай құрамындағы тұздың мөлшерін анықтау Введение в органическую химию
Введение в органическую химию Химические составляющие человеческого организма
Химические составляющие человеческого организма Основы химической термодинамики
Основы химической термодинамики Метаморфические горные породы
Метаморфические горные породы Масс-спектры спиртов и фенолов
Масс-спектры спиртов и фенолов Комплексные соединения
Комплексные соединения Процессы соосаждения. Радионуклид без носителя. Индикаторные количества
Процессы соосаждения. Радионуклид без носителя. Индикаторные количества Арены. Бензол
Арены. Бензол Химическое равновесие и его смещение
Химическое равновесие и его смещение Минералы свинца
Минералы свинца Количественный анализ. Гравиметрия
Количественный анализ. Гравиметрия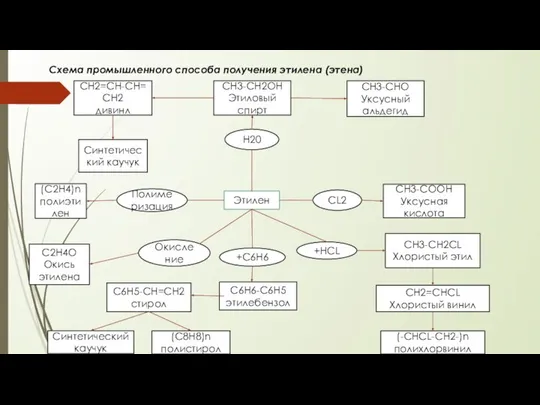 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена) Презентация по Химии "Вода" - скачать смотреть
Презентация по Химии "Вода" - скачать смотреть  Расчеты по уравнениям химической реакции
Расчеты по уравнениям химической реакции Темір және оның қосылыстары
Темір және оның қосылыстары Металлы
Металлы Электролитическая диссоциация. (Лекция 14)
Электролитическая диссоциация. (Лекция 14) Золото
Золото