Содержание
- 2. Лекция 12 Липолиз Обмен кетоновых тел
- 3. Актуальность темы Липолиз – процессы катаболизма (мобилизации) жира в организме: гидролиз ТАГ – энергетического «запаса» в
- 4. План лекции Гидролиз ТАГ Окисление ВЖК Нарушения процесса окисления ВЖК Регуляция липолиза Метаболизм кетоновых тел
- 5. Цель лекции Знать: биохимические основы процессов мобилизации жиров (гидролиз ТАГ и бета-окисление ВЖК) и метаболизма кетоновых
- 6. Гидролиз ТАГ Происходит при голодании, длительной физической нагрузке, стрессе, преимущественно в жировой ткани. Активация липолиза сопровождает
- 7. Окисление ВЖК ВЖК транспортируются через ЦПМ путем простой диффузии Транспорт ВЖК в цитозоле осуществляют белки-переносчики –
- 8. Этапы катаболизма ВЖК в тканях Активация ВЖК в цитоплазме с образованием ацил-КоА (реакция рассмотрена в предыдущих
- 9. Окисление ВЖК: этап 2 Транспорт ацил-КоА в матрикс митохондрий Транспорт ацил-КоА в митохондриальный матрикс осуществляется с
- 10. Ферменты транспорта ВЖК в митохондрии Карнитинацилтрансфераза I – «работает» в межмембранном пространстве (переносит остаток ВЖК с
- 11. Образование ацилкарнитина – транспортной формы ВЖК в митохондрии
- 13. Окисление ВЖК: этап 3 бета-окисление ВЖК β-окисление ВЖК – процесс циклический Каждый оборот цикла заканчивается образованием
- 14. Ход реакций бета-окисления ВЖК ацил-КоА + FАD+ → ∆2-транс-еноил-КоА + FАDН2 (ацил-КоА дегидрогеназа, окисление между α-β-С)
- 16. Полное окисление ВЖК Полное окисление ВЖК в митохондриях до СО2 и Н2О включает 3 этапа: β-окисление
- 17. Энергетика процесса полного окисления насыщенной ВЖК [n/2 · 12 + (n/2 – 1) · 5] –
- 18. Рассчитайте энергетический выход полного окисления пальмитиновой и стеариновой кислот (старайтесь не пользоваться формулой, следуйте логике событий!)
- 19. Другие пути окисления ВЖК без синтеза АТФ β-окисление в пероксисомах: включается при диете, богатой жирами обеспечивает
- 20. Нарушения процесса окисления ВЖК Причины: Недостаточность карнитина или карнитинацилтрансферазы Мышечная слабость, миалгия, спазмы, миоглобинурия, гипогликемия (по
- 21. Регуляция липолиза Гормональная регуляция путем изменения активности ключевых ферментов липолиза Аллостерическая регуляция ферментов липолиза Цикл Рэндла.
- 22. Гормональная регуляция липолиза Гидролиз ТАГ и окисление ВЖК происходит в период голодания (глюкагон, кортизол), стрессе и
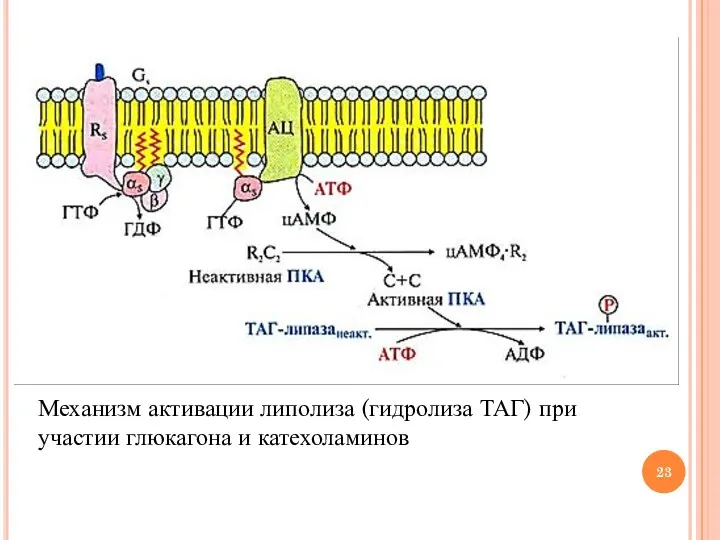
- 23. Механизм активации липолиза (гидролиза ТАГ) при участии глюкагона и катехоламинов
- 24. Аллостерическая регуляция липолиза Карнитинацилтрансфераза I – аллостерический фермент: Активаторы: АДФ, АМФ (мышцы), ацил-КоА (печень) Ингибиторы: АТФ
- 25. Цикл Рэндла Цикл Рэндла – саморегулируемая система субстратной координации (без участия гормонов) энергетического обмена углеводов и
- 26. Схема и механизм работы цикла Рэндла ↓ глюкоза в крови → ↑ липолиз (гидролиз ТАГ в
- 27. Синтез кетоновых тел Субстрат: ацетил-КоА, образованный в ходе β-окисления ВЖК Место синтеза: митохондрии гепатоцитов Условия активации
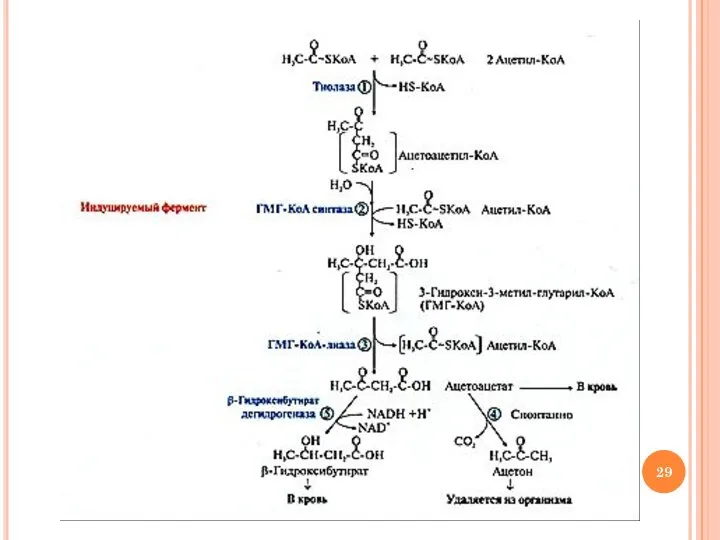
- 28. Ход процесса синтеза кетоновых тел соединение 2-х молекул ацетил-КоА с образованием ацетоацетил-КоА и HS-КоА (тиолаза) присоединение
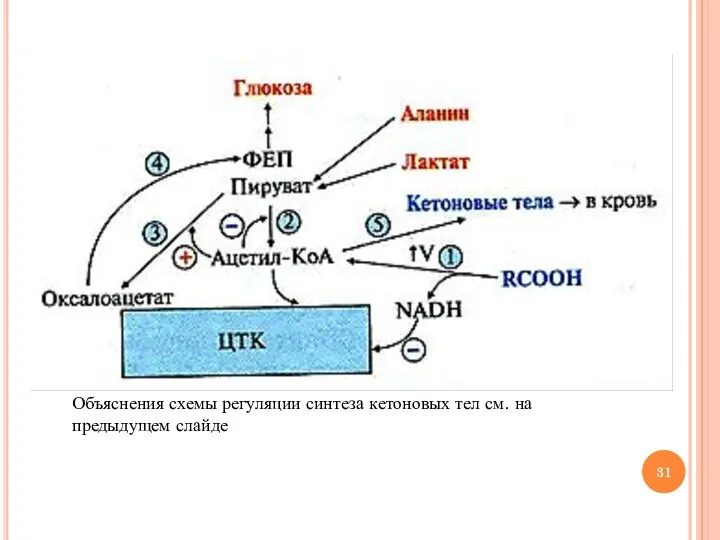
- 30. Регуляция синтеза кетоновых тел активация липолиза в печени под действием глюкагона и адреналина приводит к повышению
- 31. Объяснения схемы регуляции синтеза кетоновых тел см. на предыдущем слайде
- 32. Окисление кетоновых тел Место окисления: митохондрии клеток, кроме гепатоцитов (отсутствует сукцинил-КоА-ацетоацетат трансфераза). Не происходит в эритроцитах
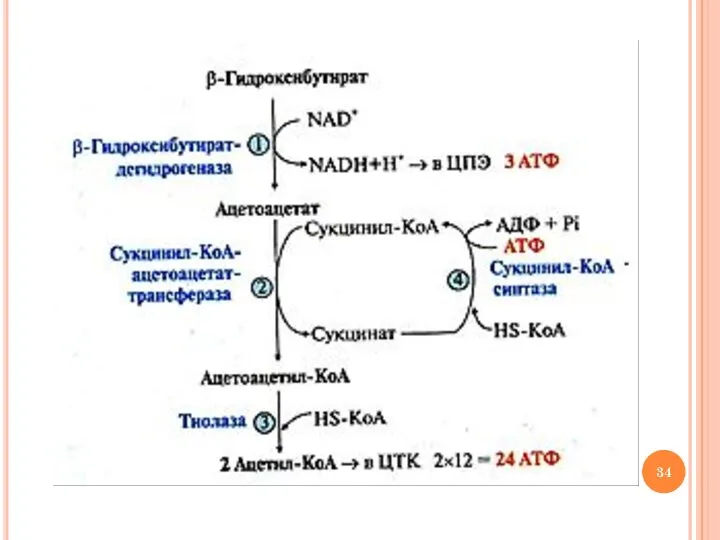
- 33. Ход процесса окисления кетоновых тел окисление β-гидроксибутирата с образованием ацетоацетата и NADН (β-гидроксибутират дегидрогеназа), который окисляется
- 35. Заключение Мобилизация жиров, или липолиз: окисление ТАГ и ВЖК – процессы, обеспечивающие организм энергией при голодании,
- 37. Скачать презентацию






























 Реакционная способность фенольных антиоксидантов при взаимодействии с пероксирадикалами
Реакционная способность фенольных антиоксидантов при взаимодействии с пероксирадикалами Химия
Химия Железо и его соединения
Железо и его соединения Физико-химические методы анализа
Физико-химические методы анализа Дисперсные системы в медицине и пищевой промышленности
Дисперсные системы в медицине и пищевой промышленности Выполнил: А. М. Галенко, учитель химии МОУ СОШ № 67 г. Волгограда
Выполнил: А. М. Галенко, учитель химии МОУ СОШ № 67 г. Волгограда  Хроматографические методы анализа. Метод газовой хроматографии
Хроматографические методы анализа. Метод газовой хроматографии Схема катаболизма углеродного скилета аминокислот
Схема катаболизма углеродного скилета аминокислот Коллоидты жүйелердің коагуляциялық және кристаллизациялық құрылымдары
Коллоидты жүйелердің коагуляциялық және кристаллизациялық құрылымдары Строение атома алюминия. Физические и химические свойства алюминия
Строение атома алюминия. Физические и химические свойства алюминия Цифровые лаборатории «Архимед» в изучении биологии и химии
Цифровые лаборатории «Архимед» в изучении биологии и химии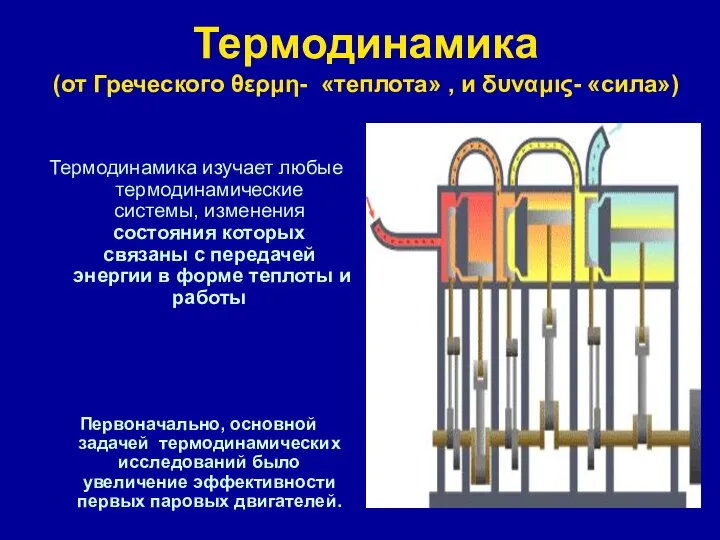 Термодинамика. Химическая термодинамика
Термодинамика. Химическая термодинамика Химический состав продуктов питания
Химический состав продуктов питания Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10)
Цинк и его сплавы. Антифрикционные сплавы, их маркировка и область применения. Олово, свинец и их свойства. (Тема 10) Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Химические элементы O2 и N2
Химические элементы O2 и N2 Колообіг нітрогену Колообіг речовин — основна властивість, характерна риса біосфери.
Колообіг нітрогену Колообіг речовин — основна властивість, характерна риса біосфери.  Карбоновые кислоты
Карбоновые кислоты Сущность процесса электролитической диссоциации
Сущность процесса электролитической диссоциации 6 классов ферментов и тривиальные названия некоторых основных групп
6 классов ферментов и тривиальные названия некоторых основных групп Методы контроля и анализа веществ
Методы контроля и анализа веществ Интегрированный урок биологии и химии с применением информационных технологий
Интегрированный урок биологии и химии с применением информационных технологий Химический элемент алюминий
Химический элемент алюминий Дисперсные системы
Дисперсные системы Химия. Введение
Химия. Введение Кристаллы вокруг нас
Кристаллы вокруг нас Свойства нейтральных атомов. Лекция 4
Свойства нейтральных атомов. Лекция 4 Молекулы и атомы. Простые и сложные вещества
Молекулы и атомы. Простые и сложные вещества