Содержание
- 2. Масс-спектрометрия К концу ХХ века инструментальные физико-химические методы анализа стали неотъемлемой частью экспериментальной работы исследователя, работающего
- 3. Масс-спектрометрия По шутливому выражению одного из «отцов» органической масс-спектрометрии Фреда Мак-Лафферти, «если химическую задачу нельзя решить
- 4. Масс-спектрометрия Масс-спектрометрия является физико-химическим методом анализа, заключающимся в переводе молекул образца в ионизированную форму с последующим
- 5. Масса самого тяжелого иона в спектре, как правило, соответствует молекулярной массе анализируемого соединения. Принято представлять масс-спектр
- 6. Масс-спектрометрия применяется для решения геохимических и космохимических проблем, задач комбинаторной химии, иммунологии, медицины, биологии и т.д.
- 7. Транспортировка самого большого в мире спектрометра (эксперимент «KATRIN», который будет использоваться в том числе и в
- 8. Достоинства масс-спектрометрии Молекулярная масса вещества. Рекорд 110,000,000 Да = 1,8*10-10 микрограмм. Непревзойденная чувствительность. Рутина 10-12 г,
- 9. Минусы масс-спектрометрии Для высокоточных измерений требуются громоздкие и чаще всего дорогие масс-спектрометры Необходим отбор вещества, т.е.
- 10. Общий принцип работы и устройство масс-спектрометра Поскольку масс-спектрометрия имеет дело с положительными или отрицательными ионами, после
- 11. Квадрупольные масс-спектрометры Прорыв масс-спектрометрии произошел в 1970-х с внедрением квадрупольных приборов в широкую практику. Это устройство
- 12. Комбинация трех квадруполей (QqQ) позволяет использовать несколько режимов тандемной масс-спектрометрии (MС/MС). Молекулярные ионы каждого типа (на
- 13. Процедура повторяется со вторым молекулярным ионом (например, розовые шарики на рис.) и так далее. Когда будет
- 14. Хроматомасс-спектрометрия В ХМС масс-спектрометр соединен со специальным прибором (хроматогрофом), позволяющим разделять разные органические соединения в пространстве
- 15. Хроматомасс-спектрометрия На рисунке изображена схема газового хроматографа (справа) и масс-спектрометра(слева), соединенных вместе. Жидкая проба ( объем
- 16. В 1 секунду современные МС позволяют измерять от ~ 0.5 до сотни масс-спектров. Характерные времена прохождения
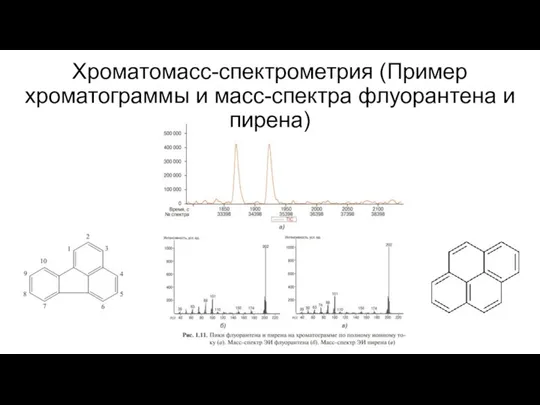
- 17. Хроматомасс-спектрометрия (Пример хроматограммы и масс-спектра флуорантена и пирена)
- 18. ГХ×ГХ/МС В случае очень сложных смесей органических соединений, например нефтепродуктов, или необходимости полного разделения соединений с
- 19. ГХ×ГХ/МС (Пример) На рисунке по оси Z – интенсивность для ионов с m/z = 55, по
- 20. Интерпретация масс-спектров
- 21. Молекулярный ион Масса М+∙ - молекулярная масса соединения, т.е. обычно самое большое m/z. Соотношение изотопных пиков
- 22. Степень ненасыщенности (число циклов и кратных связей) R – Степень ненасыщенности (число циклов и кратных связей)
- 23. Степень ненасыщенности (число циклов и кратных связей) C5H9N3O2ClBr х = 5, у = 9+1+1=11, z =
- 24. Молекулярный ион Необходимые, но недостаточные условия для установления молекулярного иона: Ион должен иметь самую большую массу
- 25. Степень ненасыщенности (число циклов и кратных связей) Все элементы с валентностью 1 заменяются на СН3 группы,
- 26. Выбросы нейтральных частиц Обычно М+∙ легко теряет молекулы СО, СО2, Н2О, С2Н4, радикалы Alk∙, H∙, Hal∙,
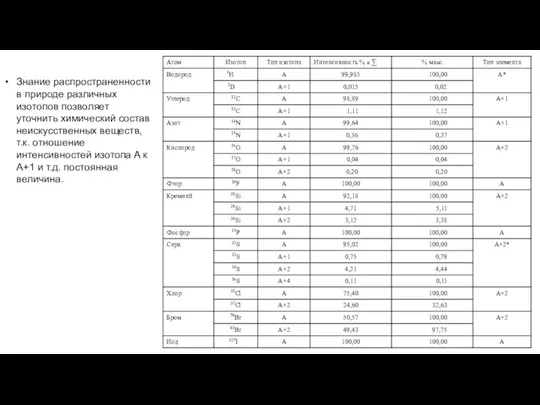
- 27. Знание распространенности в природе различных изотопов позволяет уточнить химический состав неискусственных веществ, т.к. отношение интенсивностей изотопа
- 28. Определение элементного состава соединения следует начинать с пика М+2. Необходимо учитывать, что в случае присутствия в
- 29. Ион, содержащий n атомов А+2 элемента будет характеризоваться n+1 пиками, отстоящими друг от друга на 2
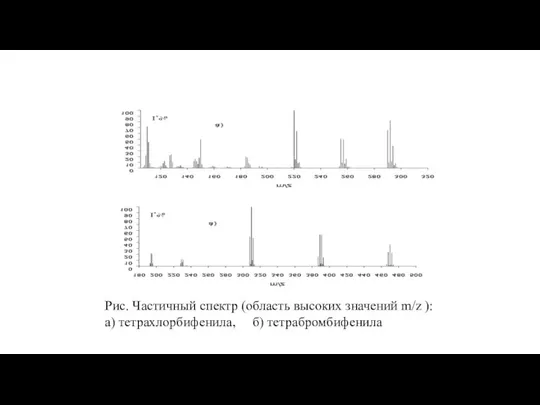
- 30. Рис. Частичный спектр (область высоких значений m/z ): а) тетрахлорбифенила, б) тетрабромбифенила
- 31. Если в ионе имеется два разных А+2 элемента, расчет интенсивностей сигналов в мультиплете осуществляется матричным перемножением.
- 32. А+1 элементы А+1 элементы – углерод, водород и азот, причем на практике водород можно исключить, так
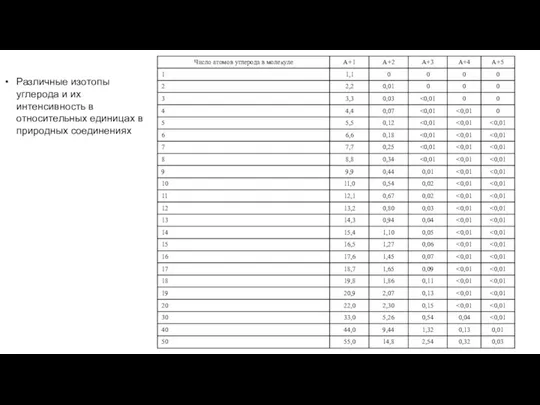
- 33. Различные изотопы углерода и их интенсивность в относительных единицах в природных соединениях
- 34. Величину изотопного пика за счет присутствия в молекуле нескольких изотопов углерода 13С легко рассчитать самостоятельно. Интенсивность
- 35. Масс-спектр соединения с молекулярной массой 94 Дальтона
- 36. Азотное правило Если молекула не содержит атомов азота, или содержит четное число атомов азота, ее молекулярный
- 37. Азот является А+1 элементом, причем природная распространенность изотопа 15N составляет примерно 0,4% от 14N. Поскольку помимо
- 38. Фрагментные ионы Осколочные ионы, перегруппировочные ионы Все важнейшие фрагментные ионы можно разделить на три типа: Наиболее
- 39. Гомологические серии ионов ряда классов органических соединений
- 40. Выбросы простейших нейтральных частиц Самые простые, но важные заключения можно сделать на основании выбросов нейтральных фрагментов
- 41. Использование дополнительной масс-спектральной информации Отсутствие пика молекулярного иона в спектре электронной ионизации - получение спектра каким-либо
- 42. Порядок действий при интерпретации масс-спектров: 1. Изучить всю имеющуюся информацию о веществе (спектральную, химическую, историю появления
- 44. Скачать презентацию





































 Презентация по Химии "Презентація про мене" - скачать смотреть
Презентация по Химии "Презентація про мене" - скачать смотреть  Фосфор
Фосфор Хімія у створенні нових матеріалів та побуті
Хімія у створенні нових матеріалів та побуті ОГЭ, вопрос 16 1-4
ОГЭ, вопрос 16 1-4 Начальные этапы обмена липидов
Начальные этапы обмена липидов Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл
Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно
Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно Щавелевая кислота
Щавелевая кислота Хімічний елемент Літій
Хімічний елемент Літій Кислородные соединения азота. Азотная кислота
Кислородные соединения азота. Азотная кислота Предельные одноатомные спирты
Предельные одноатомные спирты Серебра нитрат и другие препараты серебра. Ртути окись желтая
Серебра нитрат и другие препараты серебра. Ртути окись желтая Посвящение в химики!
Посвящение в химики! Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4)
Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4) Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы ТБ в школе и в быту
ТБ в школе и в быту Твердые тела и их свойства
Твердые тела и их свойства  Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Азотсодержащие органические соединения
Азотсодержащие органические соединения Lekcii_ - 2017-lech_ped 11
Lekcii_ - 2017-lech_ped 11 Юные химики
Юные химики Курсовая работа. Влияние микроэлементов на физиологические процессы
Курсовая работа. Влияние микроэлементов на физиологические процессы Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Electrochemistry. Oxidation-reduction equilibrium in water solutions
Electrochemistry. Oxidation-reduction equilibrium in water solutions Презентация по Химии "Углерод" - скачать смотреть
Презентация по Химии "Углерод" - скачать смотреть  Химически опасные объекты (ХОО)
Химически опасные объекты (ХОО) Теория химического строения А. М. Бутлерова. Часть III
Теория химического строения А. М. Бутлерова. Часть III Платина. Свойства
Платина. Свойства