Содержание
- 2. Згідно неї існують: Ультрамікропори – ширина до 2 молекулярних діаметрів. В цих порах адсорбційний потенціал в
- 3. Для стандартного адсорбату: W=Woexp(-kεo2)= Woexp(-kε2/β2) де Wo – об’єм мікропор. 4. Зв’язок між W і ε
- 4. Визначення поверхні і обʹєму мікропор t-plot Метод аналізу ізотерм згідно з яким обирається ділянка ізотерми після
- 5. Вплив мікропор на адсорбцію Різниця в адсорбції гелію та азоту на пористих вуглецевих волокнах, що пов’язана
- 6. Методи основані на збільшенні теплоти адсорбції (збільшення потенційної енергії) в порах порівняно з пласкою поверхнею. Існують
- 7. Різниця в адсорбції СО2 (273К) lmin=0.28 нм та N2 (77К) lmin=0.3 нм: 1. Хімічна взаємодія СО2
- 9. Скачать презентацию
Згідно неї існують:
Ультрамікропори – ширина до 2 молекулярних діаметрів. В
Згідно неї існують:
Ультрамікропори – ширина до 2 молекулярних діаметрів. В
Супермікропори – до 5 молекулярних діаметрів проміжне значення адсорбційного потенціалу. Заповнення цих пор відбувається практично повністю в межах відносних тисків 0,02-0,2.
Характерний І тип ізотерми. (Граничне значення питомої поверхні 1700 м2/г – шари графену, покриті з обох сторін адсорбатом)
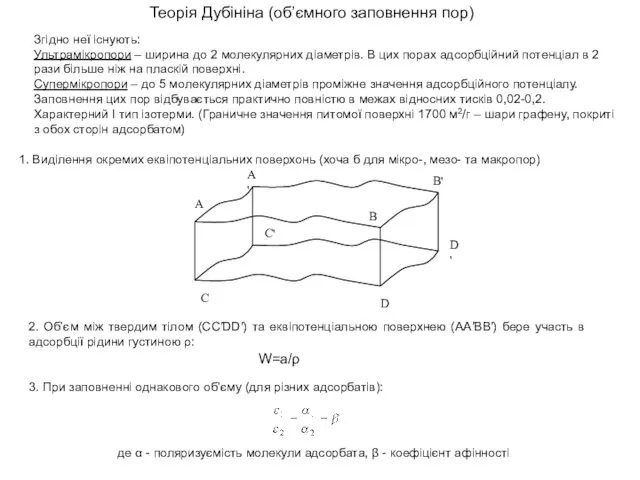
1. Виділення окремих еквіпотенціальних поверхонь (хоча б для мікро-, мезо- та макропор)
Теорія Дубініна (об’ємного заповнення пор)
2. Об’єм між твердим тілом (CC′DD′) та еквіпотенціальною поверхнею (AA′BB′) бере участь в адсорбції рідини густиною ρ:
W=a/ρ
3. При заповненні однакового об’єму (для різних адсорбатів):
де α - поляризуємість молекули адсорбата, β - коефіцієнт афінності
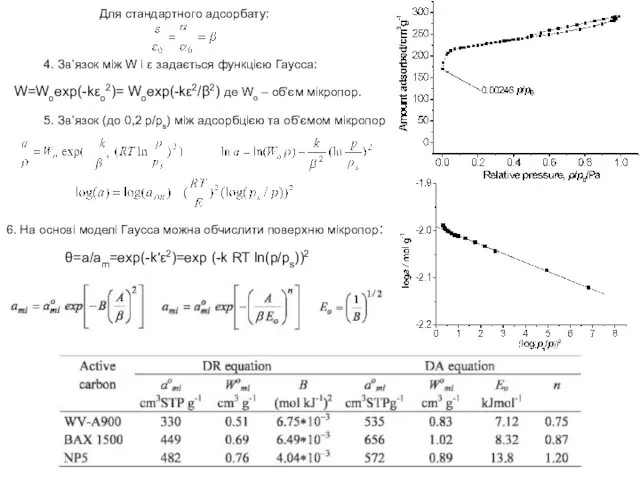
Для стандартного адсорбату:
W=Woexp(-kεo2)= Woexp(-kε2/β2) де Wo – об’єм мікропор.
4. Зв’язок між
Для стандартного адсорбату:
W=Woexp(-kεo2)= Woexp(-kε2/β2) де Wo – об’єм мікропор.
4. Зв’язок між
5. Зв’язок (до 0,2 p/ps) між адсорбцією та об’ємом мікропор
6. На основі моделі Гаусса можна обчислити поверхню мікропор:
θ=a/am=exp(-k′ε2)=exp (-k RT ln(p/ps))2
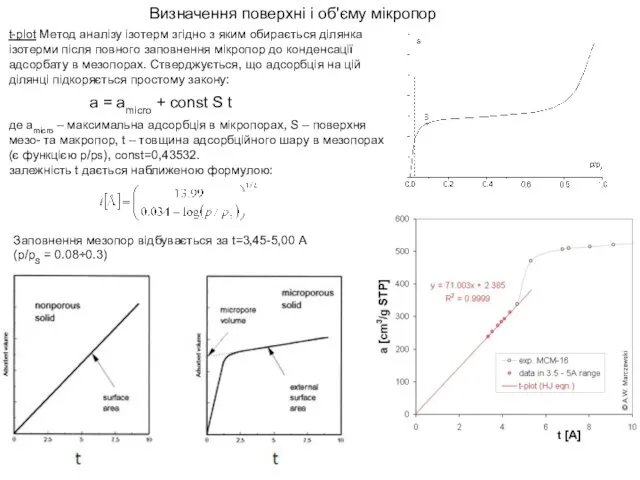
Визначення поверхні і обʹєму мікропор
t-plot Метод аналізу ізотерм згідно з яким
Визначення поверхні і обʹєму мікропор
t-plot Метод аналізу ізотерм згідно з яким
a = amicro + const S t
де amicro – максимальна адсорбція в мікропорах, S – поверхня мезо- та макропор, t – товщина адсорбційного шару в мезопорах (є функцією p/ps), const=0,43532.
залежність t дається наближеною формулою:
Заповнення мезопор відбувається за t=3,45-5,00 А
(p/pS = 0.08÷0.3)
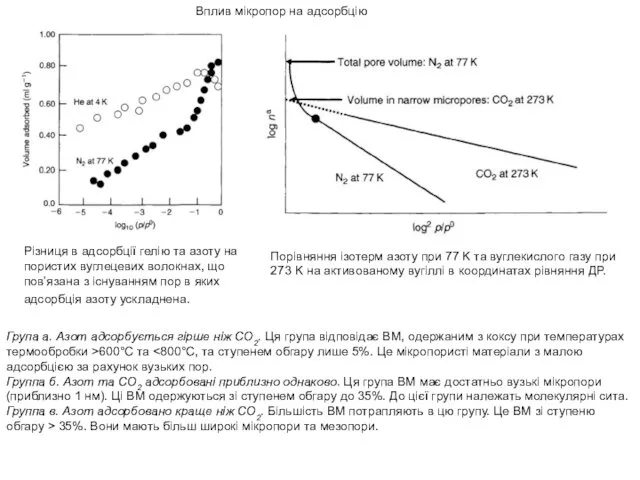
Вплив мікропор на адсорбцію
Різниця в адсорбції гелію та азоту на пористих
Вплив мікропор на адсорбцію
Різниця в адсорбції гелію та азоту на пористих
Порівняння ізотерм азоту при 77 K та вуглекислого газу при 273 K на активованому вугіллі в координатах рівняння ДР.
Група а. Азот адсорбується гірше ніж СО2. Ця група відповідає ВМ, одержаним з коксу при температурах термообробки >600°C та <800°C, та ступенем обгару лише 5%. Це мікропористі матеріали з малою адсорбцією за рахунок вузьких пор.
Группа б. Азот та СО2 адсорбовані приблизно однаково. Ця група ВМ має достатньо вузькі мікропори (приблизно 1 нм). Ці ВМ одержуються зі ступенем обгару до 35%. До цієї групи належать молекулярні сита.
Группа в. Азот адсорбовано краще ніж СО2. Більшість ВМ потрапляють в цю групу. Це ВМ зі ступеню обгару > 35%. Вони мають більш широкі мікропори та мезопори.
Методи основані на збільшенні теплоти адсорбції (збільшення потенційної енергії) в порах
Методи основані на збільшенні теплоти адсорбції (збільшення потенційної енергії) в порах
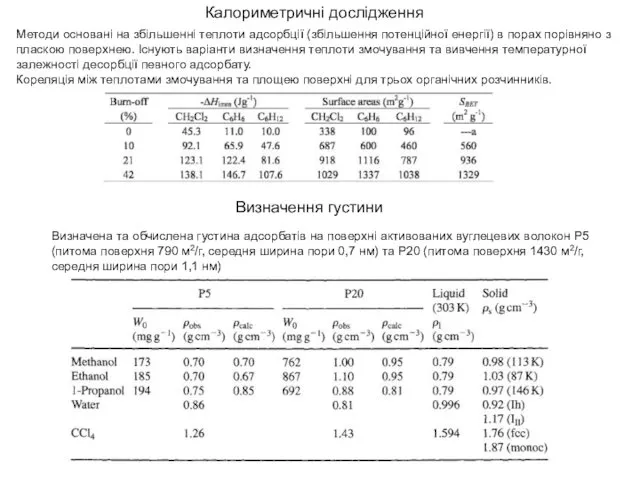
Кореляція між теплотами змочування та площею поверхні для трьох органічних розчинників.
Калориметричні дослідження
Визначена та обчислена густина адсорбатів на поверхні активованих вуглецевих волокон Р5 (питома поверхня 790 м2/г, середня ширина пори 0,7 нм) та Р20 (питома поверхня 1430 м2/г, середня ширина пори 1,1 нм)
Визначення густини
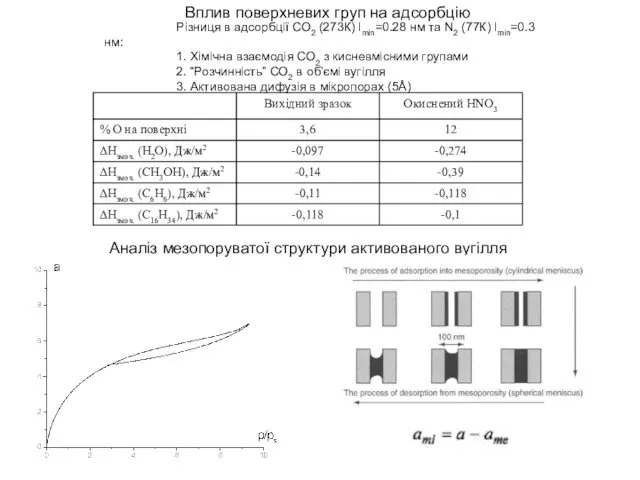
Різниця в адсорбції СО2 (273К) lmin=0.28 нм та N2 (77К) lmin=0.3
Різниця в адсорбції СО2 (273К) lmin=0.28 нм та N2 (77К) lmin=0.3
1. Хімічна взаємодія СО2 з кисневмісними групами
2. “Розчинність” СО2 в об’ємі вугілля
3. Активована дифузія в мікропорах (5Å)
Вплив поверхневих груп на адсорбцію
Аналіз мезопоруватої структури активованого вугілля
 Кейс № 4.1 одежда для металла
Кейс № 4.1 одежда для металла Презентация по Химии "Этот многоликий Кальцит" - скачать смотреть
Презентация по Химии "Этот многоликий Кальцит" - скачать смотреть  Хлористый водород
Хлористый водород Предельные углеводороды. Алканы и циклоалканы. Лекция № 2
Предельные углеводороды. Алканы и циклоалканы. Лекция № 2 Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Химические свойства кислот с позиции теории электролитической диссоциации
Химические свойства кислот с позиции теории электролитической диссоциации Химическая связь 11 класс
Химическая связь 11 класс  6 классов ферментов и тривиальные названия некоторых основных групп
6 классов ферментов и тривиальные названия некоторых основных групп Электродные потенциалы. Окислительно-восстановительные потенциалы. Потенциометрия в медицинской практике
Электродные потенциалы. Окислительно-восстановительные потенциалы. Потенциометрия в медицинской практике Характеристика азота как химического элемента и простого вещества. Урок химии в 9 классе.
Характеристика азота как химического элемента и простого вещества. Урок химии в 9 классе. Тепловой эффект сгорания топлива
Тепловой эффект сгорания топлива КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф.
КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф. Химические волокна
Химические волокна Строение атома
Строение атома Бинарный интегрированный урок (география + химия) . 8 класс
Бинарный интегрированный урок (география + химия) . 8 класс Компоненты нефти, газов и нефтепродуктов. Состав, строение, свойства. Насыщенные углеводороды
Компоненты нефти, газов и нефтепродуктов. Состав, строение, свойства. Насыщенные углеводороды Диаграммы Пурбе
Диаграммы Пурбе Лимонная кислота
Лимонная кислота Металлические сплавы
Металлические сплавы Массообменные процессы
Массообменные процессы Вещества и материалы. Классификация веществ. Индикаторы. 6 класс
Вещества и материалы. Классификация веществ. Индикаторы. 6 класс Осадочные породы. (Лекция 9.2)
Осадочные породы. (Лекция 9.2) Нуклеиновые кислоты
Нуклеиновые кислоты Поделочные или полудрагоценные камни
Поделочные или полудрагоценные камни Определение содержания солей в нефти
Определение содержания солей в нефти Галогены. Галогеноводороды
Галогены. Галогеноводороды Кислотность почвы
Кислотность почвы Масса молекул. Количество вещества
Масса молекул. Количество вещества